摘要:13.A.B.C为 短周期元素.在周期表中所处的位置如右图所示.A.C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等. (1)A.B.C三种元素的名称分别为 . . . (2)B位于元素周期表中第 周期.第 族. (3)C的原子结构示意图为 .C的单质与H2反应的化学方程式为 . (4)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式 . [解析] 依题意.A.B.C为短周期元素.从A.B.C的相对位置看.A.C只能处在第二周期.而B处在第三周期.设A的原子序数为x-1.则C为x+1.B为x+8.则有: (x-1)+x+1=x+8 x=8 所以A.B.C的原子序数分别为7.16.9.对应的元素分别为N.S.F. [答案] 三 ⅥA (3) F2+H2===2HF (4)2NH3+H2SO4===(NH4)2SO4. 完全排满时元素的种数如下表所示: 周期序数 1 2 3 4 5 6 7 元素种数 2 8 8 18 18 32 32
网址:http://m.1010jiajiao.com/timu3_id_86981[举报]
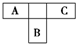 A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.(1)写出A、B、C三种元素的名称分别为
氮
氮
、硫
硫
、氟
氟
;(2)B位于元素周期表中第
三
三
周期,第ⅥA
ⅥA
族;(3)C的原子结构示意图为
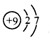
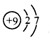
2F2+2H2O═4HF+O2
2F2+2H2O═4HF+O2
;(4)比较B、C的原子半径;B
>
>
C,写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式2NH3+H2SO4═(NH4)2SO4
2NH3+H2SO4═(NH4)2SO4
.A、B、C为短周期元素,在周期表中所处位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.
(1)B位于元素周期表第
(2)A元素形成的单质的电子式为:
 .
.
(3)在A B、C的气态氢化物中最稳定的是
(4)C的离子结构示意图为
 .
.
(5)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式
查看习题详情和答案>>
| A | C | |
| B |
三
三
周期,第ⅥA
ⅥA
族.(2)A元素形成的单质的电子式为:


(3)在A B、C的气态氢化物中最稳定的是
HF
HF
.(4)C的离子结构示意图为


(5)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式
2NH3+H2SO4=( NH4)2SO4
2NH3+H2SO4=( NH4)2SO4
.A、B、C为短周期元素,在周期表中所处的位置如图所示.A、C两元素的原子核外电子数之和等于B原子的质子数.B原子核内质子数和中子数相等.
(1)A、B、C三种元素的符号分别为
(2)B元素位于元素周期表中第
(3)C的原子结构示意图为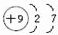
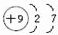 ,
,
(4)用元素符号将 A、B、C三种原子按半径从大到小排列
查看习题详情和答案>>
| A | C | |
| B |
氮
氮
、硫
硫
、氟
氟
;(2)B元素位于元素周期表中第
三
三
周期、第ⅥA
ⅥA
族;(3)C的原子结构示意图为
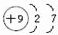
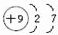
(4)用元素符号将 A、B、C三种原子按半径从大到小排列
S>N>F
S>N>F
.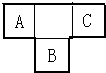 A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.
A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.(1)写出A、B、二种元素的名称
(2)B元素位于元素周期表中第
(3)C的原子结构示意图为
(4)由元素A、C及氢元素形成的化合物中含有的化学键的类型有
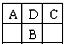 A、B、C为短周期元素,在周期表中如图所示:A、C两种元素的原子核外电子数之和等于B原子的核电荷数.有关说法错误的是( )
A、B、C为短周期元素,在周期表中如图所示:A、C两种元素的原子核外电子数之和等于B原子的核电荷数.有关说法错误的是( )| A、A的氧化物有多种形式 | B、B最高价氧化物对应的水化物是一种弱酸 | C、C的氢化物比HCl稳定 | D、D元素形成的单质不止一种 |