摘要:22.某学生利用以下装置探究氯气与氨气之间的反应.其中A.F分别为氨气和氯气的发生装置.C为纯净干燥的氯气与氨气反应的装置.. 请回答下列问题: (1)装置F中发生反应的离子方程式为 , (2)B装置的名称是 , (3)E装置的作用 , (4)装置C内出现浓厚的白烟并在容器内壁凝结.另一生成物是空气的主要成分之一.请写出反应的化学方程式: , (5)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体.如何处理? . 解析:F.E.D是制取纯净干燥Cl2的装置.E吸收Cl2中的HCl气体.D干燥Cl2.B的作用是干燥NH3.(4)C中的白烟是NH4Cl.另一产物则是N2.(5)黄绿色气体为Cl2.需用碱液吸收. 答案:(1)4H++2Cl-+MnO2△Mn2++Cl2↑+2H2O 除去氯气中的氯化氢 (4)3Cl2+8NH3===N2+6NH4Cl (5)在G处连接导管.直接把尾气通入盛有烧碱溶液的烧杯中.
网址:http://m.1010jiajiao.com/timu3_id_84428[举报]
某学生利用以下装置探究氯气与氨之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨反应的装置.

请回答下列问题:
(1)装置F中发生反应的化学方程式为
(2)装置B中仪器的名称是
(3)往装置A的烧瓶内加入粉末状固体的操作是
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.写出反应的化学方程式
当有a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗数常数为
(5)将用F、E、D装置制得的氯气通入含74gCa(OH)2的石灰乳中,最多可制得漂白粉
查看习题详情和答案>>

请回答下列问题:
(1)装置F中发生反应的化学方程式为
MnO2+4HCl(浓)
Cl2↑+MnCl2+2H2O
| ||
MnO2+4HCl(浓)
Cl2↑+MnCl2+2H2O
.
| ||
(2)装置B中仪器的名称是
干燥管
干燥管
;装置E的作用是除去氯气中的氯化氢
除去氯气中的氯化氢
.(3)往装置A的烧瓶内加入粉末状固体的操作是
将烧瓶横放,把盛有药瓶的药匙或纸槽伸入瓶底,再将烧瓶竖起
将烧瓶横放,把盛有药瓶的药匙或纸槽伸入瓶底,再将烧瓶竖起
.(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.写出反应的化学方程式
8NH3+3Cl2═6NH4Cl+N2
8NH3+3Cl2═6NH4Cl+N2
.当有a mol氯气参加反应时,转移的电子总数为b个,则阿伏加德罗数常数为
=
| b |
| 2a |
=
mol-1 (用含a、b的代数式表示).| b |
| 2a |
(5)将用F、E、D装置制得的氯气通入含74gCa(OH)2的石灰乳中,最多可制得漂白粉
127
127
g.某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置.
请回答下列问题:
(1)装置F中发生反应的离子方程式为
(2)B装置的作用
(3)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应的化学方程式:
计算生成2.8gN2转移电子数为
(4)G中的尾气可用
查看习题详情和答案>>
请回答下列问题:

(1)装置F中发生反应的离子方程式为
MnO2+4H++2C1-
Mn2++C12↑+2H2O.
| ||
MnO2+4H++2C1-
Mn2++C12↑+2H2O.
.
| ||
(2)B装置的作用
干燥氨气
干燥氨气
.(3)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应的化学方程式:
3Cl2+8NH3=N2+6NH4Cl
3Cl2+8NH3=N2+6NH4Cl
(写总式);计算生成2.8gN2转移电子数为
0.6NA
0.6NA
(NA代表阿伏伽德罗常数).(4)G中的尾气可用
NaOH
NaOH
溶液吸收.
某学生利用以下装置探究氯气与氨气之间的反应.其中 A、F 分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.
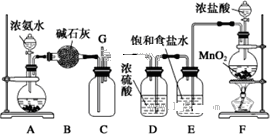
请回答下列问题:
(1)装置F中发生反应的离子方程式为 .
(2)装置A的烧瓶中可装试剂为: .
(3)装置A还可以用来制备下列哪些气体 (选填字母)
A.O2 B.HCl C.SO2 D.H2
(4)通入C装置的两根导管左边较长右边较短,目的是 .
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.
写出反应的化学方程式: ,该反应中氧化剂和还原剂的物质的量之比为 .
查看习题详情和答案>>

请回答下列问题:
(1)装置F中发生反应的离子方程式为
(2)装置A的烧瓶中可装试剂为:
(3)装置A还可以用来制备下列哪些气体
A.O2 B.HCl C.SO2 D.H2
(4)通入C装置的两根导管左边较长右边较短,目的是
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.
写出反应的化学方程式:
某学生利用以下装置探究纯净干燥的氯气与氨气之间的反应.

回答下列问题:
(1)根据下列所给试剂,选择制取氨气的装置是(填对应字母) ;写出制备氯气的离子反应方程式 .
二氧化锰、碱石灰、浓盐酸、浓氨水、烧碱、生石灰
(2)根据实验目的,所选装置的连接顺序为(填装置的接口字母): 接 , 接( f ),( g )接 , 接 , 接 ;其中,G装置的作用是 .
(3)氯气和氨气在常温下相混合就会发生反应生成氯化铵和氮气,该反应的化学方程式为: ;其中,氧化剂与还原剂的物质的量之比是 .
(4)请你评价此套装置有何缺点 .
查看习题详情和答案>>

回答下列问题:
(1)根据下列所给试剂,选择制取氨气的装置是(填对应字母)
二氧化锰、碱石灰、浓盐酸、浓氨水、烧碱、生石灰
(2)根据实验目的,所选装置的连接顺序为(填装置的接口字母):
(3)氯气和氨气在常温下相混合就会发生反应生成氯化铵和氮气,该反应的化学方程式为:
(4)请你评价此套装置有何缺点
(A)针对以下A~D四个涉及H2O2的反应(未配平),填写空白:
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2+H2O
C.H2O2→H2O+O2
D. H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是(填代号)
(2)H2O2既体现氧化性又体现还原性的反应是(填代号)
(3)H2O2体现弱酸性的反应是(填代号)
(B)某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.

请回答下列问题:
(1)装置F中发生反应的离子方程式为
(2)装置A的烧瓶中可装试剂
(3)B装置的名称是
(4)通入C装置的两根导管左边较长、右边较短,目的是
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应的化学方程式:
查看习题详情和答案>>
A.Na2O2+HCl→H2O2+NaCl
B.Ag2O+H2O2→Ag+O2+H2O
C.H2O2→H2O+O2
D. H2O2+Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O
(1)H2O2仅体现氧化性的反应是(填代号)
D
D
,该反应配平的化学方程式为3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
3H2O2+Cr2(SO4)3+10KOH═2K2CrO4+3K2SO4+8H2O
.(2)H2O2既体现氧化性又体现还原性的反应是(填代号)
C
C
.(3)H2O2体现弱酸性的反应是(填代号)
A
A
,其理由为这一反应可看作是强酸制取弱酸的反应
这一反应可看作是强酸制取弱酸的反应
.(B)某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置.

请回答下列问题:
(1)装置F中发生反应的离子方程式为
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
.
| ||
(2)装置A的烧瓶中可装试剂
生石灰或固体氢氧化钠
生石灰或固体氢氧化钠
.(3)B装置的名称是
球形干燥管
球形干燥管
;E装置的作用除去氯气中的HCl
除去氯气中的HCl
.(4)通入C装置的两根导管左边较长、右边较短,目的是
使密度大的氯气与密度小的氨气较快地均匀混合
使密度大的氯气与密度小的氨气较快地均匀混合
.(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应的化学方程式:
3Cl2+8NH3═N2+6NH4Cl
3Cl2+8NH3═N2+6NH4Cl
.