��Ŀ����
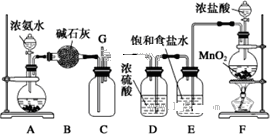
ijѧ����������װ��̽�������백֮��ķ�Ӧ������A��F�ֱ�Ϊ�����������ķ���װ�ã�CΪ��������������백��Ӧ��װ�ã�

��ش��������⣺
��1��װ��F�з�����Ӧ�Ļ�ѧ����ʽΪ
��2��װ��B��������������
��3����װ��A����ƿ�ڼ����ĩ״����IJ�����
��4��װ��C�ڳ���Ũ��İ��̲��������ڱ����ᣬ��һ�������ǿ�������Ҫ�ɷ�֮һ��д����Ӧ�Ļ�ѧ����ʽ
����a mol�����μӷ�Ӧʱ��ת�Ƶĵ�������Ϊb�������ӵ���������Ϊ
��5������F��E��Dװ���Ƶõ�����ͨ�뺬74gCa��OH��2��ʯ�����У������Ƶ�Ư��

��ش��������⣺
��1��װ��F�з�����Ӧ�Ļ�ѧ����ʽΪ
MnO2+4HCl��Ũ��
Cl2��+MnCl2+2H2O
| ||
MnO2+4HCl��Ũ��
Cl2��+MnCl2+2H2O
��
| ||
��2��װ��B��������������
�����
�����
��װ��E����������ȥ�����е��Ȼ���
��ȥ�����е��Ȼ���
����3����װ��A����ƿ�ڼ����ĩ״����IJ�����
����ƿ��ţ���ʢ��ҩƿ��ҩ��ֽ������ƿ�ף��ٽ���ƿ����
����ƿ��ţ���ʢ��ҩƿ��ҩ��ֽ������ƿ�ף��ٽ���ƿ����
����4��װ��C�ڳ���Ũ��İ��̲��������ڱ����ᣬ��һ�������ǿ�������Ҫ�ɷ�֮һ��д����Ӧ�Ļ�ѧ����ʽ
8NH3+3Cl2�T6NH4Cl+N2
8NH3+3Cl2�T6NH4Cl+N2
������a mol�����μӷ�Ӧʱ��ת�Ƶĵ�������Ϊb�������ӵ���������Ϊ
=
| b |
| 2a |
=
mol-1 ���ú�a��b�Ĵ���ʽ��ʾ����| b |
| 2a |
��5������F��E��Dװ���Ƶõ�����ͨ�뺬74gCa��OH��2��ʯ�����У������Ƶ�Ư��
127
127
g����������1���������̿��Ժ�Ũ�����ڼ��������������������������̺�ˮ��
��2������ͼ���֪BΪ����ܣ�����ʳ��ˮ���Գ�ȥ�����е��Ȼ������ʣ�
��3������ƿ�мӹ����ĩҪ��ҩ��ֽ�ۣ�Ҫ����ƿ��ֹ��ĩ����ƿ���ϣ�
��4���������֪������ӦΪ���������������Ȼ�狀͵������ɷ�Ӧ����ʽ����֪Cl2��2NH4Cl�����ϼ۽��͵õ�2�����ӣ�����1molCl2��2mol���ӣ���������������ӵ����ʵ������ٸ��ݵ��ӵĸ������NA��
��5�������������Ƶ����ʵ����ͷ�Ӧ����ʽ���Ư�۵�������
��2������ͼ���֪BΪ����ܣ�����ʳ��ˮ���Գ�ȥ�����е��Ȼ������ʣ�
��3������ƿ�мӹ����ĩҪ��ҩ��ֽ�ۣ�Ҫ����ƿ��ֹ��ĩ����ƿ���ϣ�
��4���������֪������ӦΪ���������������Ȼ�狀͵������ɷ�Ӧ����ʽ����֪Cl2��2NH4Cl�����ϼ۽��͵õ�2�����ӣ�����1molCl2��2mol���ӣ���������������ӵ����ʵ������ٸ��ݵ��ӵĸ������NA��
��5�������������Ƶ����ʵ����ͷ�Ӧ����ʽ���Ư�۵�������
����⣺��1���������̿��Ժ�Ũ�����ڼ��������������������������̺�ˮ���䷴Ӧ����ʽΪ��MnO2+4HCl��Ũ��
Cl2��+MnCl2+2H2O���ʴ�Ϊ��MnO2+4HCl��Ũ��
Cl2��+MnCl2+2H2O��
��2������ͼ���֪BΪ����ܣ�����ʳ��ˮ���Գ�ȥ�����е��Ȼ������ʣ��ʴ�Ϊ������ܣ���ȥ�����е��Ȼ��⣻
��3������ƿ�мӹ����ĩҪ��ҩ��ֽ�ۣ�Ҫ����ƿ��ֹ��ĩ����ƿ���ϣ�
�ʴ�Ϊ������ƿ��ţ���ʢ��ҩƿ��ҩ��ֽ������ƿ�ף��ٽ���ƿ����
��4��������������Ӧ���ɰ����Ȼ�狀Ϳ�������Ҫ�ɷ�֮һ��������8NH3+3Cl2�T6NH4Cl+N2��
�ɷ�Ӧ����ʽ��֪Cl2��2NH4Cl�����ϼ۽��͵õ�2�����ӣ�����1molCl2��2mol���ӣ����Ե���a mol�����μӷ�Ӧʱ��ת�Ƶĵ��ӵ����ʵ���Ϊ2amol����֪ת�Ƶĵ�������Ϊb������N=n?NA����b=2a?NA������NA=
���ʴ�Ϊ��8NH3+3Cl2�T6NH4Cl+N2��
��
��5���������Ƶ����ʵ�����n=
=1mol�����Ը��ݷ�Ӧʽ2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��֪�������ɵ�CaCl2��Ca��ClO��2��0.5mol�����������Ƶ�Ư�۵�������m=m��CaCl2��+m��Ca��ClO��2��=0.5mol��111g/mol+0.5mol��143g/mol=127g��
�ʴ�Ϊ��127g��
| ||
| ||
��2������ͼ���֪BΪ����ܣ�����ʳ��ˮ���Գ�ȥ�����е��Ȼ������ʣ��ʴ�Ϊ������ܣ���ȥ�����е��Ȼ��⣻
��3������ƿ�мӹ����ĩҪ��ҩ��ֽ�ۣ�Ҫ����ƿ��ֹ��ĩ����ƿ���ϣ�
�ʴ�Ϊ������ƿ��ţ���ʢ��ҩƿ��ҩ��ֽ������ƿ�ף��ٽ���ƿ����
��4��������������Ӧ���ɰ����Ȼ�狀Ϳ�������Ҫ�ɷ�֮һ��������8NH3+3Cl2�T6NH4Cl+N2��
�ɷ�Ӧ����ʽ��֪Cl2��2NH4Cl�����ϼ۽��͵õ�2�����ӣ�����1molCl2��2mol���ӣ����Ե���a mol�����μӷ�Ӧʱ��ת�Ƶĵ��ӵ����ʵ���Ϊ2amol����֪ת�Ƶĵ�������Ϊb������N=n?NA����b=2a?NA������NA=
| b |
| 2a |
| b |
| 2a |
��5���������Ƶ����ʵ�����n=
| 74g |
| 74g/mol |
�ʴ�Ϊ��127g��
���������⿼��ѧ��ʵ������ȡ�����������ķ�����������ʣ�������ԭ��Ӧ�����ݷ���ʽ�ļ���ȷ����֪ʶ����Ƕȹ㣬Ҫ��ѧ�����з����ͽ��������������Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ