网址:http://m.1010jiajiao.com/timu3_id_82458[举报]
已知甲、乙、丙均为常见气体,其中甲在空气中含量最多,乙在相同条件下密度最小,丙有刺激性气味,且一个丙分子由四个原子构成.
(1)实验室中可用下图A或B装置与相应的药品制得丙.
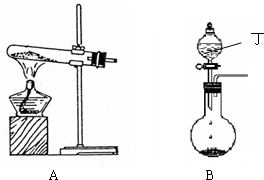
①A中试管内反应的化学方程式是______.
②B中分液漏斗内盛放的物质丁是______,圆底烧瓶内的物质是______.(均填名称)
(2)工业上将甲和乙在高温、高压、催化剂的条件下制取丙.下图是甲和乙反应过程中能量变化图:
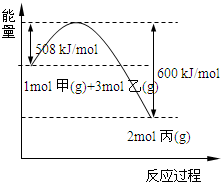
该反应的热化学方程式是______.
(3)丙在氧气中燃烧的反应是置换反应,该反应的化学方程式是______.
(4)①将丙和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式是______.
②为了验证上述晶体既不是NH4HCO3、也不是NaCl而是NaHCO3,设计实验方案如下,完成下列部分实验报告:
| 实验操作 | 实验现象 | 结论 | 相应的离子方程式 |
| 取少量晶体于试管中,充分加热 | 试管内有固体剩余 | ______ | ______ |
| ______ | 固体全部溶解,有气泡产生 | ______ | ______ |
(1)实验室中可用下图A或B装置与相应的药品制得丙.
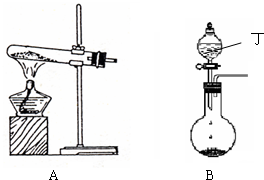
①A中试管内反应的化学方程式是______.
②B中分液漏斗内盛放的物质丁是______,圆底烧瓶内的物质是______.(均填名称)
(2)工业上将甲和乙在高温、高压、催化剂的条件下制取丙.下图是甲和乙反应过程中能量变化图:
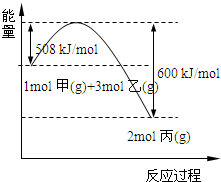
该反应的热化学方程式是______.
(3)丙在氧气中燃烧的反应是置换反应,该反应的化学方程式是______.
(4)①将丙和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式是______.
②为了验证上述晶体既不是NH4HCO3、也不是NaCl而是NaHCO3,设计实验方案如下,完成下列部分实验报告:
| 实验操作 | 实验现象 | 结论 | 相应的离子方程式 |
| 取少量晶体于试管中,充分加热 | 试管内有固体剩余 | ______ | ______ |
| ______ | 固体全部溶解,有气泡产生 | ______ | ______ |
已知甲、乙、丙均为常见气体,其中甲在空气中含量最多,乙在相同条件下密度最小,丙有刺激性气味,且一个丙分子由四个原子构成。
(1)实验室中可用下图A或B装置与相应的药品制得丙。
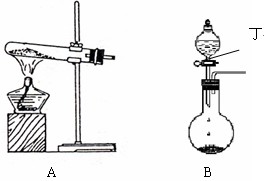
① A中试管内反应的化学方程式是 。
② B中分液漏斗内盛放的物质丁是 ,圆底烧瓶内的物质是 。(均填名称)
(2)工业上将甲和乙在高温、高压、催化剂的条件下制取丙。下图是甲和乙反应过程中能量变化图:
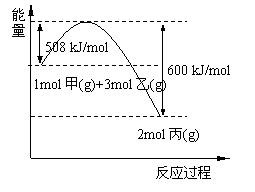 |
该反应的热化学方程式是 。
(3)丙在氧气中燃烧的反应是置换反应,该反应的化学方程式是 。
(4)① 将丙和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式是 。
②为了验证上述晶体既不是NH4HCO3、也不是NaCl而是NaHCO3,设计实验方案如下,完成下列部分实验报告:
实验操作 | 实验现象 | 结论 | 相应的离子方程式 |
取少量晶体于试管中,充分加热 | 试管内有固体剩余 |
|
|
| 固体全部溶解,有气泡产生 |
|
|
(5)若用(1)中得A制取丙,并用园底烧瓶通过排气法收集丙(标准状况),然后进行喷泉实验。当水进入到烧瓶体积得3/5时,液面不再上升,此时立即关闭止水夹,烧瓶内溶液中溶质的物质的量浓度是 mol/L(精确0.001)。 查看习题详情和答案>>
(1)实验室中可用下图A或B装置与相应的药品制得丙.
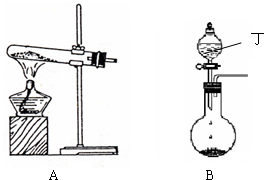
①A中试管内反应的化学方程式是
| ||
| ||
②B中分液漏斗内盛放的物质丁是
(2)工业上将甲和乙在高温、高压、催化剂的条件下制取丙.下图是甲和乙反应过程中能量变化图:
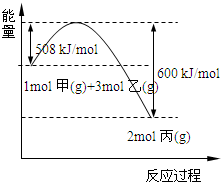
该反应的热化学方程式是
(3)丙在氧气中燃烧的反应是置换反应,该反应的化学方程式是
| ||
| ||
(4)①将丙和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式是
②为了验证上述晶体既不是NH4HCO3、也不是NaCl而是NaHCO3,设计实验方案如下,完成下列部分实验报告:
| 实验操作 | 实验现象 | 结论 | 相应的离子方程式 |
| 取少量晶体于试管中,充分加热 | 试管内有固体剩余 | 该晶体不是NH4HCO3 该晶体不是NH4HCO3 |
无离子方程式 无离子方程式 |
向冷却后试管中加入足量盐酸 向冷却后试管中加入足量盐酸 |
固体全部溶解,有气泡产生 | 该晶体不是NaCl是NaHCO3 该晶体不是NaCl是NaHCO3 |
CO32-+2H+=H2O+CO2↑ CO32-+2H+=H2O+CO2↑ |
随着流感季节的到来和N1H1的威胁,疫苗的需求空前高涨。尽管那些疫苗是有效的,但美国密苏里州大学研究人员于2009年12月研究发现,一些非处方药,如阿司匹林等抑制某些酶的药物会影响疫苗的效果。用丙酮为主要原料合成长效缓释阿司匹林的流程如下图。

回答下列问题:
Ⅰ.(1)上述合成C的路线曾用作有机玻璃单体(![]() )合成路线的一部分。现在人们利用最新开发的+2价钯的均相钯催化剂体系,将丙炔在甲醇和一氧化碳存在下,于60℃、6 MPa条件下羰基化,一步制得
)合成路线的一部分。现在人们利用最新开发的+2价钯的均相钯催化剂体系,将丙炔在甲醇和一氧化碳存在下,于60℃、6 MPa条件下羰基化,一步制得![]() ,其化学方程式为: 。
,其化学方程式为: 。
如此改进的优点为: 。
(2)阿司匹林的结构简式为 ,下列物质与阿司匹林互为同分异构体的有 (填字母)。

Ⅱ.某研究性学习小组看了市售阿司匹林的药品说明书,为了验证乙酰水杨酸的官能团和测定阿司匹林的纯度(假设杂质不参加反应),进行了下列实验探究:
(1)阿司匹林有效成分中羧基和酯基官能团的验证

试剂①是________,现象为_________;该方案通过检验乙酰水杨酸水解生成的____________,并通过分析间接验证酯基的存在。
(2)准确称取阿司匹林a g,粉碎并装入锥形瓶,加水溶解,加入标准浓度C1mol/L的氢氧化钠溶液V1mL,煮沸片刻,使其充分反应。冷却后,用酚酞作指示剂,用C2mol/L盐酸滴定,滴定前盐酸体积为V2mL,滴定终点时盐酸体积为V3mL。(已知:滴定反应是,NaOH+HCl=NaCl+H2O,乙酰水杨酸的相对分子质量为180)
①根据上述数据计算该阿司匹林的纯度为 。
②滴定终点判断“标准”是 ;操作过程中在锥形瓶底垫一张白纸,其作用是 。
③下列操作一定会导致测定结果偏高的是 (填字母)。
A.装盐酸前,滴定管未用标准溶液润洗
B.测定盐酸体积时开始仰视读数,最后俯视读数
C.锥形瓶用标准氢氧化钠溶液润洗
D.滴定过程中盐酸溅到瓶外
E.称量样品时,砝码在左边,而样品放在右边
F.用甲基橙代替酚酞作指示剂
查看习题详情和答案>>