摘要:14.某研究性学习小组为研究Cu与浓H2SO4的反应.设计如下实验探究 方案(装置中的固定仪器和酒精灯均未画出). 实验选用细铜丝.98.3% H2SO4.品红溶液.澄清石灰水.CCl4.NaOH溶液等药 品.铜丝被卷成螺旋状.一端没入浓H2SO4中.另一端露置在液面上方. 以下是该学习小组部分交流记录及后续探究实验的记录. 材料一 小组交流摘录 学生1:加热前.无现象发生,加热后.液面下铜丝变黑.产生气泡.有细小黑色颗 粒状物质从铜丝表面进入浓硫酸中.黑色物质是什么?值得探究! 学生2:加热后.我也观察到黑色颗粒状物质.后来逐渐转变为灰白色固体.我想该 灰白色固体极有可能是未溶于浓硫酸的CuSO4. 学生3:你们是否注意到液面以上的铜丝也发黑.而且试管上部内壁有少量淡黄色S 固体凝聚.会不会液面以上的铜丝与硫发生了反应.我查资料发现:2Cu+ S===Cu2S. 材料二 探究实验剪辑 实验1:将光亮的铜丝在酒精灯火焰上灼烧变黑.然后插入稀硫酸中.铜丝重新变得 光亮.溶液呈蓝绿色,将光亮的铜丝置入加热的硫蒸气中变黑.然后插入稀硫酸中 无变化. 实验2:截取浓硫酸液面上方变黑的铜丝.插入稀硫酸中无变化,将浓硫酸液面下方 变黑的铜丝.插入稀硫酸.黑色明显变浅.溶液呈蓝绿色. 实验3:将溶液中的黑色颗粒状物质.经过滤.稀硫酸洗.蒸馏水洗.干燥后放入氧 气流中加热.然后冷却.用电子天平称重发现质量减少10%左右. 根据上述材料回答下列问题: (1)A试管上方的长导管的作用是 , D.E两支试管中CCl4的作用是 . (2)加热过程中.观察到A试管中出现大量白色烟雾.起初部分烟雾在试管上部内壁 析出淡黄色固体物质.在持续加热浓硫酸时.淡黄色固体物质又慢慢地消 失.写出淡黄色固体消失的化学反应方程式: . (3)对A试管中的浓H2SO4和铜丝进行加热.很快发现C试管中品红溶液褪色.但始 终未见D试管中澄清石灰水出现混浊或沉淀.你的猜想是 . (4)根据上述研究.结合所学知识.你认为液面下方铜丝表面的黑色物质成分是 . 解析:本实验的目的是检验铜与浓硫酸反应的产物.(1)长导管的作用是冷凝气体. D.E两支试管中CCl4的作用是防止倒吸.因为产物中的SO2.CO2气体能被碱液完 全吸收.容易产生倒吸现象,(2)出现的淡黄色固体只能是单质硫.消失的原因是被 浓硫酸氧化,(3)中生成了Ca(HSO3)2而不出现沉淀,(4)依据材料二中几个实验可以 推出结论. 答案:(1)冷凝.回流 防止倒吸 (2)S+2H2SO4(浓)3SO2↑+2H2O (3)SO2生成量较大.生成了Ca(HSO3)2溶液 (4)CuO.CuS.Cu2S
网址:http://m.1010jiajiao.com/timu3_id_81300[举报]
某研究性学习小组为研究铁粉与浓硫酸反应所生成气体的成份并测定各气体的含量,进行了如下实验:
实验推测】足量的铁粉与浓硫酸反应能生成SO2和H2两种气体.
(1)该小组作出此推测的理由是: .
【实验准备】a.供选择的药品:铁粉、浓硫酸、氧化铜粉末、0.2mol/L的H2C2O4标准溶液、0.1mol/L的酸性KMnO4标准溶液、酸碱指示剂.
b.实验装置设计及组装(加热及夹持装置均已略去)
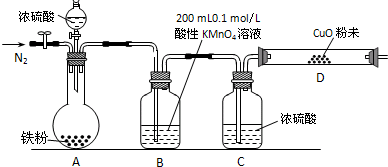
【实验过程及数据处理】
(2)B中发生反应的离子方程式为: .
(3)实验前先通入一段时间的N2,其目的是 .
(4)B、C、D中所盛试剂均足量,则证实生成的气体中同时存在SO2和H2的现象是
.
(5)A中反应结束后,继续通N2使A中生成的气体全部赶出,待B、D中反应完全后,先后三次取用B中反应后的溶液于锥形瓶中,每次取用25mL,用H2C2O4标准溶液进行滴定.
①H2C2O4标准溶液与酸性KMnO4溶液反应的离子方程式如下,请将该方程式完成并配平.
H2C2O4+ MnO4-+ H+= Mn2++ H2O+
②滴定达到终点时的现象是 .
③重复滴定两次,平均每次耗用H2C2O4标准溶液15.63mL,则铁与浓硫酸反应产生的SO2气体
的物质的量为 ;经称量,实验前后装置D的质量减少0.8g,则产生的气体中SO2的体积分数为 .
查看习题详情和答案>>
实验推测】足量的铁粉与浓硫酸反应能生成SO2和H2两种气体.
(1)该小组作出此推测的理由是:
【实验准备】a.供选择的药品:铁粉、浓硫酸、氧化铜粉末、0.2mol/L的H2C2O4标准溶液、0.1mol/L的酸性KMnO4标准溶液、酸碱指示剂.
b.实验装置设计及组装(加热及夹持装置均已略去)

【实验过程及数据处理】
(2)B中发生反应的离子方程式为:
(3)实验前先通入一段时间的N2,其目的是
(4)B、C、D中所盛试剂均足量,则证实生成的气体中同时存在SO2和H2的现象是
(5)A中反应结束后,继续通N2使A中生成的气体全部赶出,待B、D中反应完全后,先后三次取用B中反应后的溶液于锥形瓶中,每次取用25mL,用H2C2O4标准溶液进行滴定.
①H2C2O4标准溶液与酸性KMnO4溶液反应的离子方程式如下,请将该方程式完成并配平.
②滴定达到终点时的现象是
③重复滴定两次,平均每次耗用H2C2O4标准溶液15.63mL,则铁与浓硫酸反应产生的SO2气体
的物质的量为
某研究性学习小组为研究氯气是否具有漂白性,设计如下实验装置.试根据实验装置回答下列问题:

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液
(1)在常温下,KMnO4固体可以与浓盐酸反应生成氯气,其反应方程式为:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的 .
(2)B中的液体为 ,其作用为 .
(3)A、C中有色布条的颜色变化分别为 ,A、C的实 验现象说明氯气是否具有漂白性? (填“是”或“否”).
(4)D中NaOH溶液的作用 (用离子方程式说明).
(5)将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去.组内有甲、乙两种 意见:
甲:氯气溶于水溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色.
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则 的意见正确.(填“甲”或“乙”)
查看习题详情和答案>>

A、C中为干燥的有色布条,B为无色液体,D中为NaOH溶液
(1)在常温下,KMnO4固体可以与浓盐酸反应生成氯气,其反应方程式为:
2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则其反应装置应选用甲、乙、丙中的
(2)B中的液体为
(3)A、C中有色布条的颜色变化分别为
(4)D中NaOH溶液的作用
(5)将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去.组内有甲、乙两种 意见:
甲:氯气溶于水溶液显酸性,中和了NaOH,使溶液褪为无色;
乙:氯气溶于水生成漂白性物质,使溶液褪为无色.
丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则
化学试剂的生产和电镀工业排放的废水中常含有20~100mg.L-1Cr(Ⅵ),饮用含Cr(Ⅵ)的水会损害人的肠胃等,已知Cr(Ⅲ)的毒性是Cr(Ⅵ)的0.5%,国家规定工业废水含Cr(Ⅵ)的量排放标准为0.1mg.L-1.工业上常用化学法和电解法处理含Cr(Ⅵ)废水,再将Cr(Ⅲ)转化成沉淀除去,某研究性学习小组为研究废水的净化,设计了如下实验1流程: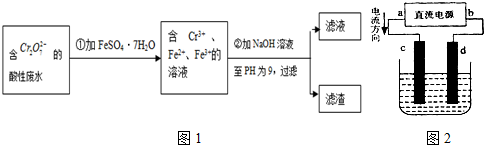
(1)配平第①步反应的离子方程式:
(2)设计一个电解装置也可以实现上述目的,装置如图2(用铁棒和石墨作电极):
电极材料c为:
d极电极反应为:
(3)已知:25℃时Ag2Cr2O7的Ksp=2×10-7.则25℃时,将4×10-2mol?L-1的AgNO3溶液与4×10-4mol?L-1的K2Cr2O7溶液等体积混合
查看习题详情和答案>>

(1)配平第①步反应的离子方程式:
1
1
Cr2O72-+6
6
Fe2++14
14
H+═2
2
Cr3++6
6
Fe3++7
7
H2O
H2O
(2)设计一个电解装置也可以实现上述目的,装置如图2(用铁棒和石墨作电极):
电极材料c为:
铁棒
铁棒
d极电极反应为:
2H2O+2e-=H2↑+2OH-
2H2O+2e-=H2↑+2OH-
(3)已知:25℃时Ag2Cr2O7的Ksp=2×10-7.则25℃时,将4×10-2mol?L-1的AgNO3溶液与4×10-4mol?L-1的K2Cr2O7溶液等体积混合
不能
不能
(填“能”或“不能”) 析出沉淀.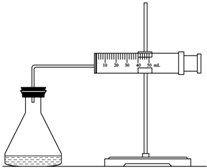 实验室用H2O2分解反应制取氧气时,常加入催化剂以加快反应速率,某研究性学习小组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应.
实验室用H2O2分解反应制取氧气时,常加入催化剂以加快反应速率,某研究性学习小组为研究催化剂FeCl3的量对O2生成速率的影响,设计了如下三组实验方案(见下表),将表中所给的试剂按一定体积混合后进行反应.| 实验编号 试剂 |
A | B | C |
| 10% H2O2/mL | 20.0 | V1 | V2 |
| 2mol/L FeCl3/mL | 0 | 5.0 | 10.0 |
| H2O/mL | V3 | V4 | 0 |
(1)欲用如图装置来比较该反应的反应速率快慢,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测
(2)为实现实验目的,则V1=
(3)根据你所掌握的知识判断,在上述实验中反应速率最快的可能是
(4)已知Fe3+催化H2O2分解的机理可分两步反应进行,其中第一步反应为:2Fe3++H2O2═2Fe2++O2↑+2H+,则第二步反应的离子方程式为:
某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出)
实验选用细铜丝、98.3%H2SO4、品红溶液、澄清石灰水、CC14、NaOH溶液等药品,铜丝被卷成螺旋状,一端没入浓H2SO4中,另一端露置在液面上方.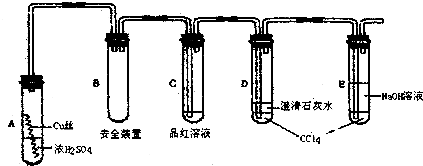
以下是该学习小组部分交流记录及后续探究实验的记录

根据上述材料回答下列问题:
(1)A试管上方的长导管的作用是 ;D、E两支试管中CC14的作用是 .
(2)加热过程中,观察到A试管中出现大量白色烟雾,起初部分烟雾在试管上部内壁析出淡黄色固体物质,在持续加热浓硫酸(沸腾)时,淡黄色固体物质又慢慢地消失.写出淡黄色固体消失的化学反应方程式: .
(3)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,但始终未见D试管中澄清石灰水出现浑浊或沉淀.学生1猜想是由于SO2溶解度较大,生成了Ca(HSO4)2的缘故.请你设计实验验证学生1的猜想 .
(4)根据上述研究,结合所学知识,你认为液面下方铜丝表面的黑色物质成分是 .(写化学式)
(5)学生2将反应后的反应液稀释后进行检验,发现溶液呈酸性,对此,学生2提出的猜想的:铜与浓硫酸反应生成的硫酸铜水解溶液呈酸性.
你的猜想是: .
请你设计一个简单的实验以验证你的猜想: .
查看习题详情和答案>>
实验选用细铜丝、98.3%H2SO4、品红溶液、澄清石灰水、CC14、NaOH溶液等药品,铜丝被卷成螺旋状,一端没入浓H2SO4中,另一端露置在液面上方.

以下是该学习小组部分交流记录及后续探究实验的记录

根据上述材料回答下列问题:
(1)A试管上方的长导管的作用是
(2)加热过程中,观察到A试管中出现大量白色烟雾,起初部分烟雾在试管上部内壁析出淡黄色固体物质,在持续加热浓硫酸(沸腾)时,淡黄色固体物质又慢慢地消失.写出淡黄色固体消失的化学反应方程式:
(3)对A试管中的浓H2SO4和铜丝进行加热,很快发现C试管中品红溶液褪色,但始终未见D试管中澄清石灰水出现浑浊或沉淀.学生1猜想是由于SO2溶解度较大,生成了Ca(HSO4)2的缘故.请你设计实验验证学生1的猜想
(4)根据上述研究,结合所学知识,你认为液面下方铜丝表面的黑色物质成分是
(5)学生2将反应后的反应液稀释后进行检验,发现溶液呈酸性,对此,学生2提出的猜想的:铜与浓硫酸反应生成的硫酸铜水解溶液呈酸性.
你的猜想是:
请你设计一个简单的实验以验证你的猜想: