摘要:15.A.B.C.D.E.F是原子序数依次增大的六种常见元素.其性质如下: 元素 性质 A 单质在C2中燃烧可生成AC和AC2两种气体 D 原子的最外层电子与其最内层电子数相同 E 单质在C2中燃烧的产物可使品红溶液褪色 F 与C元素形成的化合物F3C4具有磁性 请回答下列问题: (1)F元素在周期表中的位置是 ,AC2的电子式为 . (2)D单质在空气中燃烧的化学方程式为 . (3)元素C与元素E相比.非金属性较强的是 .能证明这一结论的事实是 . (4)A.B.C形成的10电子氢化物中.热稳定性最好的是 ,B.C的氢化物分子结合H+能力较强的是 .用离子方程式加以说明 . [答案] (1)第4周期Ⅷ族 ···· ····C········ (2)2Mg+O22MgO,3Mg+N2Mg3N2,2Mg+CO22MgO+C (3)O 氧的氢化物比硫的氢化物稳定(或S+O2SO2) (4)H2O NH3 NH3+H3O+===NH+H2O
网址:http://m.1010jiajiao.com/timu3_id_77544[举报]
A、B、C、D、E、F是原子序数依次增大的同周期元素,已知A、C、F的原子最外层电子数之和为11,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应,均生成盐和水;D元素原子的次外层电子数比最外层电子数多4,E元素原子的最外层与最内层电子数的差是3.试回答下列问题:
(1)写出下列元素符号:A
(2)用电子式表示B和F形成化合物的过程:
 .
.
(3)写出A、C、F三种元素最高价氧化物对应的水化物相互反应的化学方程式:
查看习题详情和答案>>
(1)写出下列元素符号:A
Na
Na
,CAl
Al
,DSi
Si
,EP
P
.(2)用电子式表示B和F形成化合物的过程:


(3)写出A、C、F三种元素最高价氧化物对应的水化物相互反应的化学方程式:
NaOH+Al(OH)3═NaAlO2+2H2O
NaOH+Al(OH)3═NaAlO2+2H2O
、NaOH+HClO4═NaClO4+H2O
NaOH+HClO4═NaClO4+H2O
、Al(OH)3+3HClO4═Al(ClO4)3+3H2O
Al(OH)3+3HClO4═Al(ClO4)3+3H2O
.A、B、C、D、E、F是原子序数依次增大的6种短周期元素.A、E同主族,B、C是同周期相邻的两种元素.A、C的质子数之和等于D的质子数,D2-与E+具有相同的电子层结构,D和F最外层电子数相同,F的最高正价与D的最低负价代数和等于4.试回答下列问题:
(1)常见化合物W由A、D、E三种元素组成,则W中含有的化学键类型有
(2)X、Y、Z三种常见化合物均有A、C、D三种元素组成,X和Z的水溶液呈酸性,Y的水溶液呈碱性,在溶液中,X促进水的电离,Y和Z抑制水的电离,则它们的化学式分别是:X
(3)用A2D2在酸性条件下处理含BC-的工业废水,将得到C2及BD2等无污染的物质,请写出该反应的离子方程式
查看习题详情和答案>>
(1)常见化合物W由A、D、E三种元素组成,则W中含有的化学键类型有
离子键、共价键
离子键、共价键
;(2)X、Y、Z三种常见化合物均有A、C、D三种元素组成,X和Z的水溶液呈酸性,Y的水溶液呈碱性,在溶液中,X促进水的电离,Y和Z抑制水的电离,则它们的化学式分别是:X
NH4NO3
NH4NO3
、YNH3?H2O
NH3?H2O
、ZHNO3
HNO3
;(3)用A2D2在酸性条件下处理含BC-的工业废水,将得到C2及BD2等无污染的物质,请写出该反应的离子方程式
5H2O2+2CN-+2H+═N2+2CO2+6H2O
5H2O2+2CN-+2H+═N2+2CO2+6H2O
.A、B、C、D、E、F是原子序数依次增大短周期元素.A、D同族,B、C同周期;B原子最外层电子数是次外层的两倍;在周期表中A的原子半径最小;C是地壳中含量最多的元素,C是F不同周期的邻族元素;E和F的原子序数之和为30.由于上述六种元素中的两种或三种组成的甲、乙、丙、丁、戊、己六种化合物如下表所示:
请完成下列问题:
(1)乙的电子式: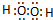
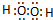 ;向含有1mol 乙的水溶液中加入MnO2,该反应中电子转移的物质的量为
;向含有1mol 乙的水溶液中加入MnO2,该反应中电子转移的物质的量为
(2)D的离子结构示意图
 ,己的空间构型
,己的空间构型
(3)8g 丙完全燃烧,生成液态水和CO2,放出445kJ的热量,则丙燃烧的热化学方程式为
(4)F的单质与甲反应的离子方程式为
(5)将丁与戊两种水溶液混合,发生反应的离子方程式为
查看习题详情和答案>>
| 化合物 | 甲 | 乙 | 丙 |
| 各元素原子个数比 | n(A):n(C)=2:1 | n(A):n(C)=1:1 | n(B):n(A)=1:4 |
| 化合物 | 丁 | 戊 | 己 |
| 各元素原子个数比 | n(D):n(B):n(C)=2:1:3 | n(E):n(F)=1:3 | n(B):n(F)=1:4 |
(1)乙的电子式:
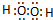
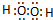
1
1
mol.(2)D的离子结构示意图


正四面体
正四面体
.(3)8g 丙完全燃烧,生成液态水和CO2,放出445kJ的热量,则丙燃烧的热化学方程式为
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ/mol
.(4)F的单质与甲反应的离子方程式为
Cl2+H2O=H++Cl-+HClO
Cl2+H2O=H++Cl-+HClO
.(5)将丁与戊两种水溶液混合,发生反应的离子方程式为
2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
.A、B、C、D、E、F是原子序数依次增大的六种常见元素.E的单质在C2中燃烧的产物可使品红溶液褪色.F和C元素形成的化合物F3C4具有磁性.A的单质在C2中燃烧可生成AC和AC2两种气体.D的单质是一种金属,该金属在AC2中剧烈燃烧生成黑、白两种固体.请回答下列问题:
(1)B的单质分子的结构式为
(2)A元素形成的同素异形体的晶体类型可能是(填序号)
①离子晶体 ②原子晶体 ③金属晶体 ④分子晶体
(3)A、B、C形成的10电子氢化物中,A、B、C的氢化物沸点最高的是(写化学式)
查看习题详情和答案>>
(1)B的单质分子的结构式为
N≡N
N≡N
;DC的化学式为MgO
MgO
;A元素在周期表中的位置是第二周期、IVA族
第二周期、IVA族
.(2)A元素形成的同素异形体的晶体类型可能是(填序号)
②④
②④
.①离子晶体 ②原子晶体 ③金属晶体 ④分子晶体
(3)A、B、C形成的10电子氢化物中,A、B、C的氢化物沸点最高的是(写化学式)
H2O
H2O
;B、C的氢化物分子结合H+能力较强的是(写化学式)NH3
NH3
,用一个离子方程式加以证明NH3+H3O+═NH4++H2O
NH3+H3O+═NH4++H2O
.A、B、C、D、E、F是原子序数依次增大的前四周期元素.A、B、C三种元素的基态原子具有相同的能级和能层,且第一电离能的顺序为A<C<B,其中C原子基态时2p轨道有两个未成对电子;D与A同族,其单质为常用的半导体材料;E为前四周期电负性最小的元素;F原子内层无空轨道,最外层电子数与E相同.请回答:
(1)F+的价层电子排布为 ;写出化合物F2C与稀硫酸反应的产物之一为红色固体且反应中只有F元素化合价发生了变化,该反应的离子方程式 .
(2)B、D形成一种超硬、耐磨、耐高温的新型化合物,该化合物化学式为 ,属于 晶体.
由氢气与C2反应生成1mol气态H2C产物,放热241.8KJ,若1g 气态H2C转化成液态H2C放热2.444KJ,则反应:2H2(g)+C2(g)=2H2C(L)的△H= KJ/mol.
(3)C与氢元素形成的正一价离子含有10电子,该离子中C原子的杂化方式为 ; C与氢元素形成的一种18电子分子M的水溶液具有弱酸性,则M与Ba(OH)2溶液反应生成酸式盐的化学方程式为 .
(4)1molAC2分子中σ键与π键的数目之比为 ;B、C形成的正一价离子N与AC2互为等电子体,N的电子式为 ;常温下,若1molAC2与等物质的量的NaOH反应后的溶液pH等于9,则c( H2CO3)-c( CO32-)= .
查看习题详情和答案>>
(1)F+的价层电子排布为
(2)B、D形成一种超硬、耐磨、耐高温的新型化合物,该化合物化学式为
由氢气与C2反应生成1mol气态H2C产物,放热241.8KJ,若1g 气态H2C转化成液态H2C放热2.444KJ,则反应:2H2(g)+C2(g)=2H2C(L)的△H=
(3)C与氢元素形成的正一价离子含有10电子,该离子中C原子的杂化方式为
(4)1molAC2分子中σ键与π键的数目之比为