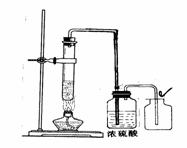
摘要:某学校化学兴趣小组同学在学习了制取氧气这一节内容后.发现在实验室里用5%H2O2溶液加热制O2.用带火星的木条检验.木条很难复燃.同学们经过认真观察.猜想其可能原因是 或 . 为了验证此猜想是否正确.兴趣小组的同学经过热烈讨论.制定了实验方案并进行了实验. (1)第一组同学采取增大H2O2溶液浓度的方法.用l0%的H2O2溶液加热.结果一段时间后.用带火星的木条检验.木条复燃, (2)第二组同学从实验装置上进行了改进.效果很好. 在实验基础上.同学们经过交流讨论.得出了一些结论: ①由第一组同学的实验可得出:影响H202分解产生02的量的多少及分解快慢的因素之一是 . ②第二组同学的实验验证了实验前同学们猜想的正确性.其中.浓硫酸的作用是 , (3)另有同学在5%的H202溶液中加入少量二氧化锰固体粉末.常温下.用带火星木条检验.木条复燃,此实验中二氧化锰所起的作用可能是 ,有关化学方程式为: .
网址:http://m.1010jiajiao.com/timu3_id_7508[举报]
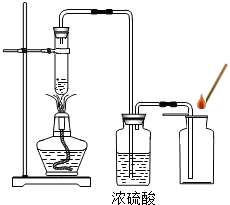 某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是
某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是H2O2溶液的浓度太低,以致于产生的氧气太少
H2O2溶液的浓度太低,以致于产生的氧气太少
或加热时伴随的水蒸气太多
加热时伴随的水蒸气太多
.为了验证此猜想是否正确,兴趣小组的同学经过热烈讨论,制定了实验方案并进行了实验.(1)第一组同学采取增大H2O2溶液浓度的方法,用l0%的H2O2溶液加热,结果一段时间后,用带火星的木条检验,木条复燃;
(2)第二组同学从实验装置上进行了改进,效果很好(见图).
在实验基础上,同学们经过交流讨论,得出了一些结论:
①由第一组同学的实验可得出:影响H2O2分解产生O2的量的多少及分解快慢的因素之一是
H2O2溶液的浓度大小
H2O2溶液的浓度大小
②第二组同学的实验验证了实验前同学们猜想的正确性,其中,浓硫酸的作用是
干燥(吸水)
干燥(吸水)
;(3)另有同学在5%的H2O2溶液中加入少量二氧化锰固体粉末,常温下,用带火星木条检验,木条复燃;此实验中二氧化锰所起的作用可能是
催化作用
催化作用
;有关化学方程式为:2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
【继续回答下列问题,你可以获得奖励分数,最多奖励4分,但化学总分不得超过60分】
某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%过氧化氢(H2O2)溶液加热制氧气,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是
第一组:同学们采取增大H2O2溶液浓度的方法,用10%的H2O2溶液加热,结果一段时间后,用带火星的木条检验,木条复燃;
第二组:同学们在5%的H2O2溶液中加入2滴新制氢氧化钠溶液,加热一段时间后,用带火星木条检验,木条复燃;
第三组:同学们从实验装置上进行了改进(见右图),效果很好.在实验基础上,同学们经过交流讨论,得出了一些结论:
(1)由第一组同学的实验可得出:影响H2O2分解产生氧气的量的多少及分解快慢的因素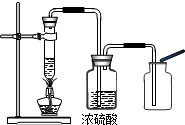 之一是
之一是
(2)由第二组同学的实验可分析得出,氢氧化钠所起的作用可能是
(3)第三组同学的实验验证了实验前同学们猜想的正确性,查阅资料知,浓硫酸在实验中常用作干燥剂,你分析第三组的同学对实验装置进行改进后,效果较好的原因可能是
(4)小明同学认真观察了第三组同学的实验装置,结合化学实验基本操作知识和氧气的物理性质,提出了一种更简单的改进装置,经现场实验,效果很好,请你写出他的改进方法(或画出他的实验装置改进简图)
查看习题详情和答案>>
某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%过氧化氢(H2O2)溶液加热制氧气,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是
大量水蒸气对实验造成了干扰
大量水蒸气对实验造成了干扰
.为了验证此猜想是否正确,兴趣小组的同学经过热烈讨论,制定了实验方案并进行了实验.第一组:同学们采取增大H2O2溶液浓度的方法,用10%的H2O2溶液加热,结果一段时间后,用带火星的木条检验,木条复燃;
第二组:同学们在5%的H2O2溶液中加入2滴新制氢氧化钠溶液,加热一段时间后,用带火星木条检验,木条复燃;
第三组:同学们从实验装置上进行了改进(见右图),效果很好.在实验基础上,同学们经过交流讨论,得出了一些结论:
(1)由第一组同学的实验可得出:影响H2O2分解产生氧气的量的多少及分解快慢的因素
 之一是
之一是H2O2溶液浓度的大小
H2O2溶液浓度的大小
;(2)由第二组同学的实验可分析得出,氢氧化钠所起的作用可能是
促进H2O2分解,减少水分蒸发
促进H2O2分解,减少水分蒸发
;(3)第三组同学的实验验证了实验前同学们猜想的正确性,查阅资料知,浓硫酸在实验中常用作干燥剂,你分析第三组的同学对实验装置进行改进后,效果较好的原因可能是
浓硫酸吸收了气体中的水蒸气,使氧气的浓度增大
浓硫酸吸收了气体中的水蒸气,使氧气的浓度增大
.(4)小明同学认真观察了第三组同学的实验装置,结合化学实验基本操作知识和氧气的物理性质,提出了一种更简单的改进装置,经现场实验,效果很好,请你写出他的改进方法(或画出他的实验装置改进简图)
加热时试管倾斜于桌面大约成45°角
加热时试管倾斜于桌面大约成45°角
.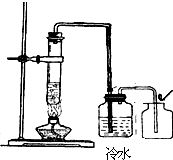 某学校化学兴趣小组同学在学习了制取氧气这~节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是
某学校化学兴趣小组同学在学习了制取氧气这~节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是H202分解产生02的量的多少及分解快慢与浓度有关
H202分解产生02的量的多少及分解快慢与浓度有关
或加热的过程中产生的水蒸气影响
加热的过程中产生的水蒸气影响
.为了验证此猜想是否正确,兴趣小组的同学经过热烈讨论,制定了实验方案并进行了实验.(1)第一组同学采取增大H2O2溶液浓度的方法,用l0%的H2O2溶液加热,结果一段时间后,用带火星的木条检验,木条复燃;
(2)第二组同学从实验装置上进行了改进,效果很好(如图图).
在实验基础上,同学们经过交流讨论,得出了一些结论:
①由第一组同学的实验可得出:影响H202分解产生02的量的多少及分解快慢的因素之一是
H2O2溶液浓度的大小
H2O2溶液浓度的大小
②第二组同学的实验验证了实验前同学们猜想的正确性,其中,冷水的作用是
冷却水蒸气,减少它对实验的影响
冷却水蒸气,减少它对实验的影响
. 某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是
某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃.同学们经过认真观察,猜想其可能原因是生成的大量水蒸气对实验造成的了干扰
生成的大量水蒸气对实验造成的了干扰
.为了验证此猜想是否正确,兴趣小组的同学经过热烈讨论,制定了实验方案并进行了实验.第一组同学采取增大H2O2溶液浓度的方法,用10%的H2O2溶液加热,结果一段时间后,用带火星的木条检验,木条复燃;
第二组的同学在5%的H2O2溶液中加入2滴新制氢氧化钠溶液,加热一段时间后,用带火星木条检验,木条复燃;
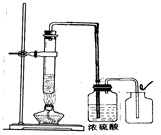
第三组同学从实验装置上进行了改进,效果很好(见图):
在实验基础上,同学们经过交流讨论,得出了一些结论
①由第一组同学的实验可得出:影响H2O2分解产生O2的量的多少及分解快慢的因素之一是
H2O2溶液浓度的大小
H2O2溶液浓度的大小
;②由第二组同学的实验可分析得出氢氧化钠所起的作用可能是
促进H2O2分解,减少水分蒸发
促进H2O2分解,减少水分蒸发
;③第三组同学的实验验证了实验前同学们猜想的正确性,其中浓硫酸的作用是
浓硫酸吸收了气体中的水蒸气,使氧气的浓度增大
浓硫酸吸收了气体中的水蒸气,使氧气的浓度增大
.某学校化学兴趣小组同学在学习了制取氧气这一节内容后,发现在实验室里用5%H2O2溶液加热制O2,用带火星的木条检验,木条很难复燃。同学们经过认真观察,猜想其可能原因是 。为了验证此猜想是否正确,兴趣小组的同学经过热烈讨论,制定了实验方案并进行了实验。
第一组同学采取增大H2O2溶液浓度的方法,用10%的H2O2溶液加热,结果一段时间后,用带火星的木条检验,木条复燃;
第二组的同学在5%的H2O2溶液中加入2滴新制氢氧化钠溶液,加热一段时间后,用带火星木条检验,木条复燃;第三组同学从实验装置上进行了改进,效果很好(见图):
在实验基础上,同学们经过交流讨论,得出了一些结论
①由第一组同学的实验可得出:影响H2O2分解产生O2的量的多少及分解快慢的因素之一是 ;
②由第二组同学的实验可分析得出氢氧化钠所起的作用可能是 ;
③第三组同学的实验验证了实验前同学们猜想的正确 性,其中,浓硫酸的作用是 ;
④小三同学认真观察了第三组同学的实验装置,结合O2的物理性质,提出了一种更简单的改进装置,经现场实验,效果很好,请你画出他的实验装置简图。