网址:http://m.1010jiajiao.com/timu3_id_72864[举报]
Ⅰ.从铝土矿中提取氧化铝的流程如图所示:

(1)试剂A是
(2)向溶液a中通入过量的CO2,将得到的不溶物煅烧后也可得到Al2O3,该方案的缺点是
Ⅱ.电解熔融的氧化铝可制备金属铝
(3)电解时,阳极的电极反应方程式为
Ⅲ.新型陶瓷氮化铝可用以下两种方法制备
(4)①氧化铝高温还原法:
| ||
②氯化铝与氨气高温合成法:AlCl3+NH3
| ||
(5)方法②比方法①在生产上更具优势.下列说法中,正确的是
A.方法①中的 Al2O3、C、N2结构稳定,反应时破坏化学键需要消耗更多的能量
B.方法①中的Al2O3和C容易残留在氮化铝中
C.两种方法中氮化铝均为还原产物.
(18分)铝土矿的主要成分是Al2O3,还含有Fe2O3、SiO2等杂质。
Ⅰ.从铝土矿中提取氧化铝的流程如下图所示:
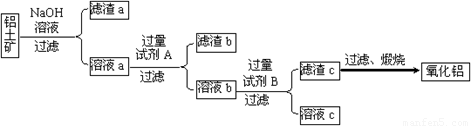
(1)试剂A是 ;溶液b与试剂B反应的离子方程式为 。
(2)加入NaOH溶液进行的反应的离子方程式为 ___、
,向溶液a中通入过量的CO2,将得到的不溶物煅烧后也可得到Al2O3,该方案的缺点是 。
Ⅱ.电解熔融的氧化铝可制备金属铝
(3)写出电解的化学方程式 。每生产0.27吨铝,理论上转移电子的物质的量为 mol。
Ⅲ.新型陶瓷氮化铝可用以下两种方法制备
(4)①氧化铝高温还原法: Al2O3 + C + N2  AlN + CO(配平)
AlN + CO(配平)
②氯化铝与氨气高温合成法:AlCl3+NH3  AlN+3HCl
AlN+3HCl
(5)方法②比方法①在生产上更具优势。下列说法中,正确的是 。
A.方法①中的 Al2O3、C、N2结构稳定,反应时破坏化学键需要消耗更多的能量
B.方法①中的Al2O3和C容易残留在氮化铝中
C.两种方法中氮化铝均为还原产物
查看习题详情和答案>>
(18分)铝土矿的主要成分是Al2O3,还含有Fe2O3、SiO2等杂质。
Ⅰ.从铝土矿中提取氧化铝的流程如下图所示: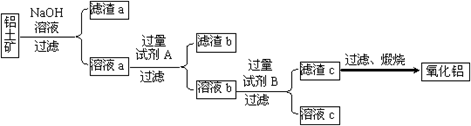
(1)试剂A是 ;溶液b与试剂B反应的离子方程式为 。
(2)加入NaOH溶液进行的反应的离子方程式为 ___、
,向溶液a中通入过量的CO2,将得到的不溶物煅烧后也可得到Al2O3,该方案的缺点是 。
Ⅱ.电解熔融的氧化铝可制备金属铝
(3)写出电解的化学方程式 。每生产0.27吨铝,理论上转移电子的物质的量为 mol。
Ⅲ.新型陶瓷氮化铝可用以下两种方法制备
(4)①氧化铝高温还原法: Al2O3 + C + N2 AlN + CO(配平)
AlN + CO(配平)
②氯化铝与氨气高温合成法:AlCl3+NH3 AlN+3HCl
AlN+3HCl
(5)方法②比方法①在生产上更具优势。下列说法中,正确的是 。
A.方法①中的 Al2O3、C、N2结构稳定,反应时破坏化学键需要消耗更多的能量
B.方法①中的Al2O3和C容易残留在氮化铝中
C.两种方法中氮化铝均为还原产物
铝土矿的主要成分是![]() ,还含有
,还含有![]() 、
、![]() 等杂质。
等杂质。
Ⅰ.从铝土矿中提取氧化铝的流程如下图所示:

(1)试剂A是 ;溶液b与试剂B反应的离子方程式为 。
(2)向溶液a中通入过量的CO2,将得到的不溶物煅烧后也可得到Al2O3,该方案的缺点是 。
Ⅱ.电解熔融的氧化铝可制备金属铝
(3)电解时,阳极的电极反应方程式为 ;每生产0.324吨铝,理论上转移电子的物质的量为 mol。
Ⅲ.新型陶瓷氮化铝可用以下两种方法制备
(4)①氧化铝高温还原法: ![]()
![]()
![]()
![]()
![]() CO(请配平)
CO(请配平)
②氯化铝与氨气高温合成法:![]()
![]()
![]()
(5)方法②比方法①在生产上更具优势。下列说法中,正确的是 。
A.方法①中的 Al2O3、C、N2结构稳定,反应时破坏化学键需要消耗更多的能量
B.方法①中的Al2O3和C容易残留在氮化铝中
C.两种方法中氮化铝均为还原产物
查看习题详情和答案>>
I.从铝土矿中提取氧化铝的流程如下图所示:
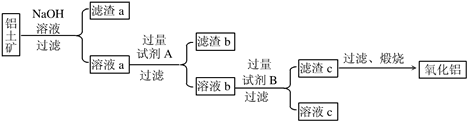
(2)向溶液a中通入过量的CO2,将得到的不溶物煅烧后也可得到Al2O3,该方案的缺点是____。
Ⅱ,电解熔融的氧化铝可制备金属铝
(3)电解时,阳极的电极反应方程式为____;每生产0. 324吨铝,理论上转移电子的物质的量为___mol。 ⅡI.新型陶瓷氮化铝可用以下两种方法制备:
(4)①氧化铝高温还原法:___Al2O3+___C+___N2
 ___AlN+___CO(请配平);
___AlN+___CO(请配平);②氯化铝与氨气高温合成法:AlCl3+NH3
 AlN+3HCl。
AlN+3HCl。 (5)方法②比方法①在生产上更具优势。下列说法中,正确的是______。
A.方法①中的Al2O3、C、N2结构稳定,反应时破坏化学键需要消耗更多的能量
B.方法①中的Al2O3和C容易残留在氮化铝中
C.两种方法中氮化铝均为还原产物