题目内容
(18分)铝土矿的主要成分是Al2O3,还含有Fe2O3、SiO2等杂质。
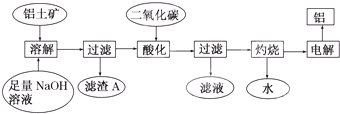
Ⅰ.从铝土矿中提取氧化铝的流程如下图所示: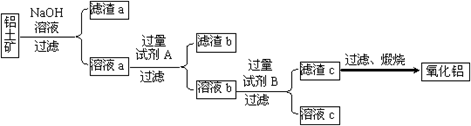
(1)试剂A是 ;溶液b与试剂B反应的离子方程式为 。
(2)加入NaOH溶液进行的反应的离子方程式为 ___、
,向溶液a中通入过量的CO2,将得到的不溶物煅烧后也可得到Al2O3,该方案的缺点是 。
Ⅱ.电解熔融的氧化铝可制备金属铝
(3)写出电解的化学方程式 。每生产0.27吨铝,理论上转移电子的物质的量为 mol。
Ⅲ.新型陶瓷氮化铝可用以下两种方法制备
(4)①氧化铝高温还原法: Al2O3 + C + N2 AlN + CO(配平)
AlN + CO(配平)
②氯化铝与氨气高温合成法:AlCl3+NH3 AlN+3HCl
AlN+3HCl
(5)方法②比方法①在生产上更具优势。下列说法中,正确的是 。
A.方法①中的 Al2O3、C、N2结构稳定,反应时破坏化学键需要消耗更多的能量
B.方法①中的Al2O3和C容易残留在氮化铝中
C.两种方法中氮化铝均为还原产物
(18分)
Ⅰ、(1)盐酸(硫酸或硝酸); Al3++3NH3·H2O =Al(OH)3↓+3NH4+
(2)Al2O3+2OH-=2AlO2-+H2O SiO2+2OH-=SiO32-+H2O
Al2O3中含有SiO2杂质
Ⅱ、(3)2Al2O3(熔融) 4Al + 3O2↑ 3×104
4Al + 3O2↑ 3×104
Ⅲ、(4) 1 Al2O3 + 3 C + 1 N2 === 2 AlN + 3 CO (5) AB
解析

练习册系列答案
相关题目
下列说法不正确的是( )
| A、赤铁矿的主要成分是Fe2O3 | B、铝土矿的主要成分是Al2O3 | C、工业制备氯气主要采用电解饱和食盐水的方法 | D、把铁矿石冶炼成铁的过程中,还原剂主要是焦炭 |


 铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程: