摘要:20.pC类似pH.是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3mol/L.则该溶液中该溶质的pC= -lg1×10-3=3.已知H2CO3溶液中存在的化学平衡为:CO2+H2OH2CO3H+ +HCO3-2H++CO32-.下图为H2CO3溶液的pC-pH图.请回答下列问题: (1)在pH=0-4时.H2CO3溶液中主要存在的离子为: ,在pH=12时.H2CO3溶液中主要存在的含碳阴离子为: , (2)pH<5时.溶液中H2CO3的pC值总是 小于3的原因是 , (3)一定浓度的NaHCO3和Na2CO3混合溶液是一种“缓冲溶液 .在这种溶液中加入少量的强酸或强碱.溶液的pH变化不大.其原因是
网址:http://m.1010jiajiao.com/timu3_id_63350[举报]
 pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为1×10-3mol/L,则溶液中该溶质的pC=-lg10-3=3.已知H2CO3溶液中存在下列平衡:CO2+H2O?H2CO3
H2CO3?H++HC
| O | - 3 |
HC
| O | - 3 |
| O | 2- 3 |
如图为H2CO3、HC
| O | - 3 |
| O | 2- 3 |
(1)在pH=9时,H2CO3溶液中浓度最大的含碳元素离子为
HCO3-
HCO3-
.(2)pH<4时,溶液中H2CO3的pC值总是约等于3的原因是
c(H+)增大后,平衡向左移动放出CO2,碳酸浓度保持不变
c(H+)增大后,平衡向左移动放出CO2,碳酸浓度保持不变
.(3)一定浓度的NaHCO3和NaCO3混合溶液是一种“缓冲溶液”,在这种溶液中加入少量的强酸或强碱,溶液的pH变化都不大,请用离子方程式表示加入少量强碱后其pH变化不大的原因
HCO3-+OH-=H2O+CO32-
HCO3-+OH-=H2O+CO32-
.(4)已知M2CO3为难溶物,则其KSP的表达式为
Ksp=c2(M+)?c(CO32-)
Ksp=c2(M+)?c(CO32-)
;现欲将某溶液中的M+以碳酸盐(KSP=1×10-12)的形式沉淀完全,则最后溶液中的C| O | 2- 3 |
2
2
(溶液中的离子浓度小于1×10-5mol/L时,沉定完全).(5)若某溶液中含3mol Na2CO3,滴入一定量的稀盐酸,恰好使溶液中Cl-和HC
| O | - 3 |
4
4
mol.
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值,如溶液中某溶质的浓度为:1×10-3mol?L-1,则pC=-lg(1×10-3)=3.H2CO3溶液的pC-pH关系如图.
请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为 .
(2)已知碳酸溶液中存在平衡:H2O+CO2?H2CO3?H++HCO3-.当溶液pH由5减小到0时,溶液中H2CO3的pC基本不变的原因是 .
(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?L-1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3-?H++CO32-移动,溶液中H+浓度变化不大.根据上述信息,下列不能形成缓冲溶液的是 .
A.碳酸钠和氢氧化钠的混和溶液 B.醋酸和醋酸钠的混和溶液
C.硫酸和硫酸钠的混合溶液 D.氨水和氯化铵的混和溶液. 查看习题详情和答案>>

请回答下列问题:
(1)pH=2~4时,H2CO3溶液中主要存在的离子为
(2)已知碳酸溶液中存在平衡:H2O+CO2?H2CO3?H++HCO3-.当溶液pH由5减小到0时,溶液中H2CO3的pC基本不变的原因是
(3)能够抵抗外来少量酸碱的影响、保持自身 pH变化不大的溶液,称之为缓冲溶液.如浓度均为0.1mol?L-1的NaHCO3和Na2CO3混合溶液就是一种缓冲溶液,加入少量酸或碱,由于平衡HCO3-?H++CO32-移动,溶液中H+浓度变化不大.根据上述信息,下列不能形成缓冲溶液的是
A.碳酸钠和氢氧化钠的混和溶液 B.醋酸和醋酸钠的混和溶液
C.硫酸和硫酸钠的混合溶液 D.氨水和氯化铵的混和溶液. 查看习题详情和答案>>
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3mol?L-1,则该溶液中溶质的pC=3.下列表达正确的是( )
| A、某温度下任何电解质的水溶液中,pC(H+)+pC(OH-)=14 | B、0.01mol/L的CaCl2溶液中逐渐滴加纯碱溶液,滴加过程中pC(Ca2+)逐渐减小 | C、用0.01mol/L的盐酸滴定某浓度的NaOH溶液,滴定过程中pC(H+)逐渐增大 | D、某温度下,AB难溶性离子化合物的Ksp=1.0×10-10,其饱和溶液中pC(A+)+pC(B-)=10 |
(11分)pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为:1×10-3mol/L,则该溶液中溶质的pC=-lg1×10-3=3。下图为,H2CO3在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC—pH图。请回答下列问题: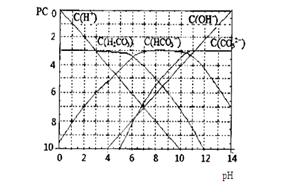
(1)在人体血液中,HCO3-能起到稳定人体PH的作用,请用电解质溶液中的平衡解释:
(用方程式表示)。
(2)H2CO3一级电离平衡常数的数值Ka1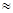
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的CO32-离子不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确 。
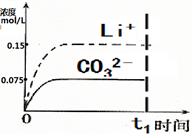
(4)已知某温度下Li2CO3的Ksp为1.68×10-3,将适量Li2CO3固体溶于100 mL水中至刚好饱和,饱和Li2CO3溶液中c(Li+)=0.15 mol·L-1。c(CO32-)=0.075 mol·L-1,若t1时刻在上述体系中加入100 mL0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
(5)请画出t1时刻后Li+和CO32-浓度随时间变化关系图(用虚线表示Li+ ,实线表示CO32-)。