网址:http://m.1010jiajiao.com/timu3_id_58271[举报]
A.在两个阴极上得到的银和汞的物质的量之比n(Ag)∶n(Hg)=2∶1
B.在两个阳极上得到的产物的物质的量不相等
C.硝酸亚汞的分子式为HgNO3
D.硝酸亚汞的分子式为Hg2(NO3)2 查看习题详情和答案>>
I、二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:
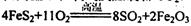 ,该反应中被氧化的元素是________(填元素符号)。
,该反应中被氧化的元素是________(填元素符号)。
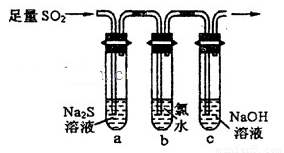
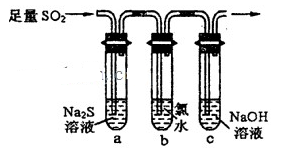
(2)一化学研究性学习小组设计用如下装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为________________________________。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaC!:溶液,产生白色沉淀上述方案合理的是方案______(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子反应方程式为____________________。
③当通入二氧化硫至试管c中溶液显中性时,溶液中c(Na+)=________________(用含硫元素微粒浓度的代数式表示)。
Ⅱ、另一化学研究性学习小组在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。
步骤一:电解精制:
电解时,粗铜应与电源的______极相连。阴极上的电极反应式为____________。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:
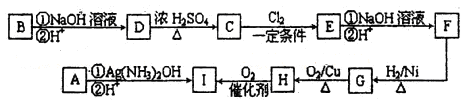
稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该反应的离子方程式:
____________________________________________________________。
查看习题详情和答案>>
I、二氧化硫是重要的工业原料,探究其制备方法和性质具有非常重要的意义。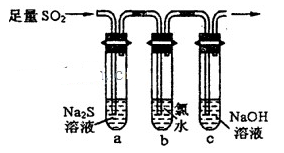
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2: ,该反应中被氧化的元素是________(填元素符号)。
,该反应中被氧化的元素是________(填元素符号)。
(2)一化学研究性学习小组设计用如下装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为________________________________。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaC!:溶液,产生白色沉淀上述方案合理的是方案______(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子反应方程式为____________________。
③当通入二氧化硫至试管c中溶液显中性时,溶液中c(Na+)=________________(用含硫元素微粒浓度的代数式表示)。
Ⅱ、另一化学研究性学习小组在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。
步骤一:电解精制:
电解时,粗铜应与电源的______极相连。阴极上的电极反应式为____________。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理: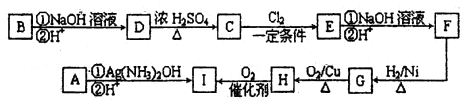
稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该反应的离子方程式:
____________________________________________________________。
(1)工业上用黄铁矿(FeS2,其中S元素为-l价)在高温下和氧气反应制备SO2:
 ,该反应中被氧化的元素是________(填元素符号)。
,该反应中被氧化的元素是________(填元素符号)。(2)一化学研究性学习小组设计用如下装置验证二氧化硫的化学性质.
①能说明二氧化硫具有氧化性的实验现象为________________________________。
②为验证二氧化硫的还原性,充分反应后,取试管b中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案Ⅱ:向第二份溶液加入品红溶液,红色褪去
方案Ⅲ:向第三份溶液加入BaC!:溶液,产生白色沉淀上述方案合理的是方案______(填“Ⅰ”、“Ⅱ”或“Ⅲ”);试管b中发生反应的离子反应方程式为____________________。
③当通入二氧化硫至试管c中溶液显中性时,溶液中c(Na+)=________________(用含硫元素微粒浓度的代数式表示)。
Ⅱ、另一化学研究性学习小组在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。
步骤一:电解精制:
电解时,粗铜应与电源的______极相连。阴极上的电极反应式为____________。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:
稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该反应的离子方程式:
____________________________________________________________。
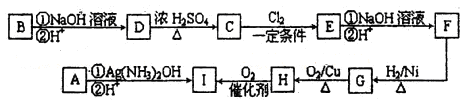
A、B、C、D、E均为钠盐,D、E具有相同的元素组成,都是由四种元素组成的化合物。向B溶液中滴加硝酸酸化的硝酸银溶液,立即产生白色沉淀,该沉淀见光变暗至灰至黑。A、B或B、C溶液混合均无明显现象,若将A、B、E和B、C、E分别按1:5:6和1:1:2的物质的量之比混合,溶液都能产生有刺激性气味黄绿色气体甲。D、E溶液混合能产生具有漂白性的刺激性气体乙。甲与乙混合气体通入水中会产生两种酸。B与E固体混合不反应,加热则能产生有刺激性气味的气体丙。若将气体丙通入A或C溶液中均能产生气体甲。甲气体通入D溶液,颜色会消失。若将A、D、E按2:1:1物质的量之比混合,能产生黄色气体丁。
请回答下列有关问题:
⑴.完成下列反应的离子方程式并配平之。
①.A + B + E → : ▲
②.D + E → : ▲
③.甲+乙+ H2O → : ▲
④.A + D + E → : ▲
⑵.丁气体消毒漂白性比甲强,是更理想的漂白试剂。相同条件下,相同体积的丁气体处理水的能力是甲的 ▲ 倍;相同质量的丁气体处理水的能力是甲的 ▲ 倍。
⑶.历史上曾把某元素的最高价的含氧酸称为某酸,如N、P、S等。A盐中对应的酸并不是该元素的最高价的含氧酸(当时误认为是最高价)。电解技术进入化学研究领域后,通过惰性材料电解A的水溶液,产生新的含氧酸盐(M=122.5 g·mol-1),我们可以把与其对应的酸称为高某酸。取出100 mL A盐溶液进行电解(惰性电极,通直流电),数小时后,收集到的阴、阳两极气体分别为6.72L和2.24L(已经折算成标准状况下的气体体积) 。
①.阴、阳两极所发生的电极反应离子方程式为 ▲ 、 ▲ 。
②.原A盐溶液的物质的量浓度为 ▲ 。(假设溶液体积变化忽略不计)
查看习题详情和答案>>