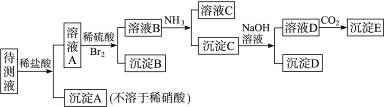
摘要:17.某待测溶液(阳离子为Na+)中可能会有SO.S2-.SO.Cl-.Br-.NO.CO.HCO中的一种或若干种.进行下列实验(每次实验所加试剂均过量): 回答以下问题: (1)待测液是否含有SO.SO?答: (2)沉淀B的化学式为 . (3)根据以上实验.待测液中肯定没有的离子是 .肯定存在的离子是 .
网址:http://m.1010jiajiao.com/timu3_id_57881[举报]
某待测溶液中可能含有SO
、SO
、CO
、HCO
、NO
、Cl-、Br-中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出).
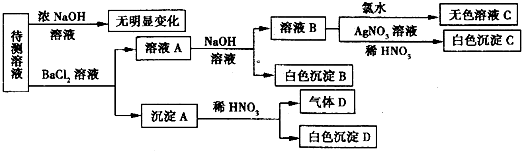
请回答下列问题:
(1)根据上述框图信息填写下表(不能确定的不填).
(2)待测溶液中是否有SO
、SO
:
(3)若Mn+为常见金属阳离子且原子序数不大于20,则要确定它具体是何种离子的方法是
查看习题详情和答案>>
2- 4 |
2- 3 |
2- 3 |
- 3 |
- 3 |

请回答下列问题:
(1)根据上述框图信息填写下表(不能确定的不填).
| 肯定存在的离子 | 肯定没有的离子 | 沉淀D | |
| 化学式或离子符号 | HCO3- HCO3- |
Br- Br- |
BaSO4 BaSO4 |
2- 3 |
2- 4 |
含有SO42-、SO32-中的一种或两种,因为待测液加入BaCl2溶液和稀HNO3生成了BaSO4沉淀,BaSO4的生成可能来自SO42-或SO32-中的一种或两种
含有SO42-、SO32-中的一种或两种,因为待测液加入BaCl2溶液和稀HNO3生成了BaSO4沉淀,BaSO4的生成可能来自SO42-或SO32-中的一种或两种
.若气体D遇空气变红色,则生成沉淀D时肯定发生的反应的离子方程式为3BaSO3+2H++2NO3-═2NO↑+3BaSO4↓+H2O
3BaSO3+2H++2NO3-═2NO↑+3BaSO4↓+H2O
,形成沉淀B时反应的离子方程式为HCO3-+Ba2++OH-═BaCO3↓+H2O
HCO3-+Ba2++OH-═BaCO3↓+H2O
.(3)若Mn+为常见金属阳离子且原子序数不大于20,则要确定它具体是何种离子的方法是
做焰色反应实验,若透过蓝色钴玻璃片观察到紫色火焰,说明是K+;若不透过蓝色钴玻璃片观察到黄色火焰,则说明是Na+
做焰色反应实验,若透过蓝色钴玻璃片观察到紫色火焰,说明是K+;若不透过蓝色钴玻璃片观察到黄色火焰,则说明是Na+
.某待测溶液中可能含有Na+、SO42-、SO32-、CO32-、Cl-、NO3-、HCO3-等离子,进行了下述实验.(所加BaCl2、H2SO4、HNO3、Ca(OH)2均过量)
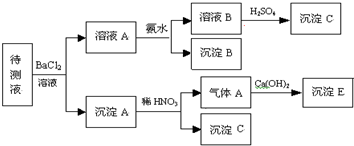
(1)判断待测液中有无SO42-、SO32-,并说明理由:
(2)写出沉淀B的化学式:
(3)沉淀C可能是什么物质:
(4)写出产生沉淀B的离子方程式:
查看习题详情和答案>>

(1)判断待测液中有无SO42-、SO32-,并说明理由:
含有SO42-、SO32-中的一种或两种,因为待测液加入BaCl2溶液和稀HNO3生成了BaSO4沉淀,BaSO4的生成可能来自SO42-或SO32-中的一种或两种
含有SO42-、SO32-中的一种或两种,因为待测液加入BaCl2溶液和稀HNO3生成了BaSO4沉淀,BaSO4的生成可能来自SO42-或SO32-中的一种或两种
;(2)写出沉淀B的化学式:
BaCO3
BaCO3
;(3)沉淀C可能是什么物质:
BaSO4
BaSO4
;(4)写出产生沉淀B的离子方程式:
HCO3-+NH3?H2O+Ba2+=BaCO3↓+NH4++H2O
HCO3-+NH3?H2O+Ba2+=BaCO3↓+NH4++H2O
.
某待测溶液中可能含有Fe2+、Fe3+、Ag+、Al3+、Ba2+、Ca2+、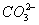 等离子。进行了下述实验(所加酸、碱、氨水、溴水都是过量的)。
等离子。进行了下述实验(所加酸、碱、氨水、溴水都是过量的)。
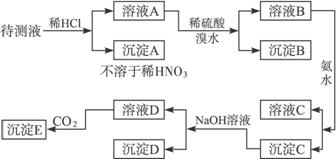
根据实验结果:
(1)判定待测液中有无Ba2+、Ca2+,并写出理由。
(2)写出沉淀D的分子式:___________________。
(3)写出从溶液D生成沉淀E的反应的离子方程式:______________________。
查看习题详情和答案>>