摘要: 没有理清元素“位构性 三者之间的关系.不能形成良好的思维习惯.定位讨论是这一部分题型的总体思路.无论是比较元素的性质.单质或化合物的性质以及原子半径等.均需由确定元素在周期表中的位置来分析讨论.
网址:http://m.1010jiajiao.com/timu3_id_56728[举报]
“位构性”展现出周期表,官能团决定了变化情。学习无机物,元素周期表是一个极强大的工具,学习有机物,官能团是我们关注的焦点。请你分析,在下列各化合物中,能发生酯化、还原、加成、消去四种反应的是
[ ]
A.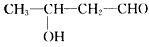
B.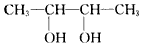
C.CH3-CH=CH-CHO
D.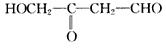
查看习题详情和答案>>
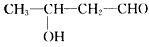
B.
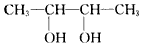
C.CH3-CH=CH-CHO
D.
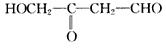
 《物质结构与性质》
《物质结构与性质》从原子、分子水平上帮助我们认识物质构成的规律;以微粒之间不同的作用力为线索,研究不同类型物质的有关性质;从物质结构决定性质的视角预测物质的有关性质.
(1)下列说法正确的是
A
A
(填字母).A.元素电负性由大到小的顺序为F>O>N
B.一个苯分子含3个π键和6个σ键
C.氯化钠和氯化铯晶体中氯离子的配位数相同
D.第一电离能的大小为Br>Se>As
(2)根据等电子体原理,羰基硫(OCS)分子的结构式为
O=C=S
O=C=S
.光气(COCl2)各原子最外层都满足8电子稳定结构,COCl2分子空间构型为平面三角形
平面三角形
(用文字描述).(3)Cu 2+基态的电子排布式为
1s22s22p63s23p63d9
1s22s22p63s23p63d9
.向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4晶体,该物质中配位原子的杂化方式为sp3
sp3
,不考虑空间构型,其内界结构可用示意图表示为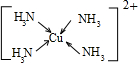

I.下列描述中正确的是
A.CS2为V形的极性分子 B.Cl0-3 的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对 D.SiF4和SO2-3 的中心原子均为sp3杂化
Ⅱ.下列说法中错误的是:
A.SO2、SO3都是极性分子
B.在NH4+ 和[Cu(NH3)4]2+中都存在配位键
C.元素电负性越大的原子,吸引电子的能力越强
D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
Ⅲ.雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得.
(1)元素第一电离能:Al Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为: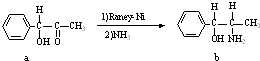
化合物b中进行sp3杂化的原子有: .
(3)一种铝镍合金的结构如图,与其结构相似的化合物是: (选填序号:a.氯化钠 b.氯化铯 c.石英 d.金刚石).
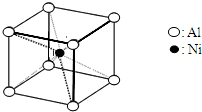
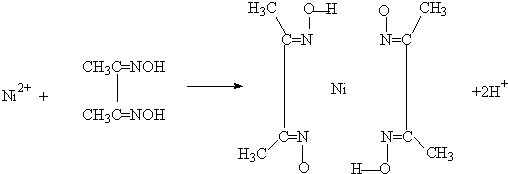
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀.
①Ni2+在基态时,核外电子排布式为: .
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4).
 查看习题详情和答案>>
查看习题详情和答案>>
A.CS2为V形的极性分子 B.Cl0-3 的空间构型为平面三角形
C.SF6中有6对完全相同的成键电子对 D.SiF4和SO2-3 的中心原子均为sp3杂化
Ⅱ.下列说法中错误的是:
A.SO2、SO3都是极性分子
B.在NH4+ 和[Cu(NH3)4]2+中都存在配位键
C.元素电负性越大的原子,吸引电子的能力越强
D.原子晶体中原子以共价键结合,具有键能大、熔点高、硬度大的特性
Ⅲ.雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得.
(1)元素第一电离能:Al
(2)雷尼镍催化的一实例为:

化合物b中进行sp3杂化的原子有:
(3)一种铝镍合金的结构如图,与其结构相似的化合物是:

(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀.
①Ni2+在基态时,核外电子排布式为:
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4).
 查看习题详情和答案>>
查看习题详情和答案>>
(2010?厦门一模)A、B、C、D、E、F、G七种前四周期元素,其原子序数依次增大.A的原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D及其同主族元素的氢化物沸点变化趋势如图;F是地壳中含量最高的金属元素;G与F同主族.请回答下列问题:
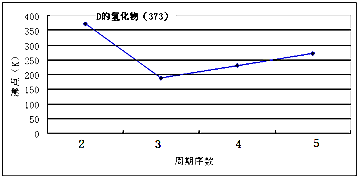
(1)写出F元素基态原子的核外电子排布式
(2)B、C、D三种元素电负性由大到小的顺序是
(3)下列有关上述元素的说法,正确的是
①CA3沸点高于BA4,主要是因为前者相对分子质量较大②Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于离子晶体③C的氢化物的中心原子采取sp2杂化④F单质的熔点高于E单质,是因为F单质的金属键较强⑤比G的原子序数少1的元素第一电离能高于G
(4)CA3分子的空间构型为
(5)ED是优良的耐高温材料,其晶体结构与NaCl晶体相似.ED的熔点比NaCl高,其原因是
查看习题详情和答案>>

(1)写出F元素基态原子的核外电子排布式
1s22s22p63S23P1
1s22s22p63S23P1
;(2)B、C、D三种元素电负性由大到小的顺序是
O>N>C
O>N>C
(用元素符号表示);(3)下列有关上述元素的说法,正确的是
④⑤
④⑤
(填序号);①CA3沸点高于BA4,主要是因为前者相对分子质量较大②Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于离子晶体③C的氢化物的中心原子采取sp2杂化④F单质的熔点高于E单质,是因为F单质的金属键较强⑤比G的原子序数少1的元素第一电离能高于G
(4)CA3分子的空间构型为
三角锥形
三角锥形
,1mol B2A4分子中含有5
5
molσ键;(5)ED是优良的耐高温材料,其晶体结构与NaCl晶体相似.ED的熔点比NaCl高,其原因是
MgO晶体中离子的电荷数大于NaCl,离子半径小,MgO离子键的键能更大,熔点更高
MgO晶体中离子的电荷数大于NaCl,离子半径小,MgO离子键的键能更大,熔点更高
.说明:O摄氏度=273K.某教师在上《元素周期表》复习课时,组织了一个“介绍自己”的活动: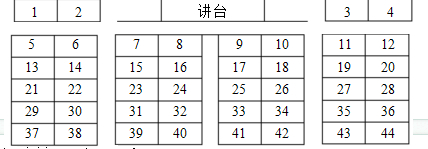
我们班级中共有44位同学,分为8个小组,按从左到右分别为IA、IIA…VIIA、0族,从上到下分别为第一、二…六周期.座位上的每一位同学对应一种元素,请在下列问题中符合要求的同学向大家介绍自己.
请你一起思考并回答下列问题:
(1)第三周期IVA族的元素对应座位号是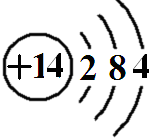
 .
.
(2)座位号为22的元素在元素周期表中的位置是
(3)比较座位号为18、19对应的元素的非金属性强弱,请用离子方程式表示
(4)课堂中有学生提出,这样的安排会导致他们没有对应的元素,则学生对应的座位号是
查看习题详情和答案>>

我们班级中共有44位同学,分为8个小组,按从左到右分别为IA、IIA…VIIA、0族,从上到下分别为第一、二…六周期.座位上的每一位同学对应一种元素,请在下列问题中符合要求的同学向大家介绍自己.
请你一起思考并回答下列问题:
(1)第三周期IVA族的元素对应座位号是
16
16
,原子结构示意图为

(2)座位号为22的元素在元素周期表中的位置是
第四周期第IIA族
第四周期第IIA族
.(3)比较座位号为18、19对应的元素的非金属性强弱,请用离子方程式表示
Cl2+S2-=S↓+2Cl-或Cl2+H2S=2H++S↓+2Cl-
Cl2+S2-=S↓+2Cl-或Cl2+H2S=2H++S↓+2Cl-
.(4)课堂中有学生提出,这样的安排会导致他们没有对应的元素,则学生对应的座位号是
2,3
2,3
.