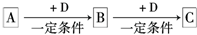摘要:16.已知A.B.c是中学化学的常见物质.它们在一定条件下有如下转化关系 (1)若A是一种淡黄色固体.B是造成酸雨的“罪魁祸首 .则X的化学式为 . (2)若A的体积分数为75%的溶液可用作医疗消毒剂,B与新制氢氧化铜共热.有砖红色沉淀生成,C能使湿润的蓝色石蕊试纸变红.则A与c在浓硫酸和加热条件下反应的化学方程式为 . (3)若A.B.c的焰色反应均为黄色.A是一种工业原料.B俗称小苏打.电解C的水溶液可以得到两种气态产物.这两种气态产物在工业上可以合成X.则电解C的水溶液的离子方程式为 . (4)若A.C为无色溶液.B为白色胶状沉淀.是治疗胃酸过多的一种药物的主要成分.X的焰色反应为黄色.则c溶液中除氢氧根外还存在的阴离子的化学式为 . (5)若A.B.C均为氧化物.X是一种黑色固态非金属单质.则B分子的结构式为 .
网址:http://m.1010jiajiao.com/timu3_id_55434[举报]
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系.A
B
C
(1)若A是一种金属固体,C是淡黄色固体,则C的化学式为
(2)若A、B、C的焰色反应均为黄色,A是一种工业原料,B俗称小苏打,电解C的水溶液可以得到两种气态产物,这两种气态产物在工业上可以合成X,则电解C的水溶液的离子方程式为
检验B中是否含有A的试剂可以是
①HCl ②BaCl2③Ca(OH)2 ④CaCl2
(3)若A为黑色非金属单质,C是造成地球温室效应的罪魁祸首,C可与金属镁发生反应,其化学方程式为
查看习题详情和答案>>
| X |
| X |
(1)若A是一种金属固体,C是淡黄色固体,则C的化学式为
Na2O2
Na2O2
.C与水反应的离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑
2Na2O2+2H2O=4Na++4OH-+O2↑
(2)若A、B、C的焰色反应均为黄色,A是一种工业原料,B俗称小苏打,电解C的水溶液可以得到两种气态产物,这两种气态产物在工业上可以合成X,则电解C的水溶液的离子方程式为
2Cl-+2H2O
2OH-+H2↑+Cl2↑
| ||
2Cl-+2H2O
2OH-+H2↑+Cl2↑
B溶液与X溶液反应的离子方程式为
| ||
HCO3-+H+=H2O+CO2↑
HCO3-+H+=H2O+CO2↑
检验B中是否含有A的试剂可以是
②④
②④
(填序号).①HCl ②BaCl2③Ca(OH)2 ④CaCl2
(3)若A为黑色非金属单质,C是造成地球温室效应的罪魁祸首,C可与金属镁发生反应,其化学方程式为
CO2+2Mg
C+2MgO
| ||
CO2+2Mg
C+2MgO
.
| ||
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系: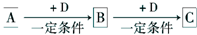
(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体.则A转化为B反应的化学方程式为
(2)若D是具有氧化性的单质,A元素为第三周期的金属元素,则C的电子式为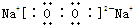
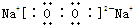 .
.
(3)若D是生活中常见的过渡金属,A是黄绿色气体,则B→C的离子方程式为
(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子.则B转化为C的离子方程式为
(5)若A为最简单的有机物,D是具有氧化性的单质.25℃、101kPa时,3.2g A完全燃烧生成稳定的氧化物时放出178kJ的热量.请写出表示物质A的燃烧热的热化学方程式
(6)若A的体积分数为75%的溶液可用作医疗消毒剂;B与新制氢氧化铜共热,有红色沉淀生成.则A生成B的化学方程为
查看习题详情和答案>>
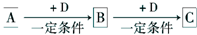
(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体.则A转化为B反应的化学方程式为
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(2)若D是具有氧化性的单质,A元素为第三周期的金属元素,则C的电子式为
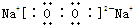
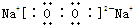
(3)若D是生活中常见的过渡金属,A是黄绿色气体,则B→C的离子方程式为
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子.则B转化为C的离子方程式为
CO32-+CO2+H2O=HCO3-
CO32-+CO2+H2O=HCO3-
.(5)若A为最简单的有机物,D是具有氧化性的单质.25℃、101kPa时,3.2g A完全燃烧生成稳定的氧化物时放出178kJ的热量.请写出表示物质A的燃烧热的热化学方程式
CH4(g)+2O2(g)=CO2(g)+2H2O(l )△H=-890kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l )△H=-890kJ/mol
.(6)若A的体积分数为75%的溶液可用作医疗消毒剂;B与新制氢氧化铜共热,有红色沉淀生成.则A生成B的化学方程为
2CH3CH2OH+O2
2CH3CHO+2H2O
| Cu |
| △ |
2CH3CH2OH+O2
2CH3CHO+2H2O
.| Cu |
| △ |
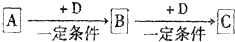 已知A、B、C是中学化学的常见物质,它们在一定条件下有如图所示转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如图所示转化关系:(1)若A能使湿润的红色石蕊试纸变蓝,C为红棕色气体.则实验室常用的制取A的化学方程式为
2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑
| ||
2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑
,A转化为B的化学方程式为
| ||
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(2)若组成D单质的元素在地壳中含量最高,A元素焰色反应为黄色,则C的电子式为


(3)若D是金属,C溶液在贮存时应加入少量D,其理由是(只用离子方程式说明)
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
,A与D反应的化学方程式是2Fe+3Cl2
2FeCl3
| ||
2Fe+3Cl2
2FeCl3
.
| ||
(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子.则B转化为C的离子方程式为
CO2+CO32-+H2O=2HCO3-
CO2+CO32-+H2O=2HCO3-
.(5)若D为一种强碱,B具有两性,则C溶液中除氢氧根外还存在的阴离子的化学式为
AlO2-
AlO2-
. 已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:(1)若A能使湿润的红色石蕊试纸变蓝,C为红棕色气体,则A转化为B反应的化学方程为
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;
| ||
| △ |
(2)若D是具有氧化性的单质,A元素属于短周期主族金属元素,则C的电子式为


(3)若D是金属,C溶液在贮存时应加入少量D,其理由是(用离子方程式说明)
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
;(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子.则B转化为C的离子方程式为
CO2+CO32-+H2O=2HCO3-
CO2+CO32-+H2O=2HCO3-
.