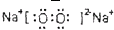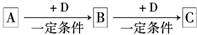题目内容
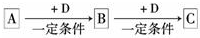 已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:(1)若A能使湿润的红色石蕊试纸变蓝,C为红棕色气体,则A转化为B反应的化学方程为
4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
;
| ||
| △ |
(2)若D是具有氧化性的单质,A元素属于短周期主族金属元素,则C的电子式为
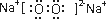
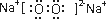
(3)若D是金属,C溶液在贮存时应加入少量D,其理由是(用离子方程式说明)
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
;(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子.则B转化为C的离子方程式为
CO2+CO32-+H2O=2HCO3-
CO2+CO32-+H2O=2HCO3-
.分析:(1)A能使湿润的红色石蕊试纸变蓝,应为NH3,C为红棕色气体,应为NO2,则B为NO,D为O2;
(2)D是具有氧化性的单质,A元素属于短周期主族金属元素,根据反应关系可知应为Na
Na2O
Na2O2的反应;
(3)D是金属,C溶液在贮存时应加入少量D,说明C易被氧化而变质,则A为Cl2,B为FeCl3,C为FeCl2,D为Fe;
(4)D是一种常见的温室气体,应为CO2,A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子,应为NaOH,则B为Na2CO3,C为NaHCO3,结合物质的性质解答该题.
(2)D是具有氧化性的单质,A元素属于短周期主族金属元素,根据反应关系可知应为Na
| O2 |
| O2 |
(3)D是金属,C溶液在贮存时应加入少量D,说明C易被氧化而变质,则A为Cl2,B为FeCl3,C为FeCl2,D为Fe;
(4)D是一种常见的温室气体,应为CO2,A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子,应为NaOH,则B为Na2CO3,C为NaHCO3,结合物质的性质解答该题.
解答:解:(1)A能使湿润的红色石蕊试纸变蓝,应为NH3,C为红棕色气体,应为NO2,则B为NO,D为O2,A转化为B反应的化学方程为4NH3+5O2
4NO+6H2O,
故答案为:4NH3+5O2
4NO+6H2O;
(2)D是具有氧化性的单质,A元素属于短周期主族金属元素,根据反应关系可知应为Na
Na2O
Na2O2的反应,C为Na2O2,电子式为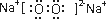 ,
,
故答案为: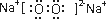 ;
;
(3)是金属,C溶液在贮存时应加入少量D,说明C易被氧化而变质,则A为Cl2,B为FeCl3,C为FeCl2,D为Fe,反应的原理为2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(4)D是一种常见的温室气体,应为CO2,A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子,应为NaOH,则B为Na2CO3,C为NaHCO3,
B转化为C的离子方程式为CO2+CO32-+H2O=2HCO3-,故答案为:CO2+CO32-+H2O=2HCO3-.
| ||
| △ |
故答案为:4NH3+5O2
| ||
| △ |
(2)D是具有氧化性的单质,A元素属于短周期主族金属元素,根据反应关系可知应为Na
| O2 |
| O2 |
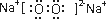 ,
,故答案为:
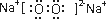 ;
;(3)是金属,C溶液在贮存时应加入少量D,说明C易被氧化而变质,则A为Cl2,B为FeCl3,C为FeCl2,D为Fe,反应的原理为2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(4)D是一种常见的温室气体,应为CO2,A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子,应为NaOH,则B为Na2CO3,C为NaHCO3,
B转化为C的离子方程式为CO2+CO32-+H2O=2HCO3-,故答案为:CO2+CO32-+H2O=2HCO3-.
点评:本题考查无机物的推断,题目难度不大,本题注意把握反应的转化特点,根据物质的性质、用途作为解答的突破口.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


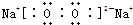
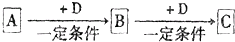 已知A、B、C是中学化学的常见物质,它们在一定条件下有如图所示转化关系:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如图所示转化关系: