摘要:23.已知抛物线上两个动点A(x1.y1).B(x2.y2)及一个定点M(1.2).F是 抛物线的焦点.若|AF|.|MF|.|BF|成等差数列.则x1+ x2= .
网址:http://m.1010jiajiao.com/timu3_id_54084[举报]
已知:下列两个热化学方程式:
Fe(s)+
O2(g)═FeO(s)?△H=-272.0KJ/mol
2Al(s)+
O2(g)═Al2O3(s)?△H=-1675.7KJ/mol
则 Al(s)的单质和FeO(s)反应的热化学方程式是
查看习题详情和答案>>
Fe(s)+
| 1 |
| 2 |
2Al(s)+
| 3 |
| 2 |
则 Al(s)的单质和FeO(s)反应的热化学方程式是
3FeO(s)+2Al(s)
Al2O3(s)+3Fe(s)?△H=-859.7KJ/mol
| ||
. |
3FeO(s)+2Al(s)
Al2O3(s)+3Fe(s)?△H=-859.7KJ/mol
.
| ||
. |
【化学-选修3物质结构与性质】
A、B、C、D、E、F是原子序数依次增大的前四周期元素.A、B、C三种元素的基态原子具有相同的能级和能层,且第一电离能的顺序为A<C<B,其中C原子基态时2p轨道有两个未成对电子;D与A同族,其单质为常用的半导体材料;E为前四周期由负性最小的元素;F原子内层无空轨道,最外层电子数与E相同.请回答:
(1)F的价层电子排布为 ;化合物F2C与稀硫酸反应的产物之一为红色固体,且反应中只有F元素的化合价发生了变化,该反应的离子方程为 .
(2)比较A、D的氢化物.稳定性:前者 后者;沸点:前者 后者(填“<”或“>”).
(3)C与氢元素形成的正一价离子含有10电子,该离子中C原子的杂化方式为 ;该离子的空间构型为 .C与氢元素形成的一种分子M的电子总数与E离子核外电子数相等,M分子为 分子(填“极性”或“非极性”).
(4)1molAC2分子中π键的数目为 个;B、C形成的正一价离子N与AC2互为等电子体,N的电子式为 ;
(5)AC2分子构成的晶体结构如图,已知最近的两个分子间距离为
acm阿伏伽德罗常数为NA,则该晶体的密度为 g/cm3.
查看习题详情和答案>>
A、B、C、D、E、F是原子序数依次增大的前四周期元素.A、B、C三种元素的基态原子具有相同的能级和能层,且第一电离能的顺序为A<C<B,其中C原子基态时2p轨道有两个未成对电子;D与A同族,其单质为常用的半导体材料;E为前四周期由负性最小的元素;F原子内层无空轨道,最外层电子数与E相同.请回答:
(1)F的价层电子排布为
(2)比较A、D的氢化物.稳定性:前者
(3)C与氢元素形成的正一价离子含有10电子,该离子中C原子的杂化方式为
(4)1molAC2分子中π键的数目为

(5)AC2分子构成的晶体结构如图,已知最近的两个分子间距离为
| 2 |
(1)家用液化气中主要成分之一是丁烷.在101kPa时,10kg丁烷(相对分子质量为58)完全燃烧生成CO2和液态H2O放出热量5×105 kJ,丁烷的燃烧热为
(2)已知:下列两个热化学方程式:
Fe(s)+
O2(g)═FeO(s)?△H=-272.0KJ/mol
2Al(s)+
O2(g)═Al2O3(s)?△H=-1675.7KJ/mol
则 Al(s)的单质和FeO(s)反应的热化学方程式是
查看习题详情和答案>>
2900kJ/mol
2900kJ/mol
,丁烷燃烧的热化学方程式为2C4H10(g)+13O2(g)═8CO2(g)+10H2O(l);△H=-5800kJ/mol
2C4H10(g)+13O2(g)═8CO2(g)+10H2O(l);△H=-5800kJ/mol
.(2)已知:下列两个热化学方程式:
Fe(s)+
| 1 |
| 2 |
2Al(s)+
| 3 |
| 2 |
则 Al(s)的单质和FeO(s)反应的热化学方程式是
3FeO(s)+2Al(s)
Al2O3(s)+3Fe(s)?△H=-859.7KJ/mol
| ||
. |
3FeO(s)+2Al(s)
Al2O3(s)+3Fe(s)?△H=-859.7KJ/mol
.
| ||
. |
[化学-选修3:物质结构与性质]
砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩.
(1)砷的基态原子的电子排布式为 .
(2)目前市售的发光二极管,其材质以砷化镓(GaAs)为主.Ga和As相比,电负性较大的 是 ,GaAs中Ga的化合价为
(3)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为 ;AsH3的沸点高于PH3,其主要原因为
(4)Na3As04可作杀虫剂.As043-的立体构型为 与其互为等电子体的分子的化学式为 (任写一种).
(5)H3As04和H3As03是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比 H3AsO3 酸性强的原因 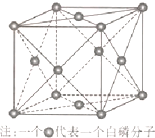
(6)磷与砷同主族,磷的一种单质白磷(P4)属于分子晶体,其晶胞如图.已知最近的两个白磷分子间距离为 a pm,阿伏加德罗常数的值为NA,则该晶体的密度为 g/cm3(只要求列算式,不必计算)
查看习题详情和答案>>
砷(As)在地壳中含量不大,但砷的化合物却是丰富多彩.
(1)砷的基态原子的电子排布式为
(2)目前市售的发光二极管,其材质以砷化镓(GaAs)为主.Ga和As相比,电负性较大的 是
(3)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为
(4)Na3As04可作杀虫剂.As043-的立体构型为
(5)H3As04和H3As03是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比 H3AsO3 酸性强的原因

(6)磷与砷同主族,磷的一种单质白磷(P4)属于分子晶体,其晶胞如图.已知最近的两个白磷分子间距离为 a pm,阿伏加德罗常数的值为NA,则该晶体的密度为
(2010?湘潭三模)某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用图甲装置进行有关实验,请回答:
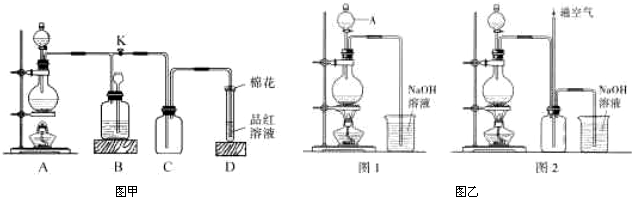
(1)装置D中试管口放置的棉花中应浸一种液体,这种液体的作用是
(2)装置B的作用是贮存多余的气体,B中应放置的液体是(填字母)
a.NaOH溶液 b.酸性KmnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是
(3)铜不能与稀硫酸直接反应得到硫酸铜,但可用下面方法制取:将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发浓缩、冷却结晶可制得硫酸铜晶体(装置如图乙图1、2所示).
①将硝酸分多次加入到铜粉与稀硫酸的混合物中,写出该反应的离子方程式
②已知NO不能被NaOH溶液直接吸收,但已知有如下两个反应:
NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO3+NaNO2+H2O.图2是图1的改进装置,其优点除可以防止倒吸外还有:
(3)如果用1molCu来制取1molCuSO4,则所需12mol/L的硝酸体积为
查看习题详情和答案>>

(1)装置D中试管口放置的棉花中应浸一种液体,这种液体的作用是
防止SO2扩散而造成污染气体
防止SO2扩散而造成污染气体
.(2)装置B的作用是贮存多余的气体,B中应放置的液体是(填字母)
d
d
.a.NaOH溶液 b.酸性KmnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是
长颈漏斗导管中液柱升高
长颈漏斗导管中液柱升高
.(3)铜不能与稀硫酸直接反应得到硫酸铜,但可用下面方法制取:将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发浓缩、冷却结晶可制得硫酸铜晶体(装置如图乙图1、2所示).
①将硝酸分多次加入到铜粉与稀硫酸的混合物中,写出该反应的离子方程式
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.②已知NO不能被NaOH溶液直接吸收,但已知有如下两个反应:
NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO3+NaNO2+H2O.图2是图1的改进装置,其优点除可以防止倒吸外还有:
促进氮的氧化物被充分吸收
促进氮的氧化物被充分吸收
.(3)如果用1molCu来制取1molCuSO4,则所需12mol/L的硝酸体积为
55.6
55.6
mL,(假设HNO3的还原产物全为NO),若所得尾气恰好被NaOH溶液完全吸收,需通入空气的体积为18.7L
18.7L
.(假设实验体积为标准状况下测定,并忽略装置中原有空气的影响,以上数据均保留小数点后一位.)