摘要:用电极反应式.离子方程式.化学方程式表示家用菜锅生锈的过程
网址:http://m.1010jiajiao.com/timu3_id_52224[举报]
 [化学--物质的结构与性质]
[化学--物质的结构与性质]砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%,推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措,已知砷化镓的晶胞结构如图.试回答下列问题
(1)下列说法正确的是
BCDE
BCDE
(选填序号).A.砷化镓晶胞结构与NaCl相同
B.第一电离能:As>Ga
C.电负性:As>Ga
D.砷和镓都属于p区元素
E.半导体GaP、SiC与砷化镓为等电子体
(2)砷化镓是将(CH3)3Ga和AsH3用MOCVD方法制备得到,该反应在700℃进行,反应的方程式为:
(CH3)3Ga+AsH3
GaAs+3CH4
| 700℃ |
(CH3)3Ga+AsH3
GaAs+3CH4
.| 700℃ |
AsH3空间形状为:
三角锥
三角锥
(CH3)3Ga中镓原子杂化方式为:sp2
sp2
.(3)Ga的核外电子排布式为:
1s22s22p63s23p63d104s24p1
1s22s22p63s23p63d104s24p1
.(4)AsH3沸点比NH3低,其原因是:
NH3分子间能形成氢键,而As电负性小,半径大,分子间不能形成氢键
NH3分子间能形成氢键,而As电负性小,半径大,分子间不能形成氢键
.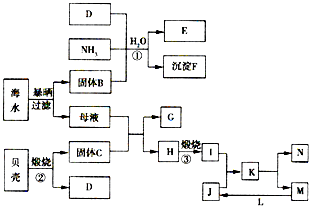 [化学与技术]海洋是巨大的资源宝库,从海洋中我们可以获得各种各样的化学物质,下图是综合利用海洋资源的一个例子(假设海水中存在的离子主要有Na+、Mg2+、Cl-).
[化学与技术]海洋是巨大的资源宝库,从海洋中我们可以获得各种各样的化学物质,下图是综合利用海洋资源的一个例子(假设海水中存在的离子主要有Na+、Mg2+、Cl-).(1)反应①是著名的侯氏制碱法生产原理中的重要反应,其化学反应方程式是
NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
.实际生产中,在固体B的溶液中是先通入D气体还是先通入NH3?
先通入NH3
先通入NH3
.(2)对固体B精制后,用惰性电极电解其水溶液,阴极的电极反应式为
2H++2e-=H2↑
2H++2e-=H2↑
.(3)在上述转化关系中,电解熔融态的K可制得一种常见的金属N.写出该反应的化学方程式
MgCl2
Mg+Cl2↑
| ||
MgCl2
Mg+Cl2↑
.
| ||
(4)由K溶液经如何处理才能制得N?
MgCl2溶液要在HCl气体氛围中进行蒸发结晶制得MgCl2晶体,熔融后电解才能制取金属镁
MgCl2溶液要在HCl气体氛围中进行蒸发结晶制得MgCl2晶体,熔融后电解才能制取金属镁
.化学电池在日常生活中有着广泛的应用.
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:
Cd+2NiO(OH)+2H2O
2Ni(OH)2+Cd(OH)2
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是
①以上电池反应是在非水溶液中进行的 ②以上电池反应是在强碱溶液中进行的
③以上电池反应不需要电解质就能进行 ④电池工作时是化学能转变为电能
A.①③B.②④C.①④D.②③
(2)另一种常用的电池是锂电池由于它的容量特别大而广泛应用于心脏起搏器,一般使用时间可长达十年.电池总反应可表示为:Li+MnO2=LiMnO2,它的负极材料是
(3)铅蓄电池是典型的可充型电池,电池总反应式为:
Pb+PbO2+4H++2SO
2PbSO4+2H2O
放电时电解液中H2SO4的浓度将变
(4)随着人们生活质量的不断提高,废弃的电池必须进行集中处理的问题被提到议事日程,其首要原因是
查看习题详情和答案>>
(1)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:
Cd+2NiO(OH)+2H2O
| 放电 |
| 充电 |
已知Ni(OH)2和Cd(OH)2均难溶于水但能溶于酸,以下说法中正确的是
B
B
.①以上电池反应是在非水溶液中进行的 ②以上电池反应是在强碱溶液中进行的
③以上电池反应不需要电解质就能进行 ④电池工作时是化学能转变为电能
A.①③B.②④C.①④D.②③
(2)另一种常用的电池是锂电池由于它的容量特别大而广泛应用于心脏起搏器,一般使用时间可长达十年.电池总反应可表示为:Li+MnO2=LiMnO2,它的负极材料是
锂
锂
,电极反应式为Li-e-=Li+
Li-e-=Li+
;锂电池中的电解质溶液需用非水溶剂配制,其原因用化学方程式表示为2Li+2H2O=2LiOH+H2↑
2Li+2H2O=2LiOH+H2↑
.(3)铅蓄电池是典型的可充型电池,电池总反应式为:
Pb+PbO2+4H++2SO
2- 4 |
| 放电 |
| 充电 |
放电时电解液中H2SO4的浓度将变
小
小
;当外电路通过1mol电子时,理论上负极板的质量增加48
48
g.(4)随着人们生活质量的不断提高,废弃的电池必须进行集中处理的问题被提到议事日程,其首要原因是
防止电池中的汞、镉和铅等重金属离子对土壤和水源的污染
防止电池中的汞、镉和铅等重金属离子对土壤和水源的污染
.[化学-选修化学与技术]金属钛(Tl)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”.常温下,钛的化学活性很小,仅能与氧气、氢氟酸等几种物质起反应.但在较高温度下,钛可与多种单质和化合物发生反应.以钛铁矿(主要成分FeTlO2,钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下:
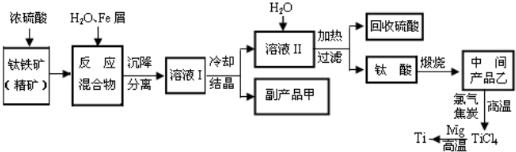
请回答下列问题:
(1)钛铁矿和浓硫酸反应的产物之一是TlOSO4,无气体生成,副产品甲是 .
(2)上述生产流程中加入Fe的目的是 ,检验副产品甲是否变质的实验方法是 .
(3)上述生产流程中所得一的金属钛中混有少量杂质,可加入 溶解后除去.
(4)科学家从电解冶炼铝的工艺得到启发,找到了冶炼钛的新工艺,它可以用熔融法直接电解中间产品乙制取金属法.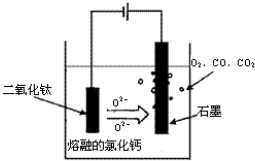
①直接电解法(剑桥法)生产钛是种较先进的方法,电解质为熔融的氧化钙,原理如图所示;在阴极,被还原的Ca进一步还原TlO2获得钛,可能发生的反应或电极反应为 .
②SOM技术是一种绿色环保先进技术,阳极用金属陶瓷,并用固体氧离子隔膜将两 极产物隔开,只允许氧离子通过,在电解过程中阳极通入某种还原性气体,可防止CO、CO2污染物产生,通入的气体若是单质,可以是 ,则阳极发生的电极反应式为 .
查看习题详情和答案>>

请回答下列问题:
(1)钛铁矿和浓硫酸反应的产物之一是TlOSO4,无气体生成,副产品甲是
(2)上述生产流程中加入Fe的目的是
(3)上述生产流程中所得一的金属钛中混有少量杂质,可加入
(4)科学家从电解冶炼铝的工艺得到启发,找到了冶炼钛的新工艺,它可以用熔融法直接电解中间产品乙制取金属法.

①直接电解法(剑桥法)生产钛是种较先进的方法,电解质为熔融的氧化钙,原理如图所示;在阴极,被还原的Ca进一步还原TlO2获得钛,可能发生的反应或电极反应为
②SOM技术是一种绿色环保先进技术,阳极用金属陶瓷,并用固体氧离子隔膜将两 极产物隔开,只允许氧离子通过,在电解过程中阳极通入某种还原性气体,可防止CO、CO2污染物产生,通入的气体若是单质,可以是
[化学-选修/物质结构与性质]
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于 .
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为 .
(2)下表为元素周期表的一部分,根据此表回答下列问题:
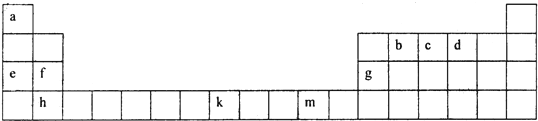
①f、g、h三种元素的第一电离能由小到大的顺序是 (用元素符号表示),b、c、d三种元素的电负性由大到小的顺序是 (用元素符号表示),b、c、d分别与a形成的简单化合物分子中,属于含有极性键的非极性分子是 .(填写化学式)
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式 .
目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为 .
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
,其中各原子的最外层电子均满足8电子稳定结构.该阴离子的中心原子的杂化轨道方式为 杂化,阴离子的电子式为 .
查看习题详情和答案>>
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为
(2)下表为元素周期表的一部分,根据此表回答下列问题:

①f、g、h三种元素的第一电离能由小到大的顺序是
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式

目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
3- 4 |