��Ŀ����
��1��Ŀǰ���õ�����Ni���ӣ�Cd����أ������ܷ�Ӧ���Ա�ʾΪ��
Cd+2NiO��OH��+2H2O
| �ŵ� |
| ��� |
��֪Ni��OH��2��Cd��OH��2��������ˮ���������ᣬ����˵������ȷ����
�����ϵ�ط�Ӧ���ڷ�ˮ��Һ�н��е� �����ϵ�ط�Ӧ����ǿ����Һ�н��е�
�����ϵ�ط�Ӧ����Ҫ����ʾ��ܽ��� �ܵ�ع���ʱ�ǻ�ѧ��ת��Ϊ����
A���٢�B���ڢ�C���٢�D���ڢ�
��2����һ�ֳ��õĵ����﮵���������������ر����㷺Ӧ��������������һ��ʹ��ʱ��ɳ���ʮ�꣮����ܷ�Ӧ�ɱ�ʾΪ��Li+MnO2=LiMnO2�����ĸ���������
��3��Ǧ�����ǵ��͵Ŀɳ��͵�أ�����ܷ�ӦʽΪ��
Pb+PbO2+4H++2SO
2- 4 |
| �ŵ� |
| ��� |
�ŵ�ʱ���Һ��H2SO4��Ũ�Ƚ���
��4�������������������IJ�����ߣ������ĵ�ر�����м��д��������ⱻ�ᵽ�����ճ̣�����Ҫԭ����
��2��ԭ����У�������ʧ���ӷ���������Ӧ����ǻ��ý�������ˮ��Ӧ����������﮺�������
��3�����ݵ�ط�Ӧʽ֪���÷�Ӧ���������ӷ�Ӧ�Ҹ÷�Ӧ������ˮ������ת�Ƶ��Ӻ����缫��Ӧʽ֮��Ĺ�ϵʽ���㣻
��4���ؽ�����������ˮ��Դ������Ⱦ��
�ڸ��ݵ�ط�Ӧʽ֪��Ni��OH��2��Cd��OH��2��������ˮ���������ᣬ���Ըõ�ط�ӦӦ������ǿ����ˮ��Һ����еģ�����ȷ��
�۸÷�Ӧ��Ҫǿ���Ե���ʣ��ʴ���
�ܸõ�طŵ�ʱ���ǽ���ѧ��ת��Ϊ���ܣ�����ȷ��
��ѡB��
��2���õ�ط�Ӧ�У��������ʧ���ӷ���������Ӧ���缫��ӦʽΪLi-e-=Li+����ǻ��ý�������ˮ��Ӧ����������﮺�������2Li+2H2O=2LiOH+H2����
�ʴ�Ϊ��ﮣ�Li-e-=Li+��2Li+2H2O=2LiOH+H2����
��3���ŵ�ʱ������μӷ�Ӧ��������Ǧ��ˮ�����������Ũ����С��������Ǧʧ���Ӻ���������ӷ�Ӧ���������Ե�����Ǧ�����Ը����������ӵ�������������ӵ���������Pb-2e-+SO42-=PbSO4֪����ת��1mol����ʱ�������ӵ�����=
| 1mol |
| 2 |
�ʴ�Ϊ��С��48��
��4������к��й�������Ǧ���ؽ�������Щ�ؽ�����������ˮ��Դ�������Ⱦ�����Է������Ҫ���д�����������㶪����
�ʴ�Ϊ����ֹ����еĹ����Ӻ�Ǧ���ؽ������Ӷ�������ˮԴ����Ⱦ��

������Ԫ��X��Y��Z��W���������е�λ�ù�ϵ����ͼ��ʾ����֪��ͬ����Ԫ�صij����������У�W�ļ����Ӱ뾶��С��X��Y��Z��W�ĵ��ʼ��仯�������ճ���������;����㷺��
| X | Y | Z |
W |
|
|
|
��1��XԪ����Ԫ�����ڱ��е�λ��___? __________��
��2��X��Y��ZԪ�ص��⻯��������ֻ��������ϣ�����һ�������£�Һ̬YH3��Һ̬H2Z���Է������Ʒ�ʽ���룬��Һ̬YH3�������ӵĵ���ʽΪ_______________��
��3����ϸWY��ĩ��Ӧ���ڴ��ģ���ɵ�·����������ԭ��ΪW2Z3��Y2��X�ڸ����·�Ӧ�������ֻ���������ֻ������������Ԫ����ɣ���ԭ�Ӹ����Ⱦ�Ϊ1��1���䷴Ӧ�Ļ�ѧ����ʽΪ????????????????????????????? _��
��4����WΪ�����Ƴɵ������ڿ����о������ұ������ã���������____����ܡ����ܡ������������̲ˣ�ԭ����_________________________________________��
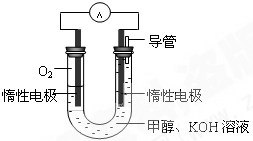
��5��ij����β����������ȼ�ϵ��Ϊ����ԭ���ⶨXZ��Ũ�ȣ���װ����ͼ��ʾ���õ���е����Ϊ�����ƣ������ƣ�����Z2-�����ڹ������NASICON�������ƶ������ķ�Ӧʽ___________��

���ڸõ�ص�����˵������ȷ����______
A������ʱ�缫b��������Z2- ͨ���������NASICON�ɵ缫b����缫a
B������ʱ�����ɵ缫aͨ������������缫b
C����������ͨ���ĵ���Խ��β����XZ�ĺ���Խ��
��6����Ԫ��X��Ԫ��Z��ɵ�ij�������Ӿ��л�ԭ�ԣ��ܱ�����KMnO4����������д��Ӧ�����ӣ���������ƽ��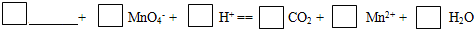 ��
��
 �״�����Ҫ�Ļ���ԭ�ϣ����ճ����������Ź㷺��Ӧ�ã�
�״�����Ҫ�Ļ���ԭ�ϣ����ճ����������Ź㷺��Ӧ�ã� CH3OH��g����H1
CH3OH��g����H1 CH3OH��g��+H2O��g����H2
CH3OH��g��+H2O��g����H2