摘要:17].已知25℃.101kPa下.石墨.金刚石燃烧的热化学方程式分别为: C+O2(g)=CO2(g),ΔH=-393.51 kJ.mol-1 C+O2(g)=CO2(g),ΔH=-395.41 kJ.mol-1 据此推理所得到的下列结论正确的是 A 金刚石的燃烧热比石墨的燃烧热小 B 石墨晶体中碳碳键的键能大于金刚石中的碳碳键 C 石墨的能量比金刚石的能量高 D 由石墨制备金刚石一定是吸热反应
网址:http://m.1010jiajiao.com/timu3_id_435358[举报]
已知25℃下,醋酸溶液中存在下列平衡:CH3COOH?CH3COO-+H+
Ka=
=1.75×10-5
请回答下列问题(已知:1.322=1.75;4.182=17.5)
(1)在25℃下,当向该溶液中加入一定量的盐酸时,上式中的Ka值是否发生变化?
(2)若醋酸溶液的浓度为0.010mol/L,计算该溶液中c(H+)是多少?(提示:醋酸的电离常数较小,平衡时的c(CH3COOH)仍可视为0.010mol/L.)
查看习题详情和答案>>
Ka=
| c(H+)?c(CH3COO-) | c(CH3COOH) |
请回答下列问题(已知:1.322=1.75;4.182=17.5)
(1)在25℃下,当向该溶液中加入一定量的盐酸时,上式中的Ka值是否发生变化?
(2)若醋酸溶液的浓度为0.010mol/L,计算该溶液中c(H+)是多少?(提示:醋酸的电离常数较小,平衡时的c(CH3COOH)仍可视为0.010mol/L.)
已知25℃,氯化银的KSP=1.8×10-10,碘化银的KSP=8.5×10-17.请解答下列问题:
(1)在25℃时,将0.002mol?L-1化钠溶液和0.001mol?L-1硝酸银溶液等体积混合后,混合溶液中 (填“有”、“无”或“无法判断”)氯化银沉淀生成,原因是 .
(2)在25%℃时,将足量氯化银分别放入:①50mL蒸馏水中;②50mL 0.2mol?L-1盐酸中;②50mL 0.2mol?L-1氯化铝溶液中;④50mL 0.2mol?L-1氯化镁溶液中.充分搅拌后,溶液中银离子浓度最小的是 (填序号).在0.2mol?L-1氯化镁溶液中,银子里的浓度最大可达到 mol?L-1.
(3)在含有0.001mol?L-1碘化钠和0.00l mol?L-1氯化钠的混合溶渣中,逐滴加入硝酸银溶液,刚此时首先生成的沉淀是 (填化学式);当氯化银沉淀开始生成时,溶液中I-的物质的量浓度是 .(计算结果保留一位小数)
查看习题详情和答案>>
(1)在25℃时,将0.002mol?L-1化钠溶液和0.001mol?L-1硝酸银溶液等体积混合后,混合溶液中
(2)在25%℃时,将足量氯化银分别放入:①50mL蒸馏水中;②50mL 0.2mol?L-1盐酸中;②50mL 0.2mol?L-1氯化铝溶液中;④50mL 0.2mol?L-1氯化镁溶液中.充分搅拌后,溶液中银离子浓度最小的是
(3)在含有0.001mol?L-1碘化钠和0.00l mol?L-1氯化钠的混合溶渣中,逐滴加入硝酸银溶液,刚此时首先生成的沉淀是
(2011?金丽衢十二校联考)已知25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17,25℃时AgCl固体在下列四个选项中,溶解度最大的是( )
查看习题详情和答案>>
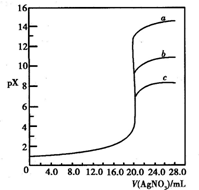 用0.1mol?L-1?AgNO3溶液分别滴定20.00mL含Cl-、Br-、I-浓度均为0.1mol?L-1的溶液,以滴入的AgNO3溶液的体积为横坐标,pX为纵坐标[pX=-lg c(X),X=Cl-、Br-、I-],可得如图所示的滴定曲线.已知25℃时,部分难溶盐的Ksp和颜色如表所示: 用0.1mol?L-1?AgNO3溶液分别滴定20.00mL含Cl-、Br-、I-浓度均为0.1mol?L-1的溶液,以滴入的AgNO3溶液的体积为横坐标,pX为纵坐标[pX=-lg c(X),X=Cl-、Br-、I-],可得如图所示的滴定曲线.已知25℃时,部分难溶盐的Ksp和颜色如表所示:
|
已知25℃时,AgC1、AgBr、Agl的Ksp分别为1.8×l0-l0、5.O×10—13、8.3×10—17,用AgNO3标准溶液滴定卤素离子的过程,以滴入AgNO3溶液的体积为横坐标,pX为纵坐标:[pX= -lgc(X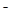 )],就可绘得滴定曲线。现以0.1 mol·L-l AgNO3溶液分别滴定20.00 mL 0.1 mol·L-lCl
)],就可绘得滴定曲线。现以0.1 mol·L-l AgNO3溶液分别滴定20.00 mL 0.1 mol·L-lCl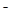 、Br
、Br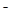 、I
、I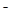 绘得滴定曲线如图,下列有关说法中正确的是
绘得滴定曲线如图,下列有关说法中正确的是
A.a、b、c分别表示Cl 、Br 、Br 、I 、I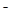 |
B.a、b、c分别表示I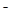 、Br 、Br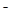 、Cl 、Cl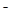 |
C.a、b、c分别表示Br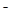 、I 、I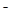 、Cl 、Cl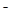 |
D.用硝酸银滴定法测定试样中c(Cl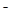 ),可用KI作指示剂 ),可用KI作指示剂 |