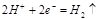摘要:7.(改编自江苏省2011高三二轮检测)如图所示的两个实验装置中.溶液的体积均为 200 mL.开始时电解质溶液的浓度均为0.1 mol/L.工作一段时间后.测得导线中均通过0.02 mol电子.若不考虑气体的溶解和溶液体积的变化.则下列叙述中正确的是 A.产生气体的体积:①>② B.电极上析出物质的质量:①>② C.溶液的pH变化:①增大.②减小 D.电极反应式:②中负极:Zn―2e―=Zn2+.①中阳极:Cu2++2e―=Cu
网址:http://m.1010jiajiao.com/timu3_id_433575[举报]
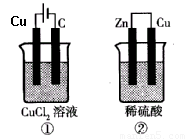
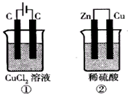 如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
查看习题详情和答案>>
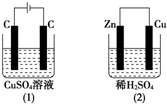 如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中正确的是( )
如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上均通过0.02mol电子,若不考虑溶液体积的变化,则下列叙述中正确的是( )
查看习题详情和答案>>
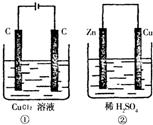 如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑气体的溶解和溶液体积的变化,则下列叙述中正确的是( )
如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑气体的溶解和溶液体积的变化,则下列叙述中正确的是( )
查看习题详情和答案>>
 (2011?顺德区模拟)(1)在-50℃时,液氨存在如下电离:2NH3?NH4++NH-2,k=2×10-12,液氨的电离达到平衡时,各微粒的浓度大小关系为
(2011?顺德区模拟)(1)在-50℃时,液氨存在如下电离:2NH3?NH4++NH-2,k=2×10-12,液氨的电离达到平衡时,各微粒的浓度大小关系为c(NH3)>c(NH4+)=c(NH2-)
c(NH3)>c(NH4+)=c(NH2-)
,加入NH4Cl固体,K=
=
2×10-12(填“<”、“>”或“=”)(2)已知25℃时Ksp(AgCl)=1.8×10--10,在10mL 0.10mol/L AgNO3溶液中加入10mL0.20mol/LNaCl溶液,充分反应后溶液中的c(Ag+)=
3.6×10-9mol/L
3.6×10-9mol/L
.(3)配平硫酸亚铁加强热制备铁红和生成硫的两种常见氧化物的化学方程式:
2
2
FeSO4| 高温 |
1
1
Fe2O3+1
1
SO2↑
SO2↑
+1
1
SO3↑
SO3↑
(4)已知氯气能溶于水,溶液呈酸性.如图所示的两个实验装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是
BC
BC
A.产生气体的体积:①>②
B.溶液的pH变化:①减小,②增大
C.电极上析出物质的质量:①>②
D.电极反应式:①中阳极 2Cl--2e-?Cl2↑ ②中负极 2H++2e-?H2↑
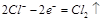 ②中负极
②中负极