摘要:27.为了测定混有少量KCl杂质的明矾KAl(SO4)2·nH2O的纯度.同时测定n的值.按下列流程进行实验: (1)晶块磨碎时使用的仪器名称 , (2)若加热过程中有固体飞溅出来造成损失.则会使测得的n值偏 .判断已脱水至恒重的方法是 , (3)在加热结束后.如何冷却固体? , (4)A溶液是 .判断A溶液是否足量的方法是 , (5)过滤后还需将沉淀洗涤干净.洗涤方法是 , (6)通过实验.测得明矾化学式中n值为12.则明矾的纯度为 %. www.k@s@5@ 高#考#资#源#网
网址:http://m.1010jiajiao.com/timu3_id_433105[举报]
为了测定混有少量KCl杂质的明矾KAl(SO4)2?nH2O的纯度,同时测定n的值,按下列流程进行实验:

(1)晶块磨碎时使用的仪器名称
(2)若加热过程中有固体飞溅出来造成损失,则会使测得的n值偏
(3)在加热结束后,如何冷却固体?
(4)A溶液是
(5)过滤后还需将沉淀洗涤干净,洗涤方法是
(6)通过实验,测得明矾化学式中n值为12,则明矾的纯度为
%.
查看习题详情和答案>>

(1)晶块磨碎时使用的仪器名称
研钵
研钵
;(2)若加热过程中有固体飞溅出来造成损失,则会使测得的n值偏
高
高
,判断已脱水至恒重的方法是两次称量质量差不超过0.1g
两次称量质量差不超过0.1g
;(3)在加热结束后,如何冷却固体?
用坩埚钳把坩埚移到干燥器中冷却
用坩埚钳把坩埚移到干燥器中冷却
;(4)A溶液是
BaCl2
BaCl2
(填化学式),判断A溶液是否足量的方法是静置后向上层清液滴加适量A观察有无沉淀产生
静置后向上层清液滴加适量A观察有无沉淀产生
;(5)过滤后还需将沉淀洗涤干净,洗涤方法是
用玻璃棒引流加入蒸馏水至浸没过沉淀物,待水流完后重复以上操作至洗净为止
用玻璃棒引流加入蒸馏水至浸没过沉淀物,待水流完后重复以上操作至洗净为止
;(6)通过实验,测得明矾化学式中n值为12,则明矾的纯度为
| 23700m2 |
| 233m |
| 23700m2 |
| 233m |
为了测定混有少量KCl杂质的明矾KAl(SO4)2?nH2O的纯度,同时测定n的值,按下列流程进行实验:

(1)称量样品需用托盘天平,下列有关使用托盘天平的叙述,不正确的是
A、称量前先调节托盘天平的零点
B、称量时左盘放被称量物,右盘放砝码
C、潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量
D、用托盘天平可以准确称量至0.01克
E、称量完毕,应把砝码放回砝码盒中
(2)判断已脱水至恒重的方法是
A、长时间加热 B、两次称量的质量必须一样
C、观察有水蒸气不再冒出 D、两次称量的质量差不超过0.1g
(3)在加热结束后,冷却固体的操作为
(4)A溶液是
(5)通过实验,测得明矾化学式中n值为12,则明矾的纯度为
%.(已知KAl(SO4)2?12H2O的式量为474)
查看习题详情和答案>>

(1)称量样品需用托盘天平,下列有关使用托盘天平的叙述,不正确的是
C、D
C、D
.A、称量前先调节托盘天平的零点
B、称量时左盘放被称量物,右盘放砝码
C、潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量
D、用托盘天平可以准确称量至0.01克
E、称量完毕,应把砝码放回砝码盒中
(2)判断已脱水至恒重的方法是
D
D
A、长时间加热 B、两次称量的质量必须一样
C、观察有水蒸气不再冒出 D、两次称量的质量差不超过0.1g
(3)在加热结束后,冷却固体的操作为
用坩埚钳把坩埚移到干燥器中冷却
用坩埚钳把坩埚移到干燥器中冷却
;(4)A溶液是
BaCl2(其它试剂只要合理也可以)
BaCl2(其它试剂只要合理也可以)
(填化学式),判断A溶液是否足量的方法是静置给上层清液滴加适量A观察有无沉淀产生
静置给上层清液滴加适量A观察有无沉淀产生
;(5)通过实验,测得明矾化学式中n值为12,则明矾的纯度为
| 23700m2 |
| 233m |
| 23700m2 |
| 233m |
为了测定混有少量KCl杂质的明矾KAl(SO4)2?nH2O的纯度,同时测定n的值,按下列流程进行实验:
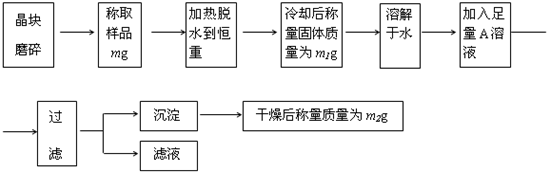
(1)称量样品需用托盘天平,下列有关使用托盘天平的叙述,不正确的是______.
A、称量前先调节托盘天平的零点
B、称量时左盘放被称量物,右盘放砝码
C、潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量
D、用托盘天平可以准确称量至0.01克
E、称量完毕,应把砝码放回砝码盒中
(2)判断已脱水至恒重的方法是______
A、长时间加热 B、两次称量的质量必须一样
C、观察有水蒸气不再冒出 D、两次称量的质量差不超过0.1g
(3)在加热结束后,冷却固体的操作为______;
(4)A溶液是______(填化学式),判断A溶液是否足量的方法是______;
(5)通过实验,测得明矾化学式中n值为12,则明矾的纯度为______%.(已知KAl(SO4)2?12H2O的式量为474)
查看习题详情和答案>>
为了测定混有少量KCl杂质的明矾KAl(SO4)2?nH2O的纯度,同时测定n的值,按下列流程进行实验:
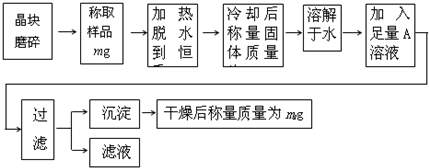
(1)晶块磨碎时使用的仪器名称______;
(2)若加热过程中有固体飞溅出来造成损失,则会使测得的n值偏______,判断已脱水至恒重的方法是______;
(3)在加热结束后,如何冷却固体?______;
(4)A溶液是______(填化学式),判断A溶液是否足量的方法是______;
(5)过滤后还需将沉淀洗涤干净,洗涤方法是______;
(6)通过实验,测得明矾化学式中n值为12,则明矾的纯度为______%.
查看习题详情和答案>>
为了测定混有少量KCl杂质的明矾KAl(SO4)2?nH2O的纯度,同时测定n的值,按下列流程进行实验:
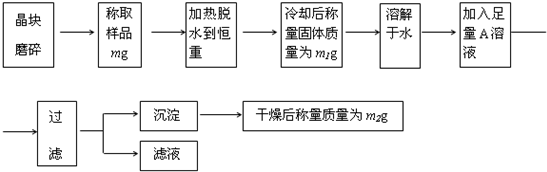
(1)称量样品需用托盘天平,下列有关使用托盘天平的叙述,不正确的是______.
A、称量前先调节托盘天平的零点
B、称量时左盘放被称量物,右盘放砝码
C、潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量
D、用托盘天平可以准确称量至0.01克
E、称量完毕,应把砝码放回砝码盒中
(2)判断已脱水至恒重的方法是______
A、长时间加热 B、两次称量的质量必须一样
C、观察有水蒸气不再冒出 D、两次称量的质量差不超过0.1g
(3)在加热结束后,冷却固体的操作为______;
(4)A溶液是______(填化学式),判断A溶液是否足量的方法是______;
(5)通过实验,测得明矾化学式中n值为12,则明矾的纯度为______%.(已知KAl(SO4)2?12H2O的式量为474)
查看习题详情和答案>>

(1)称量样品需用托盘天平,下列有关使用托盘天平的叙述,不正确的是______.
A、称量前先调节托盘天平的零点
B、称量时左盘放被称量物,右盘放砝码
C、潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量
D、用托盘天平可以准确称量至0.01克
E、称量完毕,应把砝码放回砝码盒中
(2)判断已脱水至恒重的方法是______
A、长时间加热 B、两次称量的质量必须一样
C、观察有水蒸气不再冒出 D、两次称量的质量差不超过0.1g
(3)在加热结束后,冷却固体的操作为______;
(4)A溶液是______(填化学式),判断A溶液是否足量的方法是______;
(5)通过实验,测得明矾化学式中n值为12,则明矾的纯度为______%.(已知KAl(SO4)2?12H2O的式量为474)