网址:http://m.1010jiajiao.com/timu3_id_420180[举报]
下列有关化工生产的说法中不正确的是
A.工业上用电解熔融的氯化物的方法制备金属镁和铝
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
C.从安全运输上看,硫酸厂靠近硫酸消费中心比靠近原料产地更为有利
D.利用反应NaCl(饱和)+CO2+NH3+H2O=NH4Cl+NaHCO3↓制取NaHCO3时,应在NaCl饱和溶液中先通入过量CO2再通入过量的NH3
E.硫酸厂生产时常采有高压条件提高SO2的转化率
(II)
过碳酸钠(2Na2CO3?3H2O2)俗称固体双氧水,被大量用于洗涤、印染、纺织、造纸、医药卫生等领域中.它的制备原理和路线如下:
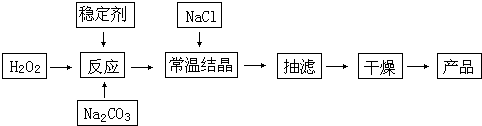
试回答下列问题:
(1)与过碳酸钠的用途相关的化学性质是
A.MnO2 B. H2S C.稀硫酸 D. NaHCO3
(2)加入NaCl的作用是
(3)工业纯碱中含有Fe3+等杂质,加入稳定剂的作用是与生成稳定的配合物.Fe3+的不良影响是
| ||
| ||
(4)反应的最佳温度控制在15~25℃,温度偏高时造成产率偏低的可能原因是
(5)有人想用过碳酸钠测定氢溴酸的浓度.若一定量的过碳酸钠与100mL氢溴酸溶液恰好完全反应,在标准状况下产生448mL气体,则所用氢溴酸的浓度为
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质).则下列有关Y的意义的叙述正确的是

A.a图表示第三周期元素的原子半径(稀有气体除外)
B.b图表示ⅡA族元素的最外层电子数
C.c图表示第二周期元素的电负性(稀有气体除外)
D.d图表示第三周期元素的第一电离能(稀有气体除外)
E.e图表示第ⅦA族元素氢化物的沸点
(II)
波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上,鲜蓝色的胆矾晶体是配制波尔多液的主要原料.胆矾CuSO4?5H2O可写成[Cu(H2O)4]SO4?H2O,其结构示意图如下:

(1)写出铜原子价层电子的轨道排布式


(2)由上图可知:胆矾中存在的作用力有
a.离子键 b.配位键 c.氢键 d.极性键 e.非极性键
(3)往浓CuSO4溶液中加入过量较浓的NH3?H2O直到原先生成的沉淀恰好溶解为止,得到深蓝色溶液.小心加入约和溶液等体积的C2H5OH并使之分成两层,静置.经过一段时间后可观察到在两层“交界处”下部析出深蓝色Cu(NH3)4SO4?H2O晶体.实验中所加C2H5OH的作用是
(4)已知Cu(NH3)42+呈平面正方形结构,则Cu(NH3)4SO4?H2O晶体中呈正四面体的粒子是
(5)如将深蓝色溶液加热,可能得到什么结果?
(20分)
(I)多项选择题(6分)
下列关于水处理的说法正确的是 。
A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程
B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度
C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术
D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化
E.电渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
(II)(14分)
下列是工业合成氨的简要流程示意图:
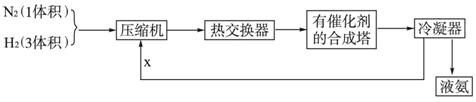
请回答下列问题:
(1)H2通常用碳氢化合物与水反应,写出有关的反应方程式 ,从冷凝器回流到压缩机中的X是 。
(2)比较工业上合成氨和SO2的催化氧化反应,其生产条件有哪些异同,并解释原因
。
(3)将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中,氨的体积分数为15%,则H2的体积分数为______________。
(4)NH3的用途之一是制造化肥,但在化肥的使用过程中要注意铵态氮肥不可以和草木灰混用,解释其原因 。
(5)NH3是一种重要的化工原料,除了制造化肥之外,再列举出两种NH3的用途
。
查看习题详情和答案>>
(20分)
(I)多项选择题(6分)
下列关于水处理的说法正确的是 。
A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程
B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度
C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术
D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化
E.电渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
(II)(14分)
下列是工业合成氨的简要流程示意图:
请回答下列问题:
(1)H2通常用碳氢化合物与水反应,写出有关的反应方程式 ,从冷凝器回流到压缩机中的X是 。
(2)比较工业上合成氨和SO2的催化氧化反应,其生产条件有哪些异同,并解释原因
。
(3)将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中,氨的体积分数为15%,则H2的体积分数为______________。
(4)NH3的用途之一是制造化肥,但在化肥的使用过程中要注意铵态氮肥不可以和草木灰混用,解释其原因 。
(5)NH3是一种重要的化工原料,除了制造化肥之外,再列举出两种NH3的用途
。
查看习题详情和答案>>
(20分)
(I)多项选择题(6分)
下列关于水处理的说法正确的是 。
| A.FeSO4·7H2O是常用的混凝剂,它除去悬浮固体颗粒的过程只是物理过程 |
| B.用纯碱和生石灰处理硬水,既可以除去暂时硬度,也可以除去永久硬度 |
| C.永久硬度的水可以采用离子交换法进行软化,其主要就是利用了离子交换膜技术 |
| D.污水处理中的三级处理是采用化学方法,对污水进行深度处理和净化 |
 渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜
渗析法是一种常用的海水淡化的方法,使用到的离子交换膜只有阳离子交换膜(II)(14分)
下列是工业合成氨的简要流程示意图:
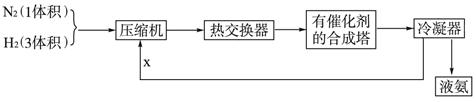
请回答下列问题:
(1)H2通常用碳氢化合物与水反应,写出有关的反应方程式 ,从冷凝器回流到压缩机中的X是 。
(2)比较工业上合成氨和SO2的催化氧化反应,其生产条件有哪些异同,并解释原因
。
(3)将N2、H2按体积比1∶3进入合成塔,从合成塔出来的混合气中,氨的体积分数为15%,则H2的体积分数为______________。
(4)NH3的用途之一是制造化肥,但在化肥的使用过程中要注意铵态氮肥不可以和草木灰混用,解释其原因 。
(5)NH3是一种重要的化工原料,除了制造化肥之外,再列举出两种NH3的用途
。 查看习题详情和答案>>