摘要:17.现有A.B.C.D.E.F六种短周期元素.它们的原子序数依次增大.A.D同主族.C与E同主族.D.E.F同周期.A.B的最外层电子数之和与C的最外层电子数相等. A能分别与B.C形成电子总数相等的分子.且A与C形成的化合物常温下为液态.A能分别与E.F形成电子总数相等的气体分子. 请回答下列问题(题中的字母只代表元素代号.与实际元素符号无关): (1) A-F六种元素原子.原子半径最大的是 . (2)A.C.D三种元素组成的一种常见化合物.是重要的工业产品.该化合物电子式为: . (3)B与F两种元素形成的一种化合物分子.各原子均达八电子结构.其中B显负价.F显正价.则该化合物水解的主要产物是: . (4)A.C.E三种元素形成的一种常见化合物.其浓溶液在加热条件下可与铜反应.该反应的化学方程式为: .
网址:http://m.1010jiajiao.com/timu3_id_41457[举报]
现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子.
请回答下列问题(题中的字母只代表元素代号,与实际元素符号无关):
(1)A~F六种元素原子,原子半径最大的是
(2)A、C、D三种元素组成的一种常见化合物,是重要的工业产品,该化合物电子式为: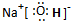
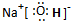 .
.
(3)B与F两种元素形成的一种化合物分子,各原子均达八电子结构,其中B显负价,F显正价,则该化合物水解的主要产物是:
(4)A、C、E三种元素形成的一种常见化合物,其浓溶液在加热条件下可与铜反应,该反应的化学方程式为
查看习题详情和答案>>
请回答下列问题(题中的字母只代表元素代号,与实际元素符号无关):
(1)A~F六种元素原子,原子半径最大的是
D
D
(填序号).(2)A、C、D三种元素组成的一种常见化合物,是重要的工业产品,该化合物电子式为:
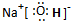
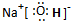
(3)B与F两种元素形成的一种化合物分子,各原子均达八电子结构,其中B显负价,F显正价,则该化合物水解的主要产物是:
HClO和NH3(NH3?H2O)
HClO和NH3(NH3?H2O)
.(4)A、C、E三种元素形成的一种常见化合物,其浓溶液在加热条件下可与铜反应,该反应的化学方程式为
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O
.
| ||
 现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.
现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.请回答下列问题(填空时用实际符号):
(1)C的元素符号是
N
N
;元素F在周期表中的位置第3周期第ⅦA族
第3周期第ⅦA族
.(2)B与D一般情况下可形成两种常见气态化合物,假若现在科学家制出另一种直线型气态化合物 B2D2分子,且各原子最外层都满足8电子结构,则B2D2电子式为
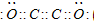
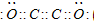
分子晶体
分子晶体
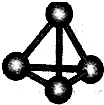
.(3)最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4分子.C4分子结构如图所示,已知断裂1molC-C吸收167kJ热量,生成1molC=C放出942kJ热量.根据以上信息和数据,下列说法正确的是
②④⑦
②④⑦
.①C4属于一种新型的化合物
②C4沸点比P4(白磷)低
③lmol C4气体转变为C2吸收882kJ热量
④C4与C2互为同素异形体
⑤C4稳定性比P4(白磷)差
⑥C4属于原子晶体
⑦C4和P4 (白磷)的晶体都属于分子晶体
⑧C4与C2互为同分异构体
(4)C与F两种元素形成一种化合物分子,各原子最外层达8电子结构,则该分子的结构式为
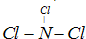
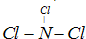
三角锥型
三角锥型
.(5)为了除去化合物乙(A2ED4)稀溶液中混有的A2ED3,常采用A2D2为氧化剂,发生反应的离子方程式为:
H2O2+H2SO3=2H++SO42-+H2O
H2O2+H2SO3=2H++SO42-+H2O
(6)E与F形成的化合物E2F2在橡胶工业上有重要用途,遇水易水解,其空间结构与A2D2极为相似.对此以下说法正确的是
acd
acd
.a.E2F2的结构式为:F-E-E-F
b.E2F2为含有极性键 和非极性键的非极性分子
c.E2Br2与E2F2结构相似,熔沸点:E2Br2>E2F2
d.E2F2与H2O反应的化学方程式可能为:2E2F2+2H2O=EO2↑+3E↓+4HF
(7)举出一种事实说明E与F的非金属性强弱(用化学方程式或用语言文字表达均可):
C12+H2S=S↓+2HCl
C12+H2S=S↓+2HCl
.现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大.室温下E元素的单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜;D元素原子核外M电子层与K电子层上的电子数相等;A可分别与B、F形成A2B,A2B2、AF等共价化合物;C可分别与B、F形成C2B、C2B2、CF等离子化合物.
请回答下列问题:
(1)以上六种元素中,金属性最强的是(填元素符号)
 .
.
(2)以上元素形成的简单离子中,核外电子数相等的是(填真实的离子符号)
(3)C2B2的电子式为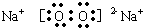
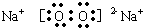 ,该物质中存在的化学键有
,该物质中存在的化学键有
(4)A2B与C2B2反应的化学方程式是
查看习题详情和答案>>
请回答下列问题:
(1)以上六种元素中,金属性最强的是(填元素符号)
Na
Na
,F原子的结构示意图为

(2)以上元素形成的简单离子中,核外电子数相等的是(填真实的离子符号)
O2-、Na+、Mg2+、Al3+
O2-、Na+、Mg2+、Al3+
.(3)C2B2的电子式为
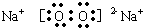
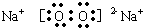
离子键、非极性键(或共价键)
离子键、非极性键(或共价键)
.(4)A2B与C2B2反应的化学方程式是
2H2O+2Na2O2=4NaOH+O2↑
2H2O+2Na2O2=4NaOH+O2↑
.现有A、B、C、D、E、F六种短周期元素,原子序数依次增大.已知A与D、C与E分别同主族,D、E、F同周期;A、B的最外层电子数之和与C的最外层电子数相等,A与C形成的化合物常温下均为液态,A分别与E、F形成的气体分子电子总数相等.
请回答下列问题:
(1)元素B在周期表中的位置是
 .
.
(2)A2C比A2E沸点高的原因是
(3)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为
(4)化合物B2A4和B2C4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染.1mol B2A4与B2C4完全反应生成两种气体时放出热量516.8kJ,则该反应的热化学方程式为
查看习题详情和答案>>
请回答下列问题:
(1)元素B在周期表中的位置是
第二周期第ⅤA族
第二周期第ⅤA族
,元素D的原子结构示意图为

(2)A2C比A2E沸点高的原因是
H2O分子间存在氢键而H2S分子间不能形成氢键
H2O分子间存在氢键而H2S分子间不能形成氢键
.(3)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为
O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
,负极的电极反应式为2H2+4OH--4e-═4H2O
2H2+4OH--4e-═4H2O
,该电池在放电过程中,电解质溶液的pH将减小
减小
(填“增大”、“减小”或“不变”).(4)化合物B2A4和B2C4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染.1mol B2A4与B2C4完全反应生成两种气体时放出热量516.8kJ,则该反应的热化学方程式为
2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H=-1033.6kJ?mol-1
2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H=-1033.6kJ?mol-1
.现有A、B、C、D、E、F六种短周期元素.它们的原子序数依次增大,A元素的某核素的原子核内没有中子,A与C、B与F同主族,C、D、F同周期,C、D、F的最高价氧化物的水化屋之间可以两两相互反应,D、E原子的最外层电子数之和等于F原子的最外层电子数,D的单质参与的反应可以用来野外焊接钢轨,E为传统无机非金属材料的重要组成元素,请回答下列问题:
(1)F的元素名称
(2)A、B、C、D、E五种元素的原子半径由大到小的顺序为(填元素符号)
(3)写出D单质参与的焊接钢轨的主要反应的化学方程式
(4)A元素分别与B、E、F元素构成的三种二元化合物的热稳定性由强到弱的顺序是(用化学式表示)
(5)用电子式描述C与F构成的化合物形成过程
 .
.
(6)试用事实说明B与F两种元素的非金属性强弱
查看习题详情和答案>>
(1)F的元素名称
氯
氯
,D在元素周期表中的位置是第三周期第IIA族
第三周期第IIA族
.(2)A、B、C、D、E五种元素的原子半径由大到小的顺序为(填元素符号)
Na>Al>Si>F>H
Na>Al>Si>F>H
.(3)写出D单质参与的焊接钢轨的主要反应的化学方程式
2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
.分别写出D、E的氧化物与C的最高价氧化物的水花物反应的化学方程式
| ||
Al2O3+2NaOH═2NaAlO2+H2O
Al2O3+2NaOH═2NaAlO2+H2O
,2NaOH+SiO2═Na2SiO3+H2O
2NaOH+SiO2═Na2SiO3+H2O
.(4)A元素分别与B、E、F元素构成的三种二元化合物的热稳定性由强到弱的顺序是(用化学式表示)
HF>HCl>SiH4
HF>HCl>SiH4
.(5)用电子式描述C与F构成的化合物形成过程


(6)试用事实说明B与F两种元素的非金属性强弱
在黑暗处氟气能和氢气发生反应且产生爆炸,光照条件下,氯气和氢气反应生成氯化氢
在黑暗处氟气能和氢气发生反应且产生爆炸,光照条件下,氯气和氢气反应生成氯化氢
.