网址:http://m.1010jiajiao.com/timu3_id_410973[举报]
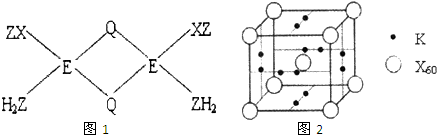 已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满.请回答下列问题:
已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满.请回答下列问题:(1)X、Y、Z第一电离能由小到大的顺序为
(2)E元素基态原子的电子排布式为
(3)X和Z形成有毒气体XZ,实验室常用EQ溶液吸收并定量测定XZ的含量.反应时,XZ与EQ形成配合物的分子中原子问成键关系如图1所示:E+和Q之间的化学键类型是
(4)XZ2分子中含有
(5)Z氢化物的沸点比Q氢化物的沸点高,理由是
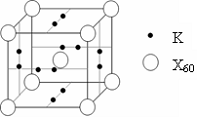
(6)X元素可形成X60.单质,它与金属钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示(白球位于立方体的体心和顶点,小黑球位于立方体的面上),该化合物中X60与钾原子个数比为
已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是p能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E的单质是常温下唯一呈液态的非金属。请回答下列问题:
(1)X、Y、Z第一电离能由小到大的顺序为 < < (填元素符号)。
(2)E元素基态原子的电子排布式为 。
(3)XZ2分子中含有 个π键。
|
(5)X元素可形成X60单质,它与金属钾掺杂在
一起制造了一种富勒烯化合物,其晶胞如图
所示(白球位于立方体的体心和顶点,小黑
球位于立方体的面上),该化合物中X60与钾
原子个数比为 。
查看习题详情和答案>>已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是p能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E的单质是常温下唯一呈液态的非金属.请回答下列问题:
(1)X、Y、Z第一电离能由小到大的顺序为 < < (填元素符号).
(2)E元素基态原子的电子排布式为 .
(3)XZ2分子中含有 个π键.
(4)Z氢化物的沸点比Q氢化物的沸点高,理由是 .
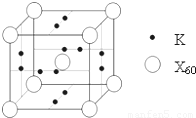
(5)X元素可形成X60单质,它与金属钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示(白球位于立方体的体心和顶点,小黑球位于立方体的面上),该化合物中X60与钾原子个数比为 .
 查看习题详情和答案>>
查看习题详情和答案>>
原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E元素原子序数为29。请用元素符号或化学式回答下列问题:
(1)X、Y、Z的第一电离能由小到大的顺序为 ;
(2)已知YZ2+与XQ2互为等电子体,则1 mol YZ2+中含有π键数目为_______;
(3)Z的气态氢化物沸点比Q的气态氢化物高的多,其原因是 ;
(4)X、Z与氢元素可形成化合物H2X2Z4,常用作工业除锈剂。H2X2Z4分子中X的杂化方式为 ;
(5)E原子的核外电子排布式为 ;E有可变价态,它的某价态的离子与Z的阴离子形成晶体的晶胞如图所示,该晶体的化学式为 。

查看习题详情和答案>>
(1)X、Y、Z的第一电离能由小到大的顺序为 ;
(2)已知YZ2+与XQ2互为等电子体,则1 mol YZ2+中含有π键数目为_______;
(3)Z的气态氢化物沸点比Q的气态氢化物高的多,其原因是 ;
(4)X、Z与氢元素可形成化合物H2X2Z4,常用作工业除锈剂。H2X2Z4分子中X的杂化方式为 ;
(5)E原子的核外电子排布式为 ;E有可变价态,它的某价态的离子与Z的阴离子形成晶体的晶胞如图所示,该晶体的化学式为 。