摘要:有三种金属A.B.C.实验证明.B能从C的硝酸盐溶液中置换出C.B 不能从A的硝酸盐溶液中置换出A.三种金属活动性由强到弱的顺序是( ) A.A>C>B B.B>A>C C.C>A>B D.A>B>C
网址:http://m.1010jiajiao.com/timu3_id_3989179[举报]
 A、B、C为三种常见的单质,其中A、C为气体,B为常见金属.A溶于水所得的溶液可使石蕊试液先变红后退色.F的水溶液为浅绿色溶液,它们的关系如图:
A、B、C为三种常见的单质,其中A、C为气体,B为常见金属.A溶于水所得的溶液可使石蕊试液先变红后退色.F的水溶液为浅绿色溶液,它们的关系如图:
(1)写出A、B、D的化学式:
A.
Cl2
Cl2
B.Fe
Fe
D.FeCl3
FeCl3
(2)写出反应①②的离子方程式
①
Fe+2H+═Fe2++H2↑
Fe+2H+═Fe2++H2↑
②
2Fe2++Cl2═2Fe3++2Cl-
2Fe2++Cl2═2Fe3++2Cl-
(3)检验D的水溶液中的阳离子的方法是:
取少量溶液于试管中,滴加两滴KSCN溶液,观察溶液是否变红色
取少量溶液于试管中,滴加两滴KSCN溶液,观察溶液是否变红色
.将D溶液逐滴加入的沸水中会产生一种红褐色的澄清液体.有同学认为该液体中的分散质粒子直径应该在1nm~100nm之间,验证这一想法的简单方法是:是否有丁达尔现象
是否有丁达尔现象
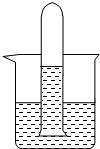
(4)如图某同学将A的饱和溶液装满大试管倒置于烧杯中,光照一段时间后,发现试管底部有无色的气体产生,溶液的颜色也变成无色,请你帮他对产生的气体进行探究:
a.你预测气体可能是
O2
O2
、或H2
或H2
b.针对你的预测写出验证实验方案:
在水下堵住试管口,取出正放,用燃着的木条放在试管口,如果气体燃烧说明是H2;如果木条燃烧更旺说明是O2
在水下堵住试管口,取出正放,用燃着的木条放在试管口,如果气体燃烧说明是H2;如果木条燃烧更旺说明是O2
.A、B、C、为三种常见的单质,其中A、C为气体,B为常见金属.A溶于水可使石蕊试液先变红后褪色.F的水溶液为浅绿色溶液,它们的关系如图1:
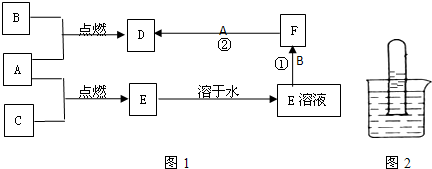
(1)写出A、B、D的化学式:A.
(2)写出反应①②的离子方程式:①
(3)A溶于水使石蕊试液先变红后褪色的原因是:
(4)检验D的水溶液中的阳离子的方法是(指出药品、试剂、步骤和现象):
(5)某同学将A的饱和溶液装满大试管倒置在烧杯中如图2,光照一段时间后,发现试管底部有无色的气体产生,溶液的颜色也变成无色,请你帮他对产生的气体进行探究:
①你预测气体可能是
②针对你的预测写出验证实验方案(步骤和现象):
查看习题详情和答案>>

(1)写出A、B、D的化学式:A.
Cl2
Cl2
B.Fe
Fe
C.FeCl3
FeCl3
(2)写出反应①②的离子方程式:①
Fe+2H+=Fe2++H2↑
Fe+2H+=Fe2++H2↑
;②2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
.(3)A溶于水使石蕊试液先变红后褪色的原因是:
因Cl2+H2O=HCl+HClO,HCl使石蕊试液变红,HClO具有漂白性
因Cl2+H2O=HCl+HClO,HCl使石蕊试液变红,HClO具有漂白性
.(4)检验D的水溶液中的阳离子的方法是(指出药品、试剂、步骤和现象):
取少量溶液于试管中,滴加两次KSCN溶液,溶液变红
取少量溶液于试管中,滴加两次KSCN溶液,溶液变红
.将D溶液逐滴加入的沸水中会产生一种红褐色的液体.你认为该液体中的分散质粒子直径在1nm-100nm
1nm-100nm
之间,验证的简单方法是:是否有丁达尔效应
是否有丁达尔效应
.(5)某同学将A的饱和溶液装满大试管倒置在烧杯中如图2,光照一段时间后,发现试管底部有无色的气体产生,溶液的颜色也变成无色,请你帮他对产生的气体进行探究:
①你预测气体可能是
O2或H2
O2或H2
②针对你的预测写出验证实验方案(步骤和现象):
在水下堵住试管口,取出正放,用燃着的木条放在试管口,如果气体燃烧说明是H2,如果木条燃烧更狂说明是O2
在水下堵住试管口,取出正放,用燃着的木条放在试管口,如果气体燃烧说明是H2,如果木条燃烧更狂说明是O2
. A.已知A、B、C、D、E是短周期中的五种元素,它们的原子序数依次增大.A和B可形成常见化合物BA4,一个BA4分子中电子总数为10;C原子的最外层电子数是核外电子总数的
A.已知A、B、C、D、E是短周期中的五种元素,它们的原子序数依次增大.A和B可形成常见化合物BA4,一个BA4分子中电子总数为10;C原子的最外层电子数是核外电子总数的| 3 |
| 4 |
(1)D与E两元素相比较,非金属性较强的是
氯
氯
(填元素名称),请你自选试剂设计实验验证该结论(说明试剂、简单操作、实验现象)将Cl2通入Na2S溶液(或氢硫酸)中,有浅黄色沉淀生成,说明Cl的非金属性比S强
将Cl2通入Na2S溶液(或氢硫酸)中,有浅黄色沉淀生成,说明Cl的非金属性比S强
;(2)A、C、D间可形成甲、乙两种微粒,它们均为负一价双原子阴离子且甲有18个电子,乙有l0个电子,则甲与乙反应的离子方程式为
HS-+OH-═S2-+H2O
HS-+OH-═S2-+H2O
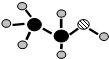
;(3)由A、B、C三种元素组成的化合物的球棍结构如图:,试写出利用植物秸秆生产这种物质的化学方程式
(C6H10O5)n+nH2O
nC6H12O6
| 催化剂 |
| △ |
(C6H10O5)n+nH2O
nC6H12O6
、| 催化剂 |
| △ |
C6H12O6
2CH3CH2OH+2CO2↑
| 一定条件 |
C6H12O6
2CH3CH2OH+2CO2↑
.| 一定条件 |
短周期元素A、B、C、D原子序数依次增大,且只有C为金属元素.A、C位于同一主族,B的最外层电子数为次外层的3倍,B、C的最外层电子灵敏之和与D的最外层电子数相等.请回答下列问题:
(1)D的最高价氧化物对应水化物名称为
(2)C2B2的电子式为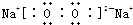
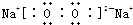 ,其中含有的化学键类型为
,其中含有的化学键类型为
(3)由上述四种元素中的三种组成某种盐,水溶液显碱性,是家用消毒剂的主要成分.将该盐溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应离子方程式为
(4)用石墨电极电解CD的饱和溶液,反应的离子方程式为
若反应后溶液的体积为200mL,测得pH为13,则阳极得到的气体质量为
(5)实验室欲检验CD溶液中所含的D-,操作方法和现象为
查看习题详情和答案>>
(1)D的最高价氧化物对应水化物名称为
高氯酸
高氯酸
.(2)C2B2的电子式为
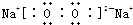
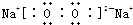
离子键、非极性键
离子键、非极性键
.(3)由上述四种元素中的三种组成某种盐,水溶液显碱性,是家用消毒剂的主要成分.将该盐溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应离子方程式为
2I-+ClO-+H2O=I2+Cl-+2OH-
2I-+ClO-+H2O=I2+Cl-+2OH-
(4)用石墨电极电解CD的饱和溶液,反应的离子方程式为
2NaCl+2H2O
Cl2↑+H2↑+2NaOH
| ||
2NaCl+2H2O
Cl2↑+H2↑+2NaOH
,
| ||
若反应后溶液的体积为200mL,测得pH为13,则阳极得到的气体质量为
0.71g
0.71g
,外电路中通过的物质的量为0.02mol
0.02mol
(5)实验室欲检验CD溶液中所含的D-,操作方法和现象为
取少许试液,向其中加入硝酸酸化的硝酸银溶液,若有白色沉淀产生,则证明有Cl-
取少许试液,向其中加入硝酸酸化的硝酸银溶液,若有白色沉淀产生,则证明有Cl-
.X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是生活中最常用的金属,它与L可以形成三种化合物.
请回答下列问题:
(1)Y在元素周期表中的位置为
(2)硒(se)是人体必需的微量元素,与L同一主族,该族2~5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1mol硒化氢反应热的是
a.+99.7mol?L-1 b.+29.7mol?L-1 c.-20.6mol?L-1 d.-241.8kJ?mol-1
(3)已知(YZ)2分子所有的原子都满足8电子,请写出其结构式
(4)L、X两元素按原子数目比l:1和1:2形成分子A和B.
①用电子式表示B的形成过程
 .
.
②M在高温下可以与B反应,写出该反应的化学方程式
某同学将反应得到的黑色粉末全部溶于足量的硫酸溶液中,发现有少量的气泡产生,溶液呈棕黄色,该同学判断溶液中一定同时存在两种M的金属阳离子.请你选择合适的试剂与合理的步骤证明该同学的推断
③若该同学将上述棕黄色溶液1mL加入到2mL A的浓溶液中,预计会看到的实验现象是
查看习题详情和答案>>
请回答下列问题:
(1)Y在元素周期表中的位置为
第二周期,第ⅣA族
第二周期,第ⅣA族
.(2)硒(se)是人体必需的微量元素,与L同一主族,该族2~5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1mol硒化氢反应热的是
b
b
(填字母代号).a.+99.7mol?L-1 b.+29.7mol?L-1 c.-20.6mol?L-1 d.-241.8kJ?mol-1
(3)已知(YZ)2分子所有的原子都满足8电子,请写出其结构式
N≡C-C≡N
N≡C-C≡N
;(YZ)2可以与X2化合生成XYZ,其水溶液是一种酸,某浓度该酸的钾盐(KYZ)溶液能使酚酞溶液显红色,请用离子方程式表示原因CN-+H2O HCN+OH-
HCN+OH-
 HCN+OH-
HCN+OH-CN-+H2O HCN+OH-
HCN+OH-
. HCN+OH-
HCN+OH-(4)L、X两元素按原子数目比l:1和1:2形成分子A和B.
①用电子式表示B的形成过程


②M在高温下可以与B反应,写出该反应的化学方程式
3Fe+4H2O
Fe3O4+4H2↑
| ||
3Fe+4H2O
Fe3O4+4H2↑
.
| ||
某同学将反应得到的黑色粉末全部溶于足量的硫酸溶液中,发现有少量的气泡产生,溶液呈棕黄色,该同学判断溶液中一定同时存在两种M的金属阳离子.请你选择合适的试剂与合理的步骤证明该同学的推断
取溶液少许,滴加KSCN溶液,溶液变红色,证明有Fe3+,另取溶液少许,加入KMnO4酸性溶液,紫色褪去,证明有Fe2+.
取溶液少许,滴加KSCN溶液,溶液变红色,证明有Fe3+,另取溶液少许,加入KMnO4酸性溶液,紫色褪去,证明有Fe2+.
.③若该同学将上述棕黄色溶液1mL加入到2mL A的浓溶液中,预计会看到的实验现象是
有大量气泡出现
有大量气泡出现
.