网址:http://m.1010jiajiao.com/timu3_id_3987136[举报]
有五种原子序数在36以内的元素A、B、C、D、E,它们的原子序数依次增大,A原子的最外层电子数等于其电子层数,A、B、C原子核外电子层数之和是6,C原子的电子数为A和B两元素原子电子总数的两倍;D和C的最高价氧化物对应水化物的酸性前者强于后者;E可和C形成原子个数比为1:1和1:2的两种化合物,其中一种物质是工业合成硫酸的常见原料,这两种化合物的摩尔质量相差32。试回答下列问题:
(1)E在周期表中的位置是 ,基态B原子的价电子排布式 。
(2)写出CD2的电子式 ,根据价层电子对互斥(VSEPR)理论推测,CD2分子的空间构型为 ,该分子是 分子(填“极性”或“非极性”)。
(3)通常情况下,AB3为无色有刺激性气味的液体,沸点303.8K,熔点193K。AB3固态时的晶体类型为 ;其水溶液有弱酸性,它的电离方程式为 。
(4)下列性质可作为比较C、D两元素非金属性强弱依据的是 (填编号)。
①C、D的最高价氧化物对应水化物的酸性强弱
②C、D的气态氢化物的水溶液的酸性强弱
③C、D的气态氢化物的稳定性强弱
④C、D的简单离子是否易被E3+氧化
⑤相同条件下,C、D的钠盐溶液的碱性强弱
查看习题详情和答案>>
(1)写出它们的元素名称:A___________,B___________,C___________,D________;
(2)A、D两元素最高价氧化物对应水化物的化学式分别为____________,____________;
(3)过量AB2与C的最高价氧化物对应的水化物反应的化学方程式为_________________;
(4)C的氧化物的水化物与D的最高价氧化物对应的水化物反应的离子方程式为_______________________。
查看习题详情和答案>>(15分)有机物A为芳香烃,质谱分析表明其相对分子质量为92,某课题小组以A为起始原料可以合成酯类香料H和高分子化合物I,其相关反应如下图所示:
已知以下信息:
①碳烯(:CH2)又称卡宾,它十分活跃,很容易用它的两个未成对电子插在烷烃分子的C-H键之间使碳链增长。
②通常在同一个碳原子连有两个羟基不稳定,易脱水形成羰基。
回答下列问题:
(1)A的化学名称为 。
(2)由B生成C的化学方程式为 ,该反应类型为 。 (3)G的结构简式为 。
(4)请写出由F生成I的化学方程式 。
(5)写出G到H的反应方程式 。
(6)H的所有同分异构体中,满足下列条件的共有 种;
①含有苯环 ②苯环上只有一个取代基 ③属于酯类
其中核磁共振氢谱有五种不同化学环境的氢,且峰面积比为1:1:2:2:6的是 (写结构简式)。
(1)盐G的晶体内所含化学键类型是
(2)将元素A与Z形成的化合物与过量NaOH反应生成物质F,F的水溶液在空气中长期放置发生反应,生成M和N两种物质,M与过氧化钠的结构和性质相似,则N的电子式为
(3)有两种化合物同时含有上述元素中的四种相同元素,这两种化合物的水溶液混合后迅速反应,生成物中仍有一种含上述四种元素,写出该产物的化学式:
(4)将由BX和BX2组成的混合气体通入下图所示的装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强(在通入混合气体之前,已通入一段时间的N2).
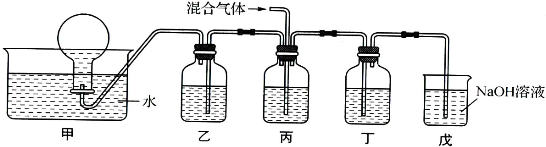
已知:①浓硝酸能将BX氧化成BX2,而稀硝酸不能氧化BX;
②NaOH溶液与BX2能发生反应生成两种盐和水,NaOH溶液与BX不反应.
a.装置乙、丙、丁中盛放的药品依次是
b.能够说明实验已成功的现象是
(1)B、C两元素按原子个数1:1组成的化合物F中的阴阳离子比为
(2)试比较D、E两元素的最高价氧化物对应水化物的酸性强弱(填写化学式):
(3)将E单质通入A、B、C三种元素组成的化合物的水溶液中,写出反应的离子方程式:
(4)写出两种均含A、B、C、D四种元素的化合物在溶液中相互反应,且生成气体的化学方程式:
(5)D的氢化物分子中,D原子的杂化方式是