摘要:14.1905年爱因斯坦在德国的上发表了一篇关于布朗运动的重要论文.在论文中.爱因斯坦把显微镜下可见粒子的运动看作是显微镜下看不到的液体分子运动的表征.这种方法在科学上叫做“转换法 .下面给出的四个研究实例中.采用“转换法 的是 ( ) A.伽利略用理想斜面实验得出力不是维持物体运动的原因 B.爱因斯坦在普朗克量子学说的启发下提出光子说 C.欧姆在研究电流与电压.电阻关系时.先使电阻不变去研究电流与电压的关系,然后再让电压不变去研究电流与电阻的关系 D.奥斯特通过放在通电直导线下方的小磁针发生偏转得出通电导线的周围存在磁场
网址:http://m.1010jiajiao.com/timu3_id_391045[举报]
[选做题](1)人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深、由低级到高级的认识过程.目前中学课本中的酸碱理论是1889年阿仑尼乌斯(Arrhenius)提出的电离理论.
①1905年富兰克林(FranKlin)深入研究了水和液氨的相似性,把阿仑尼乌斯以水为溶剂的个别现象,推广到任何溶剂,提出了酸碱溶剂理论.溶剂理论认为:凡能电离而产生溶剂正离子的物质为酸,凡能电离而产生溶剂负离子的物质为碱.试写出液氨自身电离的方程式:
②1923年丹麦化学家布朗斯特(Bronsted)和英国化学家劳莱(Lowey)提出质子理论.凡是能够释放质子(氢离子)任何含氢原子的分子或离子都是酸;凡是能够与质子(氢离子)结合的分子或离子都是碱.
按质子理论:下列粒子在水溶液既可以看作酸又可看碱的是
A、H2O B、NH4+ C、OH- D、HCO3- E、CH3COO- F、Cl-
③1923年路易斯(Lewis)提出广义的酸碱概念.凡是能给出电子对而形成化学键的物质都是碱;凡是能够和电子对结合的物质都是酸.
酸(电子对接受体)+碱(电子对给予体)→反应产物,如:H++OH-→H2O.
试指出下列两个反应中的酸或碱:
(Ⅰ)H3BO3+H2O H++B(OH)4-,该反应中的碱是
H++B(OH)4-,该反应中的碱是
(Ⅱ)NaH+H2O═NaOH+H2↑,该反应中的酸是
(2)已知A元素原子的K、L层电子数之和比M、L层电子数之和多一个电子;B元素原子核外电子占有9个轨道,且有1个未成对电子;C元素原子核外3p亚层中3个轨道还需5个电子才能达到全充满.D元素只有两个电子层,且最高化合价与最低化合价的代数和为零;E原子半径最小;F元素最外层电子排布为nSnnPn+1.按要求填写
①B的电子排布式是:
②D元素单质的晶体类型是
③E和F形成的化合物空间构型为
查看习题详情和答案>>
①1905年富兰克林(FranKlin)深入研究了水和液氨的相似性,把阿仑尼乌斯以水为溶剂的个别现象,推广到任何溶剂,提出了酸碱溶剂理论.溶剂理论认为:凡能电离而产生溶剂正离子的物质为酸,凡能电离而产生溶剂负离子的物质为碱.试写出液氨自身电离的方程式:
2NH3=NH4++NH2-
2NH3=NH4++NH2-
.②1923年丹麦化学家布朗斯特(Bronsted)和英国化学家劳莱(Lowey)提出质子理论.凡是能够释放质子(氢离子)任何含氢原子的分子或离子都是酸;凡是能够与质子(氢离子)结合的分子或离子都是碱.
按质子理论:下列粒子在水溶液既可以看作酸又可看碱的是
AD
AD
.A、H2O B、NH4+ C、OH- D、HCO3- E、CH3COO- F、Cl-
③1923年路易斯(Lewis)提出广义的酸碱概念.凡是能给出电子对而形成化学键的物质都是碱;凡是能够和电子对结合的物质都是酸.
酸(电子对接受体)+碱(电子对给予体)→反应产物,如:H++OH-→H2O.
试指出下列两个反应中的酸或碱:
(Ⅰ)H3BO3+H2O
 H++B(OH)4-,该反应中的碱是
H++B(OH)4-,该反应中的碱是H2O
H2O
(填H3BO3或H2O);(Ⅱ)NaH+H2O═NaOH+H2↑,该反应中的酸是
H2O
H2O
(填NaH 或H2O).(2)已知A元素原子的K、L层电子数之和比M、L层电子数之和多一个电子;B元素原子核外电子占有9个轨道,且有1个未成对电子;C元素原子核外3p亚层中3个轨道还需5个电子才能达到全充满.D元素只有两个电子层,且最高化合价与最低化合价的代数和为零;E原子半径最小;F元素最外层电子排布为nSnnPn+1.按要求填写
①B的电子排布式是:
1s22s22p63s23p5
1s22s22p63s23p5
,A、B两元素形成的化合物的晶体类型是离子晶体
离子晶体
.②D元素单质的晶体类型是
原子晶体
原子晶体
,C单质的制备方法是:电解法
电解法
.③E和F形成的化合物空间构型为
三角锥型
三角锥型
,该物质比D与E形成的化合物更容易液化的原因是E和F形成的化合物分子间能形成氢键
E和F形成的化合物分子间能形成氢键
.(2010?临沂一模)氨气在农业和国防工业都有很重要的作用,历史上诺贝尔化学奖曾经有3次颁给研究氮气与氢气合成氨的化学家.
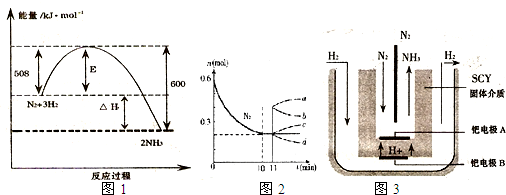
(1)如图1表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答:
①写出氮气与氢气合成氨的热化学反应方程式:
②对于合成氨的反应下列说法正确的是
A、该反应在任意条件下都可以自发进行
B、加入催化剂,能使该反应的E和△H都减小
C、若反应在298K、398K时的化学平衡常数分别为K1、K2,K1>K2
D、该反应属于人工固氮
(2)现在普遍应用的工业合成氮的方法N2+3H2?2NH3,是哈伯于1905年发明的,但此法达到平衡时反应物的转化率不高.
①能使该反应的反应速率增大,且平衡向正方向移动的措施是
A、使用的更高效催化剂
B、升高温度
C、及时分离出氨气
D、冲入氮气,增大氮气的浓度(保持容器体积不变)
②若在某温度下、2L的密闭容器中发生N2+3H2?2NH3的反应,如图2表示N2的物质的量随时间的变化曲线.用H2表示0~10min内该反应的平速率v(H2)=
A、a B、b C、c D、d
(3)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下吧氢气和用氦气稀释的氮气,分别通入一个加热到500℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质理用吸附在它内外表面上的金属但多晶薄膜像电噪,实现了常压、570℃条件下高转化率的电解法合成氮(装置如图3).
请回答:铠电极是电解池的
查看习题详情和答案>>

(1)如图1表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答:
①写出氮气与氢气合成氨的热化学反应方程式:
N2(g)+3H2(g)
2NH3(g)△H═-92kJ/mol
| ||
N2(g)+3H2(g)
2NH3(g)△H═-92kJ/mol
| ||
②对于合成氨的反应下列说法正确的是
CD
CD
(填编号)A、该反应在任意条件下都可以自发进行
B、加入催化剂,能使该反应的E和△H都减小
C、若反应在298K、398K时的化学平衡常数分别为K1、K2,K1>K2
D、该反应属于人工固氮
(2)现在普遍应用的工业合成氮的方法N2+3H2?2NH3,是哈伯于1905年发明的,但此法达到平衡时反应物的转化率不高.
①能使该反应的反应速率增大,且平衡向正方向移动的措施是
D
D
(填编号)A、使用的更高效催化剂
B、升高温度
C、及时分离出氨气
D、冲入氮气,增大氮气的浓度(保持容器体积不变)
②若在某温度下、2L的密闭容器中发生N2+3H2?2NH3的反应,如图2表示N2的物质的量随时间的变化曲线.用H2表示0~10min内该反应的平速率v(H2)=
0.06mol/(L?min)
0.06mol/(L?min)
.从1min起,压缩容器的体积为1L,则n(N2)的变化曲线为D
D
(填编号)A、a B、b C、c D、d
(3)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下吧氢气和用氦气稀释的氮气,分别通入一个加热到500℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质理用吸附在它内外表面上的金属但多晶薄膜像电噪,实现了常压、570℃条件下高转化率的电解法合成氮(装置如图3).
请回答:铠电极是电解池的
阴
阴
极(填“阳“或“阴“),该极上的电极反应式是N2+6e-+6H+=2NH3
N2+6e-+6H+=2NH3
.氨是最重要的氮肥,是产量最大的化工产品之一.课本里介绍的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的,其合成原理为:N2(g)+3H2(g)?2NH3(g);△H<0他因此获得了1918年诺贝尔化学奖.工业上合成氨的部分工艺流程如图1: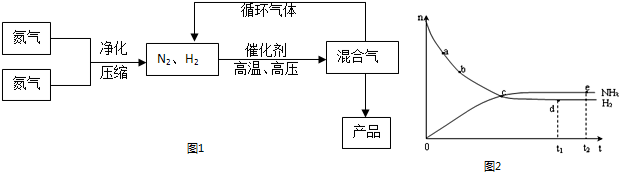
反应体系中各组分的部分性质见下表:
(1)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程.即反应后通过把混合气体的温度降低到
(2)工业上采取用上述(1)操作的目的:
(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(4)合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),在673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图2所示.下列叙述正确的是
A.点a的正反应速率比点b的大
B.点 c处反应达到平衡
C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比图2中d点的值大.
查看习题详情和答案>>

反应体系中各组分的部分性质见下表:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
-33.42
-33.42
℃使混合气体分离出来产品;继续循环的气体是N2、H2
N2、H2
.(2)工业上采取用上述(1)操作的目的:
及时分离出氨气,平衡正向移动,提高氨气的产率,且循环利用氮气和氢气,提高氮气和氢气的转化率
及时分离出氨气,平衡正向移动,提高氨气的产率,且循环利用氮气和氢气,提高氮气和氢气的转化率
.(3)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
N2(g)+3H2(g)?2NH3(g)△H=-92kJ?mol-1
N2(g)+3H2(g)?2NH3(g)△H=-92kJ?mol-1
.(4)合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),在673K,30MPa下n(NH3)和n(H2)随时间变化的关系如图2所示.下列叙述正确的是
AD
AD
A.点a的正反应速率比点b的大
B.点 c处反应达到平衡
C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比图2中d点的值大.