网址:http://m.1010jiajiao.com/timu3_id_378816[举报]
| 元素 | 原子结构或性质 | ||
| A | 原子最外层电子数是内层电子总数的
| ||
| B | 形成化合物种类最多的元素,其单质为固体 | ||
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 | ||
| D | 地壳中含量最多的元素 | ||
| E | 与D同主族 | ||
| F | 与E同周期,且最外层电子数等于电子层数 |
(1)写出A与E形成的化合物的电子式


(2)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是
| ||
| ||
(3)F的盐酸盐水溶液呈酸性,原因是
| ||
| ||
(4)化合物M是一种元素C的+6含氧酸钾盐,常用作净水剂与消毒剂.由元素C稳定的氢氧化物与次氯酸钾、氢氧化钾溶液反应制取化合物M,则制备M的离子反应方程式是
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A是原子半径最小的元素;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;E有“生物金属”之称,E4+和氩原子的核外电子排布相同。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1 : 1的化合物N是常见的有机溶剂。
请回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A2D2分子的电子式为______,E的基态原子的外围电子排布式为______。
(2)B、C、D三种元素的第一电离能由小到大的顺序为______。
(3)单质B与C的最高价氧化物的水化物的浓溶液微热反应,其化学方程式为______
(4)下列叙述正确的是______(填序号)。
a. M是极性分子,N是非极性分子 b. M和BD2分子中的中心原子均采用sp2杂化
c. N分子中含有6个σ键和1个π键 d. BD2晶体的熔点、沸点都比二氧化硅晶体的低
(5) 已知:①E的一种氧化物Q,其晶胞结构如图所示

①Q(s)+2Cl2(g)=ECl4(l)+D2(g) △H=+140kJ/mol
②2B(s)+D2(g)=2BD(g) △H=-221kJ/mol
写出物质Q和焦炭、氯气反应生成液态ECI4和BD气体的热化学方程式:__________________________
(6)在0.5 L的密闭容器中,一定量的C2和A2进行如下化学反应:C2(g) +3 A2(g)=2CA3(g) △H <0,其化学平衡常数K与温度t的关系如下表。请回答下列问题。

①试比较K1,K2的大小,K1________K2(填写“ >”、“=”或“<”)。
②在400℃时,当测得CA3和C2、A2的物质的量分别为3mol和1 mol、2 mol时,则该反应的 V(C2)正_________(C2)逆(填写“>”、“=”或“<”)。
查看习题详情和答案>>
请回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A2D2分子的电子式为______,E的基态原子的外围电子排布式为______。
(2)B、C、D三种元素的第一电离能由小到大的顺序为______。
(3)单质B与C的最高价氧化物的水化物的浓溶液微热反应,其化学方程式为______
(4)下列叙述正确的是______(填序号)。
a. M是极性分子,N是非极性分子 b. M和BD2分子中的中心原子均采用sp2杂化
c. N分子中含有6个σ键和1个π键 d. BD2晶体的熔点、沸点都比二氧化硅晶体的低
(5) 已知:①E的一种氧化物Q,其晶胞结构如图所示
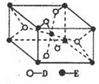
①Q(s)+2Cl2(g)=ECl4(l)+D2(g)△H=+140kJ/mol
②2B(s)+D2(g)=2BD(g) △H=-221kJ/mol
写出物质Q和焦炭、氯气反应生成液态ECI4和BD气体的热化学方程式:__________________________
(6)在0.5 L的密闭容器中,一定量的C2和A2进行如下化学反应:C2(g) +3 A2(g)=2CA3(g) △H<0,其化学平衡常数K与温度t的关系如下表。请回答下列问题。

①试比较K1,K2的大小,K1________K2(填写“ >”、“=”或“<”)。
②在400℃时,当测得CA3和C2、A2的物质的量分别为3mol和1 mol、2 mol时,则该反应的 V(C2)正_________(C2)逆(填写“>”、“=”或“<”)。
I.下图为向25mL0.1mol/L NaOH溶液中逐滴滴加0.2moL/L CH3COOH溶液过程中溶液pH的变化曲线
 |
请回答:
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确? (选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间内还是BD区间内? (若正确,此问不答)
(2)关于该滴定实验,从下列选项中选出最恰当的一项


(3)在AB区间内,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)的大小关系是
A.c(OH-)一定大于c(CH3COO-)
B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-)
D.c(OH-)可能大于、小于或等于C(CH3COO-)
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH) 2c(Na+)。(填“>”、“<”或“=”)
Ⅱ.在温度t℃时,某NaOH稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:
(5)该温度下水的离子积常数Kw=
(6)该NaOH稀溶液中NaOH物质的量浓度的精确值是 mol/L(用含字母的表达式表示)
(7)在该温度下(t℃),将100mL 0.1mol/L的稀H2SO4溶液与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=
查看习题详情和答案>>(1)写出A、E两元素形成的原子个数比为1:1的化合物的电子式
(2)向氯化亚铁溶液滴加过量的E的最高价氧化物对应水化物的溶液,现象是
(3)Y溶液显碱性的原因是(用一个离子方程式表示)
(4)检验汽车尾气中含有的化合物BD的方法是:向酸性PdCl2溶液中通A汽车尾气,若生成黑色沉淀(Pd),证明汽车尾气中含有BD.写出反应的离子方程式
(5)下列有关物质性质的比较中.不正确的是
a.热稳定性:H2S>SiH4 b.离子半径:Na+>S2-
c.第一电离能N>O d.元素电负性:C>H
(6)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
②CH3OH(g)+
| 3 | 2 |
由上述方程式可知.CH3OH的燃烧热