网址:http://m.1010jiajiao.com/timu3_id_377761[举报]
铝是地壳中含量最多的金属元素,1854年法国化学家德维尔用金属钠还原氯化钠和氯化铝的复盐,获得了铝单质。1886年,美国人豪尔和法国人海郎特,分别独立地电解熔融的氧化铝和冰晶石的混合物,制得了金属铝,奠定了今天大规模生产铝的基础。
工业生产金属铝的原料是铝土矿(主要成分为Al2O3,另含有Fe2O3和SiO2),工业中得到较纯氧化铝的过程如下图所示:

试回答下列问题:
(1)操作Ⅰ是一种重要的混合物分离方法,实验室进行该项操作用到的玻璃仪器有烧杯、________、________。
(2)经分析不溶物A的主要成分为________。
(3)工业上电解冶炼铝的化学方程式为________________,若电路中通过1 mol电子,可以得到铝________g。
(4)为了提高综合经济效益,实际工业生产中常将上述反应中的相关物质循环利用。其部分转化关系如下图所示:

①上述转化中未涉及四种基本反应类型中的________反应;
②写出过程③的化学方程式:____________。
(5)科学研究表明,人体过量吸入铝元素会严重危害身体健康。请你结合实际提出两条杜绝铝元素过量吸入的措施:____________。
查看习题详情和答案>>
工业生产金属铝的原料是铝土矿(主要成分为Al2O3,另含有Fe2O3和SiO2),工业中得到较纯氧化铝的过程如下图所示:
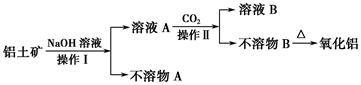
试回答下列问题:
(1)操作Ⅰ是一种重要的混合物分离方法,实验室进行该项操作用到的玻璃仪器有烧杯、________、________。
(2)经分析不溶物A的主要成分为________。
(3)工业上电解冶炼铝的化学方程式为________________,若电路中通过1 mol电子,可以得到铝________g。
(4)为了提高综合经济效益,实际工业生产中常将上述反应中的相关物质循环利用。其部分转化关系如下图所示:
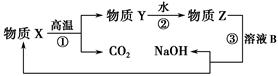
①上述转化中未涉及四种基本反应类型中的________反应;
②写出过程③的化学方程式:____________。
(5)科学研究表明,人体过量吸入铝元素会严重危害身体健康。请你结合实际提出两条杜绝铝元素过量吸入的措施:____________。

试回答下列问题:
(1)操作I是一种重要的混合物分离方法,实验室进行该项操作用到的玻璃仪器有烧杯、
(2)经分析不溶物A的主要成分为
(3)工业上电解炼铝的化学方程式为
(4)操作Ⅱ中生成不溶物B的离子方程式是
(5)为了提高综合经济效益,实际工业生产中常将上述反应中的相关物质循环利用.其部分转化关系如图所示:

①上述转化中未涉及四种基本反应类型中的
②写出③的化学方程式(该反应在工业生产中称为苛化法)
(6)科学研究表明,人体过量摄入铝元素会严重危害身体健康.请你结合实际提出两条杜绝铝元素过量摄入的措施:
在长期载人太空飞行的宇航器中,每个宇航员平均每天需要消耗0.9kg氧气,呼出1.0kg的二氧化碳。为了能保持飞船座舱内空气成分的稳定,宇航科学家进行了大量的科学探索。方法一:有的科学家提出“金属过氧化物处理系统”,即不断的将座舱内的空气通过盛有金属过氧化物(以过氧化钠为例)的容器,并把处理后的气体充入座舱。有关反应的化学方程式为:①________②________;将处理后的气体充入座舱时,应注意采取的一项措施是________
方法二:有的科学家根据电解原理设计了飞船内空气更新实验系统,该系统结构示意图如下:

(1)管道①把飞船座舱内含有较多二氧化碳的潮湿的空气通入“电化学二氧化碳处理系统”的N极室,通过该电极反应可以使二氧化碳不断被吸收;该电极反应式为________
其电解产物吸收二氧化碳的离子反应方程式为________。在N极吸收二氧化碳后形成的离子会通过隔膜进入M极室,通过M极的电极反应可以使二氧化碳从电解液中释放出来,并保持系统的pH不变;该电极反应式为________、________。
(2)管道②是将处理后的空气混入“电解水系统”产生的新鲜氧气,然后通入飞船座舱内供宇航员呼吸用。在“电解水系统”中Y为________极(填“阴”或“阳”)X极的电极反应为________
(3)逸出的二氧化碳没有排出飞船外,而是通过管道③进入“二氧化碳还原系统”。在该系统内,二氧化碳跟氢气在一定条件下反应,其产物中有甲烷等气体,请评价这种处理的意义________
下表是某食品包装上的说明,表中列出了部分配料。

(2)从上表中可以分析得知,该食品主要提供_____________________等三种营养素。
(3)我国中南地区,通常情况下,雨水量相同的元月份与8月份比较,___________(填:“前者”或“后者”)的雨水的酸性较高。
(4)汽车尾气需要用催化转换器减少有毒气体的排放。写出汽车尾气中CO、NO相互作用生成可参与大气循环的气体的化学方程式:_______________________。
(5)用氯气对居民饮用水进行消毒已有百年历史,但科学研究表明,用氯气对自来水消毒时,氯气能和水中的微量有机物反应生成氯代烃等多种有毒物质。因此,逐步被具有不同优点的铁酸钠(Na2FeO4)、氯胺(NH2Cl)、二氧化氯(ClO2)等消毒剂所替代。?
①铁酸钠(Na2FeO4)起消毒作用后,它同时具有净水作用,其理由:________________________(用离子方程式表示)。
②氯胺(NH2Cl)比次氯酸稳定,可与水作用逐步产生次氯酸,用化学方程式表示氯胺与水的反应:
____________________。
③二氧化氯(ClO2)具有很强的氧化性,与Cl2相比是一种高效消毒剂,其原因是________________。
(6)阅读并回答问题: 2009年12月哥本哈根气候变化峰会的主题是减少二氧化碳的排放、控制温室效应。世界上没有垃圾,只有放错了地方的财富。人类在认识到二氧化碳副作用的同时,应积极寻找并拓展其利用空间。上海世博会已成为低碳世博会。“四川馆”率先采用世界上最新的建筑装饰材料--大豆纤维。中国是唯一拥有“大豆纤维”完全知识产权的国家。“大豆纤维”主要原料是大豆蛋白质和高分子聚乙烯醇,它属于可降解性再生植物蛋白纤维,该纤维具有天然纤维和化学纤维的许多优良性能,被国内外专家誉为“21世纪健康舒适型纤维”。
下列说法不正确的是___________________
A.二氧化碳无毒、分子结构稳定,它可以用于做焊接保护气体。
B.发展二氧化碳地质封存技术并将其与石油开采结合起来,既能减少二氧化碳排放,又实现了石油的绿色开发。
C.从空气中提取CO2,成本较高,如果从冶金、火力发电等工厂排放的烟气中提取二氧化碳,提取成本将大大降低。
D.碳酸饮料中的二氧化碳能够被人体吸收,不会排放到空气中去。
E.不能使用含生物酶的洗涤剂洗涤大豆纤维布料的衣服。
F.大豆纤维是利用大豆中的油脂通过聚合反应合成的。
G.大豆纤维属于合成高分子化合物。
H.废弃的大豆纤维可能造成“白色污染”,最好用填埋法处理。