网址:http://m.1010jiajiao.com/timu3_id_373977[举报]
为测定碳酸钙粉末的纯度(含杂质SiO2),某学校学生设计了如下几个实验方案:
方案一:①称取碳酸钙样品M g;②加入过量盐酸;③收集并测定生成的气体体积V mL。
方案二:①称取碳酸钙样品M g;②用c mol/L盐酸V mL(过量)溶解样品;③取溶解后的溶液用c′mol/L NaOH溶液滴定,恰用去V′ mL。
方案三:①称取碳酸钙样品M g;②高温1000 ℃煅烧直至质量不再改变,冷却后称量,质量为M′ g。
方案四:①称取碳酸钙样品M g;②加入足量c mol/L盐酸V mL使之完全溶解;③过滤并取滤液;④在滤液中加入过量的c′mol/L Na2CO3溶液V′mL;⑤将步骤④中的沉淀滤出,洗涤、干燥、称量为M′g。
依据以上实验方案回答以下问题:
(1)方案一中如果称量样品时,砝码底部有一处未被发现的残缺,那么测得的碳酸钙纯度会________(填“偏高”、“偏低”或“无影响”)。
(2)方案二中:列出本实验中所用到的仪器名称(除铁架台、烧杯、铁架台附件外)_________________________________________________________________________。
(3)方案三中的“冷却”应如何操作:
____________________________________________________________;
理由是_________________________________________________________。
(4)方案四中计算碳酸钙纯度的公式为______________;步骤⑤中要将沉淀进行洗涤,如果未经洗涤,则测定结果碳酸钙纯度将________(填“偏高”、“偏低”或“无影响”)。
(5)综上所述,请从实验条件的难易、操作引起实验误差的大小等方面进行综合判断,你认为四个方案中,最好的方案是________。其他方案的缺点分别是:
方案四:沉淀的洗涤、干燥、称量操作过程复杂,容易造成较大误差。
方案________:_____________________________________________________。
方案________:____________________________________________________。
查看习题详情和答案>>
方案Ⅰ:①称取碳酸钙样品M g;②加入过量盐酸;③收集并测定生成的气体体积V mL。
方案Ⅱ:①称取碳酸钙样品M g;②用c mol·L-1?盐酸V mL(过量)溶解样品;③取溶解后的溶液用c′ mol·L-1 NaOH溶液滴定,恰用去V′ mL。
方案Ⅲ:①称取碳酸钙样品M g;②高温煅烧1
方案Ⅳ:①称取碳酸钙样品Mg;②加入足量c mol·L-1盐酸V mL使完全溶解;③过滤并取滤液;④在滤液中加入过量c′ mol·L-1 Na2CO3溶液V′ mL;⑤将步骤④中的沉淀滤出,洗涤、干燥、称量为M′ g。
依据以上实验方案回答以下问题:
(1)方案Ⅰ中如果称量样品时,砝码底部有一处未被人发现的残缺,那么测得的碳酸钙纯度会____________(填“偏高”“偏低”或“无影响”)。
(2)方案Ⅱ中:列出本实验中所用到的仪器名称(除铁架台、烧杯、铁架台附件外)____________________________________________________________________。
(3)方案Ⅲ中的“冷却”应如何操作:_________________________________________;理由是__________________________________________________________________。
(4)方案Ⅳ中计算碳酸钙纯度的公式为_____________;步骤⑤中要将沉淀进行洗涤,如果未经洗涤,则测定结果,碳酸钙纯度将_____________(填“偏高”“偏低”或“无影响”)。
(5)综上所述,请从实验条件的难易、操作引起实验误差的大小等方面进行综合判断,你认为四个方案中,最好的方案是_____________。其他方案的缺点分别是:
方案Ⅳ:沉淀的洗涤、干燥、称量操作过程复杂,容易造成较大误差。
方案:__________:___________________________________________________。
方案:__________:___________________________________________________。
查看习题详情和答案>>
(1)写出图1序号所代表的仪器的名称:B
(2)图2是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
现用该浓硫酸配制100mL 1mol/L的稀硫酸.可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平.
请回答下列问题:
Ⅰ配制稀硫酸时,上述仪器中不需要使用的有
Ⅱ经计算,该浓硫酸的物质的量浓度为
Ⅲ用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是
A.吸出多余液体,使凹液面与刻度线相切
B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
C.经计算加入一定量的浓盐酸
D.重新配制
Ⅳ用该浓硫酸配制100mL1mol/L稀硫酸的正确顺序是
A.冷却 B.量取 C.洗涤 D.定容 E.溶解 F.摇匀 G.移液
Ⅴ将所配制的稀硫酸进行测定,发现浓度大于1mol/L.请你分析配制过程中可能引起该误差的原因是(填序号)
①容量瓶不干燥,含有少量蒸馏水 ②定容时俯视刻度线 ③定容时仰视刻度线
④未冷却至室温就转移到容量瓶中 ⑤没有洗涤烧杯和玻璃棒
Ⅵ请写出“定容”的具体操作:
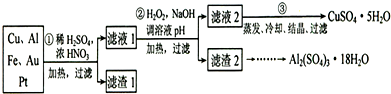
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
| ||
| ||
| ||
| ||
(2)第②步加H2O2的作用是
(3)用第③步所得CuSO4?5H2O制备无水CuSO4的方法是
(4)由滤渣2制取Al2(SO4)3?18H2O,探究小组设计了三种方案:
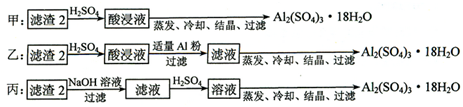
上述三种方案中,

部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀物 | 1.1 | 4.0 | 5.4 |
| 完全沉淀物 | 3.2 | 5.2 | 6.7 |
(2)Cu可溶于稀硫酸与H2O2的混合溶液,其离子方程式是
(3)滤渣a的主要成分是
(4)步骤③中X的取值范围是
(5)某小组甲同学提出如下方案测定CuSO4?5H2O晶体的纯度.取b g试样配成100m L溶液,每次取20.00m L,消除干扰离子后,用c mol?L-1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液12.00m L.滴定反应如下:Cu2++H2Y2-═CuY2-+2H+.
①写出计算CuSO4?5H2O质量分数的表达式w=
| 15c |
| a |
| 15c |
| a |
②下列操作会导致CuSO4?5H2O含量的测定结果偏高的是
a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡c.未除净可与EDTA反应的干扰离子
③该小组乙同学提出通过直接测定样品中SO42一的量也可求得硫酸铜晶体的纯度,老师审核后予以否决,其原因是