题目内容
信息时代给人们的生活带来了极大的便利,但同时也产生了大量的电子垃圾.某化学兴趣小组将一批废弃的线路板简单处理后,得到了主要含Cu、Al及少量Fe、Au等金属的混合物,并设计了如下制备硫酸铜晶体和硫酸铝晶体的路线: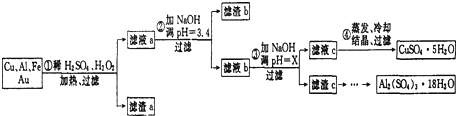
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)过滤操作中用到的玻璃仪器有
(2)Cu可溶于稀硫酸与H2O2的混合溶液,其离子方程式是
(3)滤渣a的主要成分是
(4)步骤③中X的取值范围是
(5)某小组甲同学提出如下方案测定CuSO4?5H2O晶体的纯度.取b g试样配成100m L溶液,每次取20.00m L,消除干扰离子后,用c mol?L-1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液12.00m L.滴定反应如下:Cu2++H2Y2-═CuY2-+2H+.
①写出计算CuSO4?5H2O质量分数的表达式w=
.
②下列操作会导致CuSO4?5H2O含量的测定结果偏高的是
a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡c.未除净可与EDTA反应的干扰离子
③该小组乙同学提出通过直接测定样品中SO42一的量也可求得硫酸铜晶体的纯度,老师审核后予以否决,其原因是

部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀物 | 1.1 | 4.0 | 5.4 |
| 完全沉淀物 | 3.2 | 5.2 | 6.7 |
烧杯、漏斗、玻璃棒
烧杯、漏斗、玻璃棒
.(2)Cu可溶于稀硫酸与H2O2的混合溶液,其离子方程式是
Cu+H2O2+2H+═Cu2++2H2O
Cu+H2O2+2H+═Cu2++2H2O
.(3)滤渣a的主要成分是
Au
Au
.(4)步骤③中X的取值范围是
5.2≤X<5.4
5.2≤X<5.4
.(5)某小组甲同学提出如下方案测定CuSO4?5H2O晶体的纯度.取b g试样配成100m L溶液,每次取20.00m L,消除干扰离子后,用c mol?L-1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液12.00m L.滴定反应如下:Cu2++H2Y2-═CuY2-+2H+.
①写出计算CuSO4?5H2O质量分数的表达式w=
| 15c |
| a |
| 15c |
| a |
②下列操作会导致CuSO4?5H2O含量的测定结果偏高的是
c
c
(填字母).a.未干燥锥形瓶 b.滴定终点时滴定管尖嘴中产生气泡c.未除净可与EDTA反应的干扰离子
③该小组乙同学提出通过直接测定样品中SO42一的量也可求得硫酸铜晶体的纯度,老师审核后予以否决,其原因是
样品中的杂质Na2SO4中也含有SO42-
样品中的杂质Na2SO4中也含有SO42-
.分析:(1)过滤操作用到的仪器有烧杯、漏斗、玻璃棒;
(2)铜被双氧水氧化成铜离子,Cu+H2O2+2H+→Cu2++2H2O;
(3)Cu、Al及少量Fe、Au等金属的混合物,其中铜、铝、铁都发生反应而溶解,Au化学性质稳定,成为滤渣a的主要成分;
(4)滤渣c是氢氧化铝,根据部分阳离子以氢氧化物形式沉淀时溶液的pH表,选择使氢氧化铝沉淀完全且氢氧化铜不沉淀的PH;
(5)①根据反应方程式及滴定数据计算出硫酸铜的物质的量,再计算出硫酸铜晶体的质量分数;
②根据CuSO4?5H2O质量分数的表达式:
×100% 分析误差;
③样品中的杂质Na2SO4中也含有SO42-.
(2)铜被双氧水氧化成铜离子,Cu+H2O2+2H+→Cu2++2H2O;
(3)Cu、Al及少量Fe、Au等金属的混合物,其中铜、铝、铁都发生反应而溶解,Au化学性质稳定,成为滤渣a的主要成分;
(4)滤渣c是氢氧化铝,根据部分阳离子以氢氧化物形式沉淀时溶液的pH表,选择使氢氧化铝沉淀完全且氢氧化铜不沉淀的PH;
(5)①根据反应方程式及滴定数据计算出硫酸铜的物质的量,再计算出硫酸铜晶体的质量分数;
②根据CuSO4?5H2O质量分数的表达式:
| 15c |
| a |
③样品中的杂质Na2SO4中也含有SO42-.
解答:解:(1)过滤是化学实验中经常用到的实验操作.过滤操作中用到的玻璃仪器有烧杯、玻璃棒、漏斗;
故答案为:烧杯、漏斗、玻璃棒;
(2)Cu可溶于稀硫酸与H2O2的混合溶液,铜被氧化成铜离子,双氧水生成水,根据化合价升降相等配平,反应的离子方程式是:Cu+H2O2+2H+=Cu2++2H2O;
故答案为:Cu+H2O2+2H+═Cu2++2H2O;
(3)由于Cu、Al、Fe都因反应溶解于溶液中,剩下Au不反应,过滤到了滤渣a中;
故答案为:Au;
(4)加入氢氧化钠溶液调节PH=x,目的是生成氢氧化铝沉淀,氢氧化铝开始沉淀PH=4,沉淀完全PH=5.2,氢氧化铜开始沉淀PH=5.4,所以选择的PH范围是:5.2≤X<5.4;
故答案为:5.2≤X<5.4;
(5)①根据方程式可知20.00mL溶液中n(CuSO4?5H2O)=n(EDTA)=c×12×10-3mol;
所以m(CuSO4?5H2O)=c×12×10-3mol×250g/mol=3c g,
因此100mL溶液中CuSO4?5H2O的质量为:3c×5=15cg,所以ω=
×100%,
故答案为:
×100%;
②根据CuSO4?5H2O质量分数的表达式:
×100% 分析,
a.未干燥锥形瓶,对滴定无影响;
b.滴定终点时滴定管尖嘴中产生气泡,读数时标准溶液体积偏小,结果偏小;
c.未除净可与EDTA反应的干扰离子,导致消耗的EDTA偏多,计算结果偏大,
故答案为c;
③由于样品中的杂质Na2SO4中也含有SO42-,不能通过直接测定样品中SO42-的量求得硫酸铜晶体的纯度,
故答案为:样品中的杂质Na2SO4中也含有SO42-.
故答案为:烧杯、漏斗、玻璃棒;
(2)Cu可溶于稀硫酸与H2O2的混合溶液,铜被氧化成铜离子,双氧水生成水,根据化合价升降相等配平,反应的离子方程式是:Cu+H2O2+2H+=Cu2++2H2O;
故答案为:Cu+H2O2+2H+═Cu2++2H2O;
(3)由于Cu、Al、Fe都因反应溶解于溶液中,剩下Au不反应,过滤到了滤渣a中;
故答案为:Au;
(4)加入氢氧化钠溶液调节PH=x,目的是生成氢氧化铝沉淀,氢氧化铝开始沉淀PH=4,沉淀完全PH=5.2,氢氧化铜开始沉淀PH=5.4,所以选择的PH范围是:5.2≤X<5.4;
故答案为:5.2≤X<5.4;
(5)①根据方程式可知20.00mL溶液中n(CuSO4?5H2O)=n(EDTA)=c×12×10-3mol;
所以m(CuSO4?5H2O)=c×12×10-3mol×250g/mol=3c g,
因此100mL溶液中CuSO4?5H2O的质量为:3c×5=15cg,所以ω=
| 15c |
| a |
故答案为:
| 15c |
| a |
②根据CuSO4?5H2O质量分数的表达式:
| 15c |
| a |
a.未干燥锥形瓶,对滴定无影响;
b.滴定终点时滴定管尖嘴中产生气泡,读数时标准溶液体积偏小,结果偏小;
c.未除净可与EDTA反应的干扰离子,导致消耗的EDTA偏多,计算结果偏大,
故答案为c;
③由于样品中的杂质Na2SO4中也含有SO42-,不能通过直接测定样品中SO42-的量求得硫酸铜晶体的纯度,
故答案为:样品中的杂质Na2SO4中也含有SO42-.
点评:本题考查金属混合物的分离和提纯,关键是提取题中的信息,根据所学知识完成,本题难度中等

练习册系列答案
相关题目
信息时代给人们的生活带来了极大的便利,但同时也产生了大量的电子垃圾.某化学兴趣小组将一批废弃的线路板简单处理后,得到了主要含Cu、Al及少量Fe、Au等金属的混合物,并设计了如下制备硫酸铜晶体和硫酸铝晶体的路线:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 3.2 | 5.2 | 6.7 |

(1)过滤操作中用到的玻璃仪器有______.
(2)Cu可溶于稀硫酸与H2O2的混合溶液,其离子方程式是______.
(3)滤渣a的主要成分是______.
(4)步骤③中X的取值范围是______.
(5)假设制得的CuSO4?5H2O中只含Na2SO4杂质,若用该样品进行“硫酸铜晶体结晶水含量的测定”实验,测得结晶水含量______(填“偏低”、“偏高”或“无影响”).乙同学取1.280g该样品,加热至恒重称得质量变为0.830g,则此样品的纯度为______.(用小数表示,保留三位有效数字)