摘要:根据如图2所示A D的实验装置和试剂进行实验.试剂:①盐酸 ②溴水③亚硫酸钠 ④FeS ⑤CuSO4 ⑥品红溶液 图2 (1)装置A主要是由仪器 组装起来的. (2)要制取SO2气体.证明它既有氧化性又具还原性.并组装一套装置: (Ⅰ)按实验连接的顺序.把a f各导管口连接起来a→ . (Ⅱ)上述A C装置中.放入的试剂是A .B .C . (Ⅲ)表现SO2还原性的实验是在 装置中.现象是 . (Ⅳ)表现SO2氧化性的实验是在 装置中.现象是 . (Ⅴ)D装置连接的烧杯中NaOH溶液的作用是 .
网址:http://m.1010jiajiao.com/timu3_id_36976[举报]
根据如图回答问题:
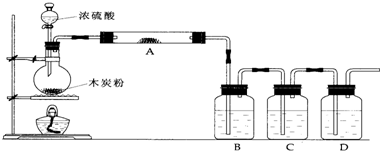
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气.
答:
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂是
B中加入的试剂是
C中加入的试剂是
D中加入的试剂是
(4)实验时,C中应观察到的现象是
查看习题详情和答案>>

(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气.
答:
反应前点燃酒精灯,加热烧瓶一小会儿.在瓶B、C、D中出现气泡,熄灭酒精灯,瓶B、C、D中导管液面上升,证明该装置不漏气
反应前点燃酒精灯,加热烧瓶一小会儿.在瓶B、C、D中出现气泡,熄灭酒精灯,瓶B、C、D中导管液面上升,证明该装置不漏气
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:
2H2SO4(浓)+C
CO2↑+2SO2↑+2H2O
| ||
2H2SO4(浓)+C
CO2↑+2SO2↑+2H2O
| ||
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂是
无水硫酸铜
无水硫酸铜
,作用是检验 H2O
检验 H2O
.B中加入的试剂是
品红溶液
品红溶液
,作用是检验 SO2
检验 SO2
.C中加入的试剂是
足量酸性KMnO4 溶液
足量酸性KMnO4 溶液
,作用是除尽SO2
SO2
气体.D中加入的试剂是
澄清石灰水
澄清石灰水
,作用是检验 CO2
检验 CO2
.(4)实验时,C中应观察到的现象是
导管有气泡冒出,溶液紫色逐渐变浅,瓶底有少量黑色固体生成
导管有气泡冒出,溶液紫色逐渐变浅,瓶底有少量黑色固体生成
.根据如图回答问题:
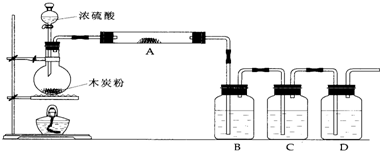
(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气.
答:______
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:______
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂是______,作用是______.
B中加入的试剂是______,作用是______.
C中加入的试剂是______,作用是除尽______气体.
D中加入的试剂是______,作用是______.
(4)实验时,C中应观察到的现象是______.
查看习题详情和答案>>

(1)上述装置中,在反应前用手掌紧贴烧瓶外壁检查装置的气密性,如观察不到明显的现象,还可以用什么简单的方法证明该装置不漏气.
答:______
(2)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:______
(3)如果用图中的装置检验上述反应的全部产物,写出下面标号所表示的仪器中应加入的试剂的名称及其作用:
A中加入的试剂是______,作用是______.
B中加入的试剂是______,作用是______.
C中加入的试剂是______,作用是除尽______气体.
D中加入的试剂是______,作用是______.
(4)实验时,C中应观察到的现象是______.
如图所示为常见气体制备、干燥、性质验证和尾气处理的部分仪器装置(加热设备及固定装置均略去),请根据要求完成下列各题,仪器装置可任意选用,必要时可重复选择.
(1)若锥形瓶中盛装锌片,分液漏斗中盛装稀硫酸,可验证H2的还原性并检验H2的氧化产物.当仪器连接顺序为A→D→B→B→C时,两次使用B装置,其中所盛的药品依次是CuO、
(2)若锥形瓶中盛装
①各仪器装置按气流方向从左到右连接顺序A→C→B→E,请写出B中氨的催化氧化反应方程式
②装置C的作用是
(3)若锥形瓶中盛装Na2SO3固体,分液漏斗中盛装H2SO4溶液,B中盛装Na2O2固体,可探究SO2气体与过氧化钠反应时是否有O2生成.
若SO2与过氧化钠反应没有O2生成,根据气流方向,从图中世择适当的仪器进行实验,装置的连接顺序为(填字母):A→
若有O2生成,实验室检验O2的方法是
查看习题详情和答案>>
(1)若锥形瓶中盛装锌片,分液漏斗中盛装稀硫酸,可验证H2的还原性并检验H2的氧化产物.当仪器连接顺序为A→D→B→B→C时,两次使用B装置,其中所盛的药品依次是CuO、
无水硫酸铜
无水硫酸铜
.(2)若锥形瓶中盛装
Na2O2
Na2O2
固体,分液漏斗中盛装浓氨水,B中盛装固体催化剂,可进行氨的催化氧化,其反应产物为NO和H2O.①各仪器装置按气流方向从左到右连接顺序A→C→B→E,请写出B中氨的催化氧化反应方程式
4NH3+5O2=4NO+6H2O
4NH3+5O2=4NO+6H2O
.②装置C的作用是
除去水蒸气,干燥氨气和氧气
除去水蒸气,干燥氨气和氧气
.(3)若锥形瓶中盛装Na2SO3固体,分液漏斗中盛装H2SO4溶液,B中盛装Na2O2固体,可探究SO2气体与过氧化钠反应时是否有O2生成.
若SO2与过氧化钠反应没有O2生成,根据气流方向,从图中世择适当的仪器进行实验,装置的连接顺序为(填字母):A→
D
D
→B
B
→C/E
C/E
,装置B中可能观察到的现象是淡黄色固体粉末变为白色
淡黄色固体粉末变为白色
.若有O2生成,实验室检验O2的方法是
用带火星木条放到导气管出口,木头复燃证明有氧气
用带火星木条放到导气管出口,木头复燃证明有氧气
.
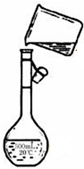 实验室需要0.2mol/L的Na2CO3溶液480mL.现用Na2CO3?10H2O晶体配制,如图装置是某同学转移溶液的示意图.
实验室需要0.2mol/L的Na2CO3溶液480mL.现用Na2CO3?10H2O晶体配制,如图装置是某同学转移溶液的示意图.(1)图中的错误是
没有用玻璃棒引流
没有用玻璃棒引流
,除了图中给出的仪器和托盘天平外,为完成实验还需要的仪器有药匙、玻璃棒、胶头滴管;
药匙、玻璃棒、胶头滴管;
.(2)应用托盘天平称取Na2CO3?10H2O的晶体的质量为
28.6
28.6
g.(3)配制时其正确的操作顺序是(字母表示)
BCAFED
BCAFED
.A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶.
B.准确称取计算量的Na2CO3?10H2O固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解,并冷却至室温.
C.将溶解的Na2CO3溶液沿玻璃棒注入500mL的容量瓶中.
D.将容量瓶盖紧,振荡,摇匀.
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切.
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处.
(4)根据下列操作对所配溶液的浓度各有什么影响,完成填空.
①碳酸钠晶体失去了部分结晶水 ②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠 ④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有
①④
①④
,无影响的有⑤
⑤
.(填序号)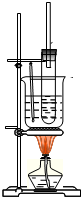 如图所示为实验室制取少量硝基苯的装置.根据题意完成下列填空:
如图所示为实验室制取少量硝基苯的装置.根据题意完成下列填空:(1)写出制取硝基苯的化学方程式
(2)长玻璃导管兼做冷凝管,冷凝的是
(3)用胶头滴管吸取少许上层反应液,滴到水中,当观察到油珠下沉时,表示硝 基苯已生成.这样操作的理由是
(4)将除去混酸后的粗硝基苯先用冷水洗涤,再用10%碳酸钠溶液洗至不显酸性,最后用水洗至中性.洗涤和分离粗硝基苯的仪器是(填仪器名称)
(5)经上述洗涤的硝基苯中仍含少量的间二硝基苯等杂质,提纯硝基苯的方法是
A.苯 B.酒精 C.硫酸 D.水.