题目内容
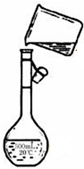 实验室需要0.2mol/L的Na2CO3溶液480mL.现用Na2CO3?10H2O晶体配制,如图装置是某同学转移溶液的示意图.
实验室需要0.2mol/L的Na2CO3溶液480mL.现用Na2CO3?10H2O晶体配制,如图装置是某同学转移溶液的示意图.(1)图中的错误是
没有用玻璃棒引流
没有用玻璃棒引流
,除了图中给出的仪器和托盘天平外,为完成实验还需要的仪器有药匙、玻璃棒、胶头滴管;
药匙、玻璃棒、胶头滴管;
.(2)应用托盘天平称取Na2CO3?10H2O的晶体的质量为
28.6
28.6
g.(3)配制时其正确的操作顺序是(字母表示)
BCAFED
BCAFED
.A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶.
B.准确称取计算量的Na2CO3?10H2O固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解,并冷却至室温.
C.将溶解的Na2CO3溶液沿玻璃棒注入500mL的容量瓶中.
D.将容量瓶盖紧,振荡,摇匀.
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切.
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处.
(4)根据下列操作对所配溶液的浓度各有什么影响,完成填空.
①碳酸钠晶体失去了部分结晶水 ②用“左码右物”的称量方法称量晶体
③碳酸钠晶体不纯,其中混有氯化钠 ④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥就使用
其中引起所配溶液浓度偏高的有
①④
①④
,无影响的有⑤
⑤
.(填序号)分析:(1)转移溶液时,通过玻璃棒引流;根据实验操作的步骤以及每步操作需要仪器确定反应所需仪器;
(2)根据n=cv计算溶质Na2CO3的物质的量,利用Na2CO3?10H2O的物质的量等于Na2CO3的物质的量,根据m=nM计算Na2CO3?10H2O的质量;
(3)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作来解答;
(4)根据c=
分析操作对溶质的物质的量或对溶液的体积的影响判断;
(2)根据n=cv计算溶质Na2CO3的物质的量,利用Na2CO3?10H2O的物质的量等于Na2CO3的物质的量,根据m=nM计算Na2CO3?10H2O的质量;
(3)配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作来解答;
(4)根据c=
| n |
| V |
解答:解:(1)转移溶液时,通过玻璃棒引流,防止液体漏出;配制步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以除了图中给出的仪器和托盘天平外,为完成实验还需要的仪器有
胶头滴管、玻璃棒;
故答案为:没有用玻璃棒引流;药匙、玻璃棒、胶头滴管;
(2)实验室需要0.2mol/L的Na2CO3溶液480mL,由于容量瓶的规格没有480mL,只能用500mL容量瓶,则500mLNa2CO3溶液需要Na2CO3的物质的量为:0.5L×0.2mol/L=0.1mol,Na2CO3?10H2O的物质的量为0.1mol,Na2CO3?10H2O的质量为:0.1mol×286g/mol=28.6g,
故答案为:28.6;
(3)配制步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,先准确称取计算量的Na2CO3?10H2O固体于烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其充分溶解,并冷却至室温,将溶解的Na2CO3溶液沿玻璃棒注入500mL的容量瓶中,用蒸馏水洗涤烧杯2~3次,洗涤液均注入容量瓶,继续往容量瓶内小心加水,直到液面接近刻度2~3cm处,改用胶头滴管加水,使溶液凹面恰好与刻度相切,将容量瓶盖紧,振荡,摇匀.
故答案为:B C A F E D;
(4)①碳酸钠晶体失去了部分结晶水,溶质的质量偏大,溶质的物质的量偏大,则配制溶液浓度偏高;
②用“左码右物”的称量方法称量晶体,溶质的质量偏低,溶质的物质的量偏低,则配制溶液浓度偏低;
③碳酸钠晶体不纯,其中混有氯化钠,溶质的质量偏低,溶质的物质的量偏低,则配制溶液浓度偏低;
④称量碳酸钠晶体时所用砝码生锈,溶质的质量偏大,溶质的物质的量偏大,则配制溶液浓度偏高;
⑤容量瓶未经干燥就使用,溶质的物质的量和溶液的体积都不改变,所以配制溶液浓度不变;
故答案为:①④;⑤;
胶头滴管、玻璃棒;
故答案为:没有用玻璃棒引流;药匙、玻璃棒、胶头滴管;
(2)实验室需要0.2mol/L的Na2CO3溶液480mL,由于容量瓶的规格没有480mL,只能用500mL容量瓶,则500mLNa2CO3溶液需要Na2CO3的物质的量为:0.5L×0.2mol/L=0.1mol,Na2CO3?10H2O的物质的量为0.1mol,Na2CO3?10H2O的质量为:0.1mol×286g/mol=28.6g,
故答案为:28.6;
(3)配制步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,先准确称取计算量的Na2CO3?10H2O固体于烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其充分溶解,并冷却至室温,将溶解的Na2CO3溶液沿玻璃棒注入500mL的容量瓶中,用蒸馏水洗涤烧杯2~3次,洗涤液均注入容量瓶,继续往容量瓶内小心加水,直到液面接近刻度2~3cm处,改用胶头滴管加水,使溶液凹面恰好与刻度相切,将容量瓶盖紧,振荡,摇匀.
故答案为:B C A F E D;
(4)①碳酸钠晶体失去了部分结晶水,溶质的质量偏大,溶质的物质的量偏大,则配制溶液浓度偏高;
②用“左码右物”的称量方法称量晶体,溶质的质量偏低,溶质的物质的量偏低,则配制溶液浓度偏低;
③碳酸钠晶体不纯,其中混有氯化钠,溶质的质量偏低,溶质的物质的量偏低,则配制溶液浓度偏低;
④称量碳酸钠晶体时所用砝码生锈,溶质的质量偏大,溶质的物质的量偏大,则配制溶液浓度偏高;
⑤容量瓶未经干燥就使用,溶质的物质的量和溶液的体积都不改变,所以配制溶液浓度不变;
故答案为:①④;⑤;
点评:本题考查一定物质的量浓度溶液的配制,易错点是计算溶质的质量,很多同学将溶液的体积认为是480mL而导致出错.

练习册系列答案
相关题目