题目内容
如图所示为常见气体制备、干燥、性质验证和尾气处理的部分仪器装置(加热设备及固定装置均略去),请根据要求完成下列各题,仪器装置可任意选用,必要时可重复选择.
(1)若锥形瓶中盛装锌片,分液漏斗中盛装稀硫酸,可验证H2的还原性并检验H2的氧化产物.当仪器连接顺序为A→D→B→B→C时,两次使用B装置,其中所盛的药品依次是CuO、
(2)若锥形瓶中盛装
①各仪器装置按气流方向从左到右连接顺序A→C→B→E,请写出B中氨的催化氧化反应方程式
②装置C的作用是
(3)若锥形瓶中盛装Na2SO3固体,分液漏斗中盛装H2SO4溶液,B中盛装Na2O2固体,可探究SO2气体与过氧化钠反应时是否有O2生成.
若SO2与过氧化钠反应没有O2生成,根据气流方向,从图中世择适当的仪器进行实验,装置的连接顺序为(填字母):A→
若有O2生成,实验室检验O2的方法是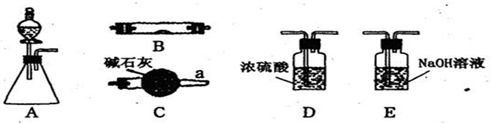
(1)若锥形瓶中盛装锌片,分液漏斗中盛装稀硫酸,可验证H2的还原性并检验H2的氧化产物.当仪器连接顺序为A→D→B→B→C时,两次使用B装置,其中所盛的药品依次是CuO、
无水硫酸铜
无水硫酸铜
.(2)若锥形瓶中盛装
Na2O2
Na2O2
固体,分液漏斗中盛装浓氨水,B中盛装固体催化剂,可进行氨的催化氧化,其反应产物为NO和H2O.①各仪器装置按气流方向从左到右连接顺序A→C→B→E,请写出B中氨的催化氧化反应方程式
4NH3+5O2=4NO+6H2O
4NH3+5O2=4NO+6H2O
.②装置C的作用是
除去水蒸气,干燥氨气和氧气
除去水蒸气,干燥氨气和氧气
.(3)若锥形瓶中盛装Na2SO3固体,分液漏斗中盛装H2SO4溶液,B中盛装Na2O2固体,可探究SO2气体与过氧化钠反应时是否有O2生成.
若SO2与过氧化钠反应没有O2生成,根据气流方向,从图中世择适当的仪器进行实验,装置的连接顺序为(填字母):A→
D
D
→B
B
→C/E
C/E
,装置B中可能观察到的现象是淡黄色固体粉末变为白色
淡黄色固体粉末变为白色
.若有O2生成,实验室检验O2的方法是
用带火星木条放到导气管出口,木头复燃证明有氧气
用带火星木条放到导气管出口,木头复燃证明有氧气
.
分析:(1)第二次使用B装置的作用是检验产物水;
(2)A为制取氧气的装置;
①氨气与氧气反应生成一氧化氮和水;
②碱石灰可干燥气体;
(3)A生成的二氧化硫通过D浓硫酸可干燥二氧化硫,然后在B中与过氧化钠反应,再通过C除掉未反应的二氧化硫,若有氧气生成,则E中有气泡生成,反之则无;过氧化钠是淡黄色固体,与二氧化硫反应后生成硫酸钠白色固体;实验室检验O2的方法是用带火星木条放到导气管出口,木头复燃证明有氧气;
(2)A为制取氧气的装置;
①氨气与氧气反应生成一氧化氮和水;
②碱石灰可干燥气体;
(3)A生成的二氧化硫通过D浓硫酸可干燥二氧化硫,然后在B中与过氧化钠反应,再通过C除掉未反应的二氧化硫,若有氧气生成,则E中有气泡生成,反之则无;过氧化钠是淡黄色固体,与二氧化硫反应后生成硫酸钠白色固体;实验室检验O2的方法是用带火星木条放到导气管出口,木头复燃证明有氧气;
解答:解:(1)第二次使用B装置的作用是检验产物水,可用无水硫酸铜,故答案为:无水硫酸铜;
(2)根据进行进行氨的催化氧化可知A为制取氧气的装置,故锥形瓶中盛装Na2O2,故答案为:Na2O2;
①氨的催化氧化反应方程式:4NH3+5O2=4NO+6H2O,故答案为:4NH3+5O2=4NO+6H2O;
②碱石灰可干燥气体,C的作用为除去水蒸气,干燥氨气和氧气,故答案为:除去水蒸气,干燥氨气和氧气;
(3)A生成的二氧化硫通过D浓硫酸可干燥二氧化硫,然后在B中与过氧化钠反应,再通过C除掉未反应的二氧化硫,若有氧气生成,则E中有气泡生成,反之则无;过氧化钠是淡黄色固体,与二氧化硫反应后生成硫酸钠白色固体,故B中现象为淡黄色固体粉末变为白色;实验室检验O2的方法是用带火星木条放到导气管出口,木头复燃证明有氧气,
故答案为:D;B;C/E;淡黄色固体粉末变为白色;用带火星木条放到导气管出口,木头复燃证明有氧气;
(2)根据进行进行氨的催化氧化可知A为制取氧气的装置,故锥形瓶中盛装Na2O2,故答案为:Na2O2;
①氨的催化氧化反应方程式:4NH3+5O2=4NO+6H2O,故答案为:4NH3+5O2=4NO+6H2O;
②碱石灰可干燥气体,C的作用为除去水蒸气,干燥氨气和氧气,故答案为:除去水蒸气,干燥氨气和氧气;
(3)A生成的二氧化硫通过D浓硫酸可干燥二氧化硫,然后在B中与过氧化钠反应,再通过C除掉未反应的二氧化硫,若有氧气生成,则E中有气泡生成,反之则无;过氧化钠是淡黄色固体,与二氧化硫反应后生成硫酸钠白色固体,故B中现象为淡黄色固体粉末变为白色;实验室检验O2的方法是用带火星木条放到导气管出口,木头复燃证明有氧气,
故答案为:D;B;C/E;淡黄色固体粉末变为白色;用带火星木条放到导气管出口,木头复燃证明有氧气;
点评:本题考查化学实验方案设计,难度较大,注意掌握实验的原理.

练习册系列答案
相关题目
(12分) 在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
(1)写出实验室制取NH3的化学方程式 。
(2)实验室制取、收集干燥的NH3 ,需选用上述仪器装置的接口连接顺序是(选填字母):a接 , 接 , 接h;
,需选用上述仪器装置的接口连接顺序是(选填字母):a接 , 接 , 接h;
(3)用如图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用(选填字母编号);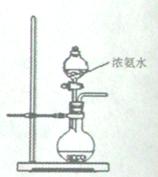
| A.碱石灰 | B.生石灰 | C.无水氯化钙 | D.无水硫酸铜 E.烧碱 |
(5)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级