摘要:酚酞的变色范围
网址:http://m.1010jiajiao.com/timu3_id_354335[举报]
已知:①酚酞的变色范围:pH<8时为无色;pH在8—10之间为粉红色;pH>10至c(OH-)为6 mol·L-1之间呈红色。在其他pH范围时,酚酞显无色。②过氧化氢具有漂白性。
据此完成下列问题:
现将0.39 g Na2O2溶解在10.0 mL水中,再向所得溶液中滴入2滴酚酞,溶液先变红,片刻后红色褪去。
(1)甲同学认为红色褪去的原因是由于溶液中c(OH-)较大,此种说法_________(填“正确”或“不正确”),通过估算说明理由。
(2)乙同学认为红色褪去的原因可能是由于反应中有过氧化氢生成,此种说法_________(填“正确”或“不正确”),并通过①分析推理;②提出假设;③设计实验,来说明理由。
①分析推理_________;②提出假设_________;③设计实验_________。
查看习题详情和答案>>
已知甲基橙和酚酞的变色范围分别为3.1~4.4、8.2~10。用稀盐酸中和碳酸钠溶液时,分两个阶段进行反应,第一阶段:Na2CO3+HCl NaCl+NaHCO3,此时溶液的pH=8.3;第二阶段:NaHCO3+HCl
NaCl+NaHCO3,此时溶液的pH=8.3;第二阶段:NaHCO3+HCl NaCl+CO2↑+H2O,若未赶掉,则溶液的pH约为3.9。取体积相同(
NaCl+CO2↑+H2O,若未赶掉,则溶液的pH约为3.9。取体积相同(0.025 L )的两份0.1 mol·L-1的NaOH溶液,把其中一份放在空气中一段时间后,溶液的pH (填“增大”“减小”或“不变”),其原因是 。用已知浓度的硫酸溶液中和上述两份溶液,中和第一份(在空气中一段时间)所消耗硫酸溶液的体积为V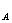 ,另一份消耗硫酸溶液的体积为V
,另一份消耗硫酸溶液的体积为V ,则?
,则?
(1)以甲基橙为指示剂时,V![]() 与V
与V![]() 的关系是 。?
的关系是 。?
(2)以酚酞为指示剂时,V![]() 与V
与V![]() 的关系是 。
的关系是 。
以下是几种酸碱指示剂的变色范围:
①甲基橙3.1~4.4,
②甲基红4.4~6.2,
③酚酞8.2~10.
现用0.1000 mol·L-1 NaOH溶液滴定浓度相近的甲酸时,上述指示剂
- A.都可以用
- B.只能用③
- C.可以用①或②
- D.可以用②或③
|
以下是几种酸碱指示剂的变色范围:①甲基橙3.1~4.4,②甲基红4.4~6.2,③酚酞8.2~10.现用0.1000 mol·L-1 NaOH溶液滴定浓度相近的甲酸时,上述指示剂 | |
| [ ] | |
A. |
都可以用 |
B. |
只能用③ |
C. |
可以用①或② |
D. |
可以用②或③ |
过氧化氢是一种应用范围极广的过氧化物,根据题意,回答下列有关问题:
(1)请举出H2O2的一种用途 .
(2)H2O2是一种二元弱酸,请写出它的第一步电离方程式 .
(3)将H2O2溶液加入盐酸酸化的FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式并标出电子转移情况 .
(4)向盛有少量过氧化钠固体的试管中滴加水,直到气体不再放出,再加水稀释所得溶液,将得到的溶液平均分成两份盛放在两只试管中,进行下列实验:①一只试管中滴加酚酞试液,溶液变红.半分钟红色褪去;②另一只试管中加入少量二氧化锰.又有气体放出,待气体不再放出,再滴加酚酞,溶液变红,持久不褪色.上述实验表明,过氧化钠和水反应可分两步,其化学方程式为:
第一步: ;第二步 .
查看习题详情和答案>>
(1)请举出H2O2的一种用途
(2)H2O2是一种二元弱酸,请写出它的第一步电离方程式
(3)将H2O2溶液加入盐酸酸化的FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式并标出电子转移情况
(4)向盛有少量过氧化钠固体的试管中滴加水,直到气体不再放出,再加水稀释所得溶液,将得到的溶液平均分成两份盛放在两只试管中,进行下列实验:①一只试管中滴加酚酞试液,溶液变红.半分钟红色褪去;②另一只试管中加入少量二氧化锰.又有气体放出,待气体不再放出,再滴加酚酞,溶液变红,持久不褪色.上述实验表明,过氧化钠和水反应可分两步,其化学方程式为:
第一步: