题目内容
已知甲基橙和酚酞的变色范围分别为3.1~4.4、8.2~10。用稀盐酸中和碳酸钠溶液时,分两个阶段进行反应,第一阶段:Na2CO3+HCl(1)以甲基橙为指示剂时,V![]() 与V
与V![]() 的关系是 。?
的关系是 。?
(2)以酚酞为指示剂时,V![]() 与V
与V![]() 的关系是 。
的关系是 。
减小 NaOH溶液吸收空气中的酸性气体CO2生成碳酸钠,碱性减弱 (1)VA=VB(2)VA<VB
解析:相同浓度的NaOH溶液和Na2CO3溶液,碱性前者大于后者。用甲基橙作指示剂,两者都生成Na2SO4,据n(Na+)=2n(SO![]() )得:VA=VB。若用酚酞作指示剂时第一份生成Na2SO4和NaHCO3,第二份生成Na2SO4。根据Na+守恒可知:VA<VB。
)得:VA=VB。若用酚酞作指示剂时第一份生成Na2SO4和NaHCO3,第二份生成Na2SO4。根据Na+守恒可知:VA<VB。

为探究铜与浓硫酸的反应,甲、乙两同学分别设计了图1、图2所示装置,将足量铜和10 mL 18 mol·L-1浓硫酸共热,直到无气体生成为止(假定反应前后试管中溶液的体积不变)。
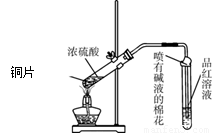

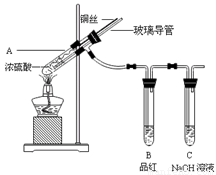 图1
图2
图1
图2
(1)比较两实验装置,图2装置的优点是:① ;② 。
(2)①甲根据所学的化学知识认为还有一定量的硫酸剩余。甲认为硫酸剩余的理论依据是 。
②下列药品中能够用来证明反应结束后的烧瓶中确有硫酸剩余的是_______。(选填编号)
A.过量铁粉 B.氯化钡溶液 C.银粉 D.碳酸氢钠溶液
(3)乙在拆除图2装置前,不打开胶塞,为使装置中的残留气体完全被吸收,应当采取的操作是 。
(4)为定量测定当剩余硫酸浓度不大于何值时,铜与硫酸就不能反应,甲、乙两位同学进行了如下设计:
①甲方案:将产生的气体缓缓通过预先称量过的盛有 的干燥管,反应结束后再次称量,干燥管质量增加m g。其余酸浓度为 mol·L-1。
②乙方案:分离出反应后的溶液并加蒸馏水稀释至1 000 mL,取20.00 mL于锥形瓶中,滴入2~3滴 ,(选填“酚酞”、“甲基橙”)用0.1000mol·L-1标准NaOH溶液进行滴定(已知氢氧化铜开始沉淀的pH约为5),用去NaOH溶液V mL。其余酸浓度为 mol·L-1。
③甲、乙两方案比较,你认为误差较大的是 ,理由是 。