网址:http://m.1010jiajiao.com/timu3_id_352164[举报]
|
在一定温度下,发生可逆反应:2A(g)+2B(g)
| |
| [ ] | |
A. |
甲、乙两容器中的反应达到化学平衡时,若向两容器内各充入1 mol氩气,平衡均不移动 |
B. |
甲、乙两容器中的反应达到化学平衡时,C的体积分数相等 |
C. |
向甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的体积分数不变 |
D. |
向乙容器中再充入2 mol C和6 mol D,平衡后乙中物质C的浓度为原来的2倍 |

关于两容器中反应的说法正确的是( )
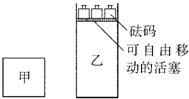 一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )
一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )| A、甲、乙两容器中的反应达到化学平衡时,两容器内压强相等 | B、甲、乙两容器中的反应达到化学平衡时,C的体积分数相等 | C、向甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度不变 | D、向乙容器中再充入2molC和6molD,平衡后乙中物质C的浓度为原来的2倍 |

图1

图2
A.甲容器中的反应先达到化学平衡状态
B.两容器中的反应均达平衡时,平衡混合物中各组分的体积百分组成相同,混合气体的平均相对分子质量也相同
C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲容器中物质C的浓度是乙容器中物质C的浓度的3倍
查看习题详情和答案>>一定温度下,有可逆反应:2A(g)+2B(g) ![]() C(g)3D(g);
C(g)3D(g);![]()
![]() 学科网
学科网
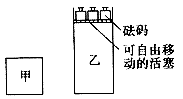
现将2mol A和2 mol B充人体积为V的甲容器,将2mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同。下列说法正确的是![]() 学科网
学科网
![]() 学科网
学科网
A.甲、乙两容器中的反应达到化学平衡时,两容器内压强相等![]() 学科网
学科网
B.甲、乙两容器中的反应达到化学平衡时,C的体积分数相等![]() 学科网
学科网
C.向甲容器中再充人2 molA和2 molB,平衡后甲中物质C的浓度不变![]() 学科网
学科网
D.向乙容器中再充入2 molC和6 molD,平衡后乙中物质C的浓度为原来的2倍![]() 学科网
学科网