题目内容
一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图1).
关于两容器中反应的说法正确的是( )

关于两容器中反应的说法正确的是( )
分析:据题意可知,该反应前后气体的物质的量不变,乙中的气体的物质的量是甲中的两倍,体积也是两倍,且温度相同,将乙容器中的物质全部转化为A、B得出甲容器的浓度与乙容器一样,所以甲与乙完全等效,利用等效平衡分析各个选项即可.
解答:解:A、虽然等效平衡后甲、乙容器中A、B浓度相等,但是该反应一个是从正反应进行,一个从逆反应进行,所以无法判断哪个容器先达平衡,故A错误;
B、等效平衡后甲、乙容器中A、B浓度相等,反应前后气体体积不变,压强不变,所以平衡混合物中各组分的体积百分组成相同,混合气体的平均相对分子质量也相同,故B正确;
C、△H<0,该反应是放热反应,两容器中的反应均达平衡时,升高相同的温度,平衡向逆反应方向移动,物质D的体积分数随温度的升高而降低.因为平衡混合物中各组分的体积百分组成相同,所以两容器中物质D的体积分数随温度变化应该用同曲线表示,故C错误;
D、向甲容器中再充入2molA和2molB,等效为再甲中平衡基础上,增大1倍压强,体积缩小一倍,平衡不移动,反应物转化率不变,平衡后甲中物质C的浓度加倍,所以向甲容器中再充入2molA和2molB,平衡后甲容器中物质C的浓度是乙容器中物质C的浓度的2倍,故D错误;
故选B.
B、等效平衡后甲、乙容器中A、B浓度相等,反应前后气体体积不变,压强不变,所以平衡混合物中各组分的体积百分组成相同,混合气体的平均相对分子质量也相同,故B正确;
C、△H<0,该反应是放热反应,两容器中的反应均达平衡时,升高相同的温度,平衡向逆反应方向移动,物质D的体积分数随温度的升高而降低.因为平衡混合物中各组分的体积百分组成相同,所以两容器中物质D的体积分数随温度变化应该用同曲线表示,故C错误;
D、向甲容器中再充入2molA和2molB,等效为再甲中平衡基础上,增大1倍压强,体积缩小一倍,平衡不移动,反应物转化率不变,平衡后甲中物质C的浓度加倍,所以向甲容器中再充入2molA和2molB,平衡后甲容器中物质C的浓度是乙容器中物质C的浓度的2倍,故D错误;
故选B.
点评:本题考查化学平衡的影响因素、等效平衡等,理解等效平衡是解本题的关键,但本题又是一个反应前后气体体积不变的反应,所以解题时应注意分析.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
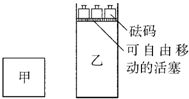 一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )
一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )| A、甲、乙两容器中的反应达到化学平衡时,两容器内压强相等 | B、甲、乙两容器中的反应达到化学平衡时,C的体积分数相等 | C、向甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度不变 | D、向乙容器中再充入2molC和6molD,平衡后乙中物质C的浓度为原来的2倍 |
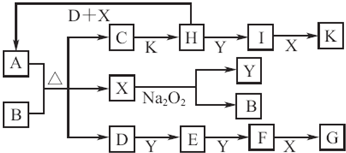
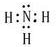
 (2009?肇庆一模)一定温度下,有可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)△H>0,以下说法中正确的是( )
(2009?肇庆一模)一定温度下,有可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)△H>0,以下说法中正确的是( )