题目内容
一定温度下,有可逆反应:2A(g)+2B(g)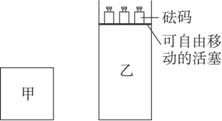
图1
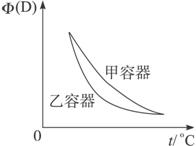
图2
A.甲容器中的反应先达到化学平衡状态
B.两容器中的反应均达平衡时,平衡混合物中各组分的体积百分组成相同,混合气体的平均相对分子质量也相同
C.两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示
D.在甲容器中再充入2 mol A和2 mol B,平衡后甲容器中物质C的浓度是乙容器中物质C的浓度的3倍
B
解析:若乙容器维持体积为2V,则甲、乙反应等效且同时达到化学平衡状态,A不正确;因加压此反应的化学平衡不移动,故两容器中化学平衡等效,即平衡混合物中的各组分的体积百分组成相同,混合气体的平均相对分子质量也相同,所以选项B正确;因为达平衡后两容器的化学平衡等效,则升温过程中物质D的体积分数的变化情况保持一致,故C项不正确;在甲容器若再充入2 mol A和2 mol B,且把容器的体积扩大一倍,则平衡时甲容器中物质C的浓度与乙容器中物质C的浓度相等,现将其体积压缩一倍,化学平衡不移动,但物质C的浓度增大一倍,故甲容器中物质C的浓度是乙容器中物质C的浓度的2倍,选项D错误。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目
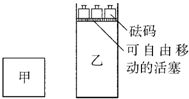 一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )
一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )| A、甲、乙两容器中的反应达到化学平衡时,两容器内压强相等 | B、甲、乙两容器中的反应达到化学平衡时,C的体积分数相等 | C、向甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度不变 | D、向乙容器中再充入2molC和6molD,平衡后乙中物质C的浓度为原来的2倍 |

 (2009?肇庆一模)一定温度下,有可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)△H>0,以下说法中正确的是( )
(2009?肇庆一模)一定温度下,有可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)△H>0,以下说法中正确的是( )