题目内容
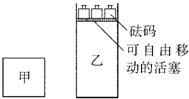 一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )
一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2molA和2molB充入体积为V的甲容器,将2molC和6molD充入乙容器并使乙容器在反应开始前的体积为2V(如图所示),保持反应过程中两容器的温度与起始时相同.下列说法正确的是( )| A、甲、乙两容器中的反应达到化学平衡时,两容器内压强相等 | B、甲、乙两容器中的反应达到化学平衡时,C的体积分数相等 | C、向甲容器中再充入2molA和2molB,平衡后甲中物质C的浓度不变 | D、向乙容器中再充入2molC和6molD,平衡后乙中物质C的浓度为原来的2倍 |
分析:由于反应2A(g)+2B(g)?C(g)+3D(g)中,反应两边气体的体积不变,所以压强不影响化学平衡,只要按照计量数将各物质的物质的量转化成A、B,满足物质的量之比1:1,就是等效平衡,各组分的含量不变;将乙中6molD、2molC转化成反应物为2molA、2molB,所以甲、乙为等效平衡;注意甲的容积不变,乙的压强不变、容积可变.
解答:解:该反应前后气体的体积不变,压强不影响化学平衡,只要按照计量数将各物质的物质的量转化成A、B,满足物质的量之比1:1,就是等效平衡,各组分的含量不变;将乙中6molD、2molC转化成反应物为2molA、2molB,所以甲、乙为等效平衡,
A、根据以上分析,甲乙为等效平衡,反应前后气体的物质的量不变,压强始终不变,反应前压强相等,反应达到化学平衡时,两容器内压强仍然相等,故A正确;
B、甲乙两容器为完全等效平衡,达到化学平衡状态时,甲乙中各组分的含量相同,所以C的体积分数相等,故B正确;
C、向甲容器中再充入2molA和2molB,由于甲的容积固定,达到平衡后,各组分的浓度增大为原来的2倍,故C错误;
D、向乙容器中再充入2molC和6molD,由于乙的容积可变,所以平衡后乙中物质C的浓度不变,故D错误;
故选AB.
A、根据以上分析,甲乙为等效平衡,反应前后气体的物质的量不变,压强始终不变,反应前压强相等,反应达到化学平衡时,两容器内压强仍然相等,故A正确;
B、甲乙两容器为完全等效平衡,达到化学平衡状态时,甲乙中各组分的含量相同,所以C的体积分数相等,故B正确;
C、向甲容器中再充入2molA和2molB,由于甲的容积固定,达到平衡后,各组分的浓度增大为原来的2倍,故C错误;
D、向乙容器中再充入2molC和6molD,由于乙的容积可变,所以平衡后乙中物质C的浓度不变,故D错误;
故选AB.
点评:本题考查了等效平衡的知识,题目难度中等,注意该反应为体积不变的反应,压强不影响平衡,只要满足加入各组分物质的物质的量之比相等,反应达到平衡时一定为等效平衡,各组分的含量、总的物质的量不变.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



 (2009?肇庆一模)一定温度下,有可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)△H>0,以下说法中正确的是( )
(2009?肇庆一模)一定温度下,有可逆反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2 (g)△H>0,以下说法中正确的是( )