网址:http://m.1010jiajiao.com/timu3_id_33260[举报]
Na2SO3是常用的抗氧剂。
(1)实验室通常用浓硫酸(1:1)和Na2SO3微热制备SO2气体,
反应方程式为: ,制备的SO2气体中通常含有水蒸气,下列干燥剂能干燥SO2气体的是: ;
A.浓硫酸 B.碱石灰 C.无水CaCl2
(2) 少量SO2气体通入NaOH溶液中可得NaOH和Na2SO3的混合溶液,向该混合溶液中加入少许溴水,振荡后溶液变为无色。碱性溶液中Br2与Na2SO3发生氧化还原反应,反应的离子方程式为______________;
(3)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO32-、SO42-和Br-的实验报告;
限选试剂:2 mol·L-1HCl;1 mol·L-1H2SO4;1mol·L-1HNO3;1 mol·L-1BaCl2;
1 mol·L-1Ba(NO3)2;0.1 mol·L-1AgNO3;CCl4;苯;新制饱和溴水;新制饱和氯水。
|
编号 |
实验操作 |
预期现象和结论 |
|
步骤① |
取少量待测液于试管A中,滴加2 mol·L-1HCl至溶液呈酸性,加入几滴________(填试剂),振荡 |
________,证明待测液中含SO32- |
|
步骤② |
另取少量待测液于试管B中,加入 ,再滴加适量 1 mol·L-1 BaCl2溶液 |
|
|
步骤③ |
另取少量待测液于试管C中, ,振荡,静置后观察颜色 |
溶液分层,上层液体呈橙红色,证明待测液中很Br- |
查看习题详情和答案>>
Na2SO3是常用的抗氧剂。
(1)实验室通常用浓硫酸(1:1)和Na2SO3微热制备SO2气体,
反应方程式为: ,制备的SO2气体中通常含有水蒸气,下列干燥剂能干燥SO2气体的是: ;
A.浓硫酸 B.碱石灰 C.无水CaCl2
(2) 少量SO2气体通入NaOH溶液中可得NaOH和Na2SO3的混合溶液,向该混合溶液中加入少许溴水,振荡后溶液变为无色。碱性溶液中Br2与Na2SO3发生氧化还原反应,反应的离子方程式为______________;
(3)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO32-、SO42-和Br-的实验报告;
限选试剂:2 mol·L-1HCl;1 mol·L-1H2SO4;1mol·L-1HNO3;1 mol·L-1BaCl2;
1 mol·L-1Ba(NO3)2;0.1 mol·L-1AgNO3;CCl4;苯;新制饱和溴水;新制饱和氯水。
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液于试管A中,滴加2 mol·L-1HCl至溶液呈酸性,加入几滴________(填试剂),振荡 | ________,证明待测液中含SO32- |
| 步骤② | 另取少量待测液于试管B中,加入 ,再滴加适量 1 mol·L-1 BaCl2溶液 | |
| 步骤③ | 另取少量待测液于试管C中, ,振荡,静置后观察颜色 | 溶液分层,上层液体呈橙红色,证明待测液中很Br- |
(1)实验室通常用浓硫酸(1:1)和Na2SO3微热制备SO2气体,
反应方程式为: ,制备的SO2气体中通常含有水蒸气,下列干燥剂能干燥SO2气体的是: ;
A.浓硫酸 B.碱石灰 C.无水CaCl2
(2) 少量SO2气体通入NaOH溶液中可得NaOH和Na2SO3的混合溶液,向该混合溶液中加入少许溴水,振荡后溶液变为无色。碱性溶液中Br2与Na2SO3发生氧化还原反应,反应的离子方程式为______________;
(3)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO32-、SO42-和Br-的实验报告;
限选试剂:2 mol·L-1HCl;1 mol·L-1H2SO4;1mol·L-1HNO3;1 mol·L-1BaCl2;
1 mol·L-1Ba(NO3)2;0.1 mol·L-1AgNO3;CCl4;苯;新制饱和溴水;新制饱和氯水。
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液于试管A中,滴加2 mol·L-1HCl至溶液呈酸性,加入几滴________(填试剂),振荡 | ________,证明待测液中含SO32- |
| 步骤② | 另取少量待测液于试管B中,加入 ,再滴加适量 1 mol·L-1 BaCl2溶液 | |
| 步骤③ | 另取少量待测液于试管C中, ,振荡,静置后观察颜色 | 溶液分层,上层液体呈橙红色,证明待测液中很Br- |

回答下列问题:
(1)①粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A:盐酸;B:BaCl2溶液;C:NaOH溶液;D:Na2CO3溶液.加入试剂的顺序是
②电解饱和食盐水时,与电源正极相连的电极上发生的反应为
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱.
①气体A、B是CO2或NH3,则气体A应是
| ||
| ||
②滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却析出不含有NaHCO3的副产品
NH4Cl晶体,则通入NH3的作用是
(3)空气吹出法工艺,是目前“海水提溴”的最主要方法之一.
a、写出步骤①④反应的离子方程式:①
b、在步骤⑥的蒸馏过程中,温度应控制在80-90℃、温度过高过低都不利于生产,请解释原因:
c、在步骤①、②之后并未直接用“含溴的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是
实验:称取铁钉5.6g放入15.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y.
(l)甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,应选用
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.浓氨水 d.酸性KMnO4溶液
(2)乙同学取448mL (标准状况)气体飞通入足量溴水中,溴水褪色.写出反应的离子方程式:
提出猜想:
II.分析上述实验中SO2体积分数的结果,同学们认为气体Y中还可能含有其它气体并作如下猜想:
猜想一:Y气体中可能含有H2;
猜想二:Y气体中可能含有CO2;
猜想三:Y气体中可能含有H2和CO2
设计实验,验证猜想:
为验证以上猜想,同学们准备用下列装置设计探究实验(装置可重复使用,夹持仪器省略).
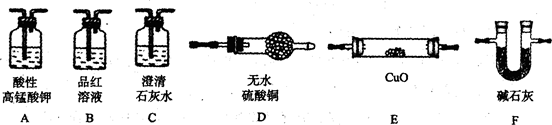
(l)实验装置的连接顺序为A→
(2)装置B中试剂的作用是
(3)猜想一的理由是
(4)如果猜想一成立,预计按①中装置反应则可观察到得实验现象应为: