题目内容
Na2SO3是常用的抗氧剂。
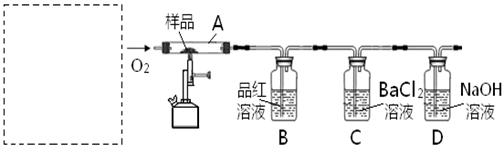
(1)实验室通常用浓硫酸(1:1)和Na2SO3微热制备SO2气体,
反应方程式为: ,制备的SO2气体中通常含有水蒸气,下列干燥剂能干燥SO2气体的是: ;
A.浓硫酸 B.碱石灰 C.无水CaCl2
(2) 少量SO2气体通入NaOH溶液中可得NaOH和Na2SO3的混合溶液,向该混合溶液中加入少许溴水,振荡后溶液变为无色。碱性溶液中Br2与Na2SO3发生氧化还原反应,反应的离子方程式为______________;
(3)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO32-、SO42-和Br-的实验报告;
限选试剂:2 mol·L-1HCl;1 mol·L-1H2SO4;1mol·L-1HNO3;1 mol·L-1BaCl2;
1 mol·L-1Ba(NO3)2;0.1 mol·L-1AgNO3;CCl4;苯;新制饱和溴水;新制饱和氯水。
(1)实验室通常用浓硫酸(1:1)和Na2SO3微热制备SO2气体,
反应方程式为: ,制备的SO2气体中通常含有水蒸气,下列干燥剂能干燥SO2气体的是: ;
A.浓硫酸 B.碱石灰 C.无水CaCl2
(2) 少量SO2气体通入NaOH溶液中可得NaOH和Na2SO3的混合溶液,向该混合溶液中加入少许溴水,振荡后溶液变为无色。碱性溶液中Br2与Na2SO3发生氧化还原反应,反应的离子方程式为______________;
(3)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO32-、SO42-和Br-的实验报告;
限选试剂:2 mol·L-1HCl;1 mol·L-1H2SO4;1mol·L-1HNO3;1 mol·L-1BaCl2;
1 mol·L-1Ba(NO3)2;0.1 mol·L-1AgNO3;CCl4;苯;新制饱和溴水;新制饱和氯水。
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液于试管A中,滴加2 mol·L-1HCl至溶液呈酸性,加入几滴________(填试剂),振荡 | ________,证明待测液中含SO32- |
| 步骤② | 另取少量待测液于试管B中,加入 ,再滴加适量 1 mol·L-1 BaCl2溶液 | |
| 步骤③ | 另取少量待测液于试管C中, ,振荡,静置后观察颜色 | 溶液分层,上层液体呈橙红色,证明待测液中很Br- |
(1)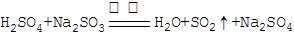 2 分 AC 2分 每个选项1分,错选不给分
2 分 AC 2分 每个选项1分,错选不给分
(2)SO32-+Br2+2OH-=H2O+SO42-+2Br- 2分
(3)
(每空2分)
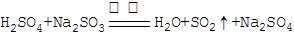 2 分 AC 2分 每个选项1分,错选不给分
2 分 AC 2分 每个选项1分,错选不给分(2)SO32-+Br2+2OH-=H2O+SO42-+2Br- 2分
(3)
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 新制饱和溴水 | 溴水褪色 |
| 步骤② | 加入过量的2 mol·L-1盐酸, | 有白色沉淀生成,证明待测液中含SO42- |
| 步骤③ | 加入足量新制饱和氯水,再加入苯 | |
试题分析:(1)根据强酸制弱酸,浓硫酸(1:1)和Na2SO3微热可制取SO2,化学方程式为:
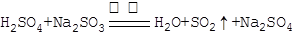 ;SO2为酸性氧化物,不能用碱石灰干燥,可用浓硫酸或无水CaCl2干燥,故A、C项正确。
;SO2为酸性氧化物,不能用碱石灰干燥,可用浓硫酸或无水CaCl2干燥,故A、C项正确。(2)Br2把Na2SO3氧化为SO42?,在碱性条件下离子方程式为:SO32-+Br2+2OH-=H2O+SO42-+2Br-。
(3)SO32?利用还原性检验,加入新制溴水,SO32?被Br2氧化,现象为溴水褪色;SO42?的检验应先加入足量稀盐酸,排除Ag+、CO32?、SO32?等离子的干扰,然后加入BaCl2溶液,有白色沉淀生成,证明待测液含有SO42?;加入足量新制饱和氯水,可把Br?氧化为Br2,因为上层液体呈橙红色,所以加入了密度小于水的苯。

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目


 CaO+CO2 ㈡ 2CaO+2SO2+O2 =2CaSO4
CaO+CO2 ㈡ 2CaO+2SO2+O2 =2CaSO4