摘要:观察右图.若用1 L水来代表地球上的总水量.要比较精确地量取地球上的淡水量.应选择的仪器是 A. 100 mL烧杯 B. 50 mL烧杯 C. 100 mL量筒 D. 50 mL量筒 考室座号 政和一中2006-2007高三第二次月考 化 学 试 卷 班次 姓名 座号 得分
网址:http://m.1010jiajiao.com/timu3_id_329852[举报]
 (1)根据右图回答下列问题:
(1)根据右图回答下列问题:①该仪器的准确名称是
酸式滴定管
酸式滴定管
.②关于该仪器的叙述,不正确的是
D
D
.A.其“0”刻度在上B.精确度比量筒高
C.可量取KMnO4溶液D.可量取NaOH溶液
③现要用该仪器量取VmL液体,若开始时平视刻度读数,结束时俯视刻度读数,则实际所得液体体积比VmL
偏大
偏大
(填“偏大”、“偏小”).(2)用0.100mol/LNaOH溶液滴定未知浓度的盐酸,进行以下滴定操作:
A.用蒸馏水洗净碱式滴定管,然后用标准NaOH溶液润洗,再将标准NaOH溶液装入碱式滴定管中,调整液面至零刻度线.
B.用酸式滴定管量取25.00mL盐酸于锥形瓶中,并滴加几滴酚酞指示剂.
C.在锥形瓶下垫一张白纸,滴定至终点,记下读数为20.00mL.
就此实验完成下列填空:
①滴定时眼睛应观察
锥形瓶中溶液的颜色变化
锥形瓶中溶液的颜色变化
.②滴到终点,溶液的颜色由
无
无
色变为粉红
粉红
色,且半分钟内不褪色.③根据上述数据求得盐酸的物质的量浓度为
0.0800
0.0800
mol/L. 实验室配制500mL 0.500mol?L-1的NaCl溶液,有如下操作步骤:
实验室配制500mL 0.500mol?L-1的NaCl溶液,有如下操作步骤:①把称量好的NaCl晶体放入小烧杯中,加适量蒸馏水溶解;
②把①所得溶液小心转入500mL容量瓶中;
③继续向容量瓶中加蒸馏水至液面距刻度1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹面底部与刻度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀;
⑤将容量瓶塞塞紧,充分摇匀.
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)
①②④③⑤
①②④③⑤
.(2)本实验必须用到的玻璃仪器有
烧杯
烧杯
,玻璃棒
玻璃棒
,500mL容量瓶
500mL容量瓶
,胶头滴管
胶头滴管
.(3)某同学观察液面的情况如右图所示,对所配溶液浓度将有何影响?
偏高
偏高
(选填“偏高”、“偏低”或“无影响”).(4)若没有进行操作步骤④,对所配溶液浓度将有何影响?
偏低
偏低
.(选填“偏高”、“偏低”或“无影响”).(5)若实验过程中出现如下情况,应如何处理?
①加蒸馏水时不慎超过了刻度线:
重新配置
重新配置
.②向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面:
重新配置
重新配置
. NiSO4?6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Zn、Fe、Cr等杂质)为原料获得.操作步骤如下:
NiSO4?6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Zn、Fe、Cr等杂质)为原料获得.操作步骤如下:①用稀硫酸溶液溶解废渣,保持pH约1.5,搅拌30min,过滤.
②向滤液中滴入适量的Na2S,除去Cu2+、Zn2+,过滤.
③保持滤液在40℃左右,用6%的H2O2氧化Fe2+,再在95℃加入NaOH调节pH,除去铁和铬.
④在③的滤液中加入足量Na2CO3溶液,搅拌,得NiCO3沉淀.
⑤
过滤,并用蒸馏水洗涤沉淀2~3次直至流出液用pH试纸检验呈中性
过滤,并用蒸馏水洗涤沉淀2~3次直至流出液用pH试纸检验呈中性
.⑥
向沉淀中加6mol/L的H2SO4溶液,直至恰好完全溶解
向沉淀中加6mol/L的H2SO4溶液,直至恰好完全溶解
.⑦蒸发、冷却结晶并从溶液中分离出晶体.
⑧用少量乙醇洗涤并凉干.
(1)步骤②除可观察到黑色沉淀外,还可嗅到臭鸡蛋气味,用离子方程式说明气体的产生:
S2-+2H+═H2S↑
S2-+2H+═H2S↑
.(2)步骤③中,加6%的H2O2时,温度不能过高,其原因是
减少过氧化氢的分解
减少过氧化氢的分解
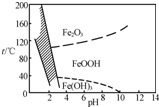
.(3)除铁方法有两种,一是用H2O2作氧化剂,控制pH在2~4范围内生成氢氧化铁沉淀;另一种方法常用NaClO3作氧化剂,在较小的pH条件下水解,最终生成一种浅黄色的黄铁矾钠[Na2Fe6(SO4)4(OH)12]沉淀除去.右图是温度-pH与生成的沉淀关系图,图中阴影部分是黄铁矾稳定存在的区域(已知25℃时,Fe(OH)3的Ksp=2.64×10-39).
下列说法正确的是
cd
cd
(选填序号).a.FeOOH中铁为+2价
b.若在25℃时,用H2O2氧化Fe2+,再在pH=4时除去铁,此时溶液中c(Fe3+)=2.64×10-29
c.用氯酸钠在酸性条件下氧化Fe2+离子方程式为6Fe2++Cl
| O | - 3 |
d.工业生产中温度常保持在85℃~95℃生成黄铁矾钢,此时水体的pH约为1.2~1.8
(4)确定步骤④中Na2CO3溶液足量,碳酸镍已完全沉淀的简单方法是
上层清液呈无色
上层清液呈无色
.(5)补充上述步骤⑤和⑥(可提供的试剂有6mol/L的H2SO4溶液、蒸馏水、pH试纸).
实验室有一瓶Na2SO3固体,可能含有NaCl、Na2SO4、BaCl2、K2CO3、K2SO4中的一种或几种杂质,通过下列实验确定该样品的成分及Na2SO3的质量分数.
①取少量样品于试管中,加水振荡,未见沉淀生成;
②透过蓝色钴玻璃观察,焰色反应无紫色;
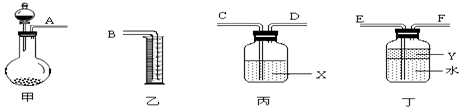
③用右图所示仪器进行合理组装,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)
请回答下列问题:
(1)按气流从左到右方向,正确的连接顺序为:A接 , 接 , 接B.
(2)利用所组装置,由分液漏斗向圆底烧瓶中滴加10mL水,将排入量筒中 mL液体.
(3)液体X是 ,其作用是 .
(4)Y的作用是防止产生的气体溶于水,下列所给试剂符合要求的是 .
A.苯B.四氯化碳C.酒精D.汽油
若称取样品3.00g,加入10.0mol/L的硫酸至过量(共5mL),产生无色气体,排入量筒中液体的体积为229mL(标准状况).
(5)对获得准确的气体体积无益的操作有 (填序号)
①检查装置的气密性;
②连通乙、丁的导管要预先注满水;
③读数时视线与量筒内凹液面最低点相平;
④恢复到室温后再上下调整量筒位置,使乙、丁两液面相平;
⑤在甲装置胶塞上再连接一个导管,通入N2将系统中SO2全部排出.
(6)向逸出气体后的溶液中加入稍过量的BaCl2溶液,过滤、洗涤、干燥,得到白色沉淀13.98g.根据实验所得现象及数据,可知:样品中Na2SO3的质量分数是 ,含有的杂质是 .
查看习题详情和答案>>

①取少量样品于试管中,加水振荡,未见沉淀生成;
②透过蓝色钴玻璃观察,焰色反应无紫色;
③用右图所示仪器进行合理组装,测定产生气体的体积(SO2在硫酸中的溶解忽略不计)
请回答下列问题:
(1)按气流从左到右方向,正确的连接顺序为:A接
(2)利用所组装置,由分液漏斗向圆底烧瓶中滴加10mL水,将排入量筒中
(3)液体X是
(4)Y的作用是防止产生的气体溶于水,下列所给试剂符合要求的是
A.苯B.四氯化碳C.酒精D.汽油
若称取样品3.00g,加入10.0mol/L的硫酸至过量(共5mL),产生无色气体,排入量筒中液体的体积为229mL(标准状况).
(5)对获得准确的气体体积无益的操作有
①检查装置的气密性;
②连通乙、丁的导管要预先注满水;
③读数时视线与量筒内凹液面最低点相平;
④恢复到室温后再上下调整量筒位置,使乙、丁两液面相平;
⑤在甲装置胶塞上再连接一个导管,通入N2将系统中SO2全部排出.
(6)向逸出气体后的溶液中加入稍过量的BaCl2溶液,过滤、洗涤、干燥,得到白色沉淀13.98g.根据实验所得现象及数据,可知:样品中Na2SO3的质量分数是
同学们为了探究镁条与盐酸、醋酸反应时,浓度或温度对反应速率(观察镁条消失的时间)的影响,他们准备了以下化学用品:0.20mol/L与0.40mol/L的HCl溶液、0.2mol/L与0.40mol/L的CH3COOH溶液、4条镁条(形状、大小、质量相同)、几支试管和胶头滴管,酸液温度控制为298K和308K.
(1)该实验缺少的仪器是
(2)酸液都取足量、相同体积,请你帮助完成以下面实验设计表:
(3)相同温度时,镁条与相同浓度的盐酸、醋酸反应,刚开始时两者产生气体的速率盐酸
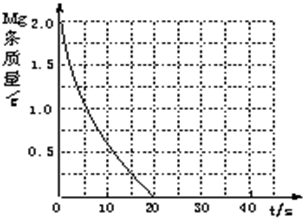
(4)若(2)中实验①镁条消失的时间是20s,则镁条剩余质量与时间关系图如右图.假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同、浓度相同时,醋酸的平均反应速度是盐酸的
.请你在此图中大致画出“实验②”(用实线)、“实验④中醋酸实验”(用虚线)的镁条质量与时间关系曲线.
(5)某温度下,醋酸的电离平衡常数K(CH3COOH)=1.0×10-5.若醋酸的起始浓度为0.10mol/L,则平衡时溶液的pH值是多少?(写出计算过程)
查看习题详情和答案>>
(1)该实验缺少的仪器是
计时器
计时器
.(2)酸液都取足量、相同体积,请你帮助完成以下面实验设计表:
| 实验编号 | 温度(K) | 盐酸浓度(mol?L-1) | 醋酸浓度(mol?L-1) | 实验目的 |
| ① | 298 | 0.20 | a.实验①和②是探究 不同温度 不同温度 对镁与盐酸反应速率的影响;b.实验①和③是探究 不同浓度 不同浓度 对镁与盐酸反应速率的影响;c.实验①和④是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别. | |
| ② | 308 | 0.20 | ||
| ③ | 298 | 0.40 | ||
| ④ | 298 298 |
0.20 0.20 |
>
>
醋酸(选填“=、>或<”),镁条最先消失的是盐酸
盐酸
(选填“盐酸或醋酸”,下同);如果镁条足量,选pH相同、等体积的盐酸和醋酸与镁条反应,产生气体最多的是醋酸
醋酸
.
(4)若(2)中实验①镁条消失的时间是20s,则镁条剩余质量与时间关系图如右图.假设:该反应温度每升高10℃,反应速率是原来的2倍;温度相同、浓度相同时,醋酸的平均反应速度是盐酸的
| 1 |
| 2 |
(5)某温度下,醋酸的电离平衡常数K(CH3COOH)=1.0×10-5.若醋酸的起始浓度为0.10mol/L,则平衡时溶液的pH值是多少?(写出计算过程)