摘要:4.该混合气体只含有一氧化碳.二氧化碳和氢气 [查阅资料]a.无水硫酸铜遇水由白色变为蓝色. b.碱石灰是固体氢氧化钠和氧化钙的混合物. c.浓硫酸具有强烈的吸水性.常用作某些气体的干燥剂 [实验过程]同学们在老师的指导下设计了如下图所示装置.并进行了实验. (1)装置A中无水硫酸铜变蓝.装置B中澄清石灰水变浑浊.由此得出的结论为混合气体中有 .B中变化的化学方程式为 . (2)装置C中的药品为 . (3)E中氧化铜变红.F中无水硫酸铜变蓝.G中澄清石灰水变浑浊.说明混合气体中还存在的气体是 , E中的变化说明氧化铜具有 性. [实验结论]猜想 正确. [实验反思] 经过讨论.同学们将上图中装置C~H进行了简化.只 用下图所示装置并自选必要试剂就能完成探究.其中.干燥管中碱石灰的作用为 . 烧杯上能观察到的现象是 .最后一步的实验操作及现象是 . 评卷人
网址:http://m.1010jiajiao.com/timu3_id_32977[举报]
有一包白色粉末A,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成。为探究其组成,进行如下实验(实验流程如图):

(1)取白色粉末A,向其中加入足量水,充分搅拌后过滤,得到白色沉淀B和无色滤液C。由此可判断,原白色粉末中一定不含有 。
(2)向白色沉淀B中加入足量稀盐酸,沉淀全部溶解,并产生无色气体。由此可判断,原白色粉末中一定含有 。
(3)向无色滤液C中通入一定量二氧化碳,充分反应后过滤,得到白色沉淀D和无色滤液E,由此可判断,原白色粉末中一定还含有 。
(4)若流程图中白色粉末A为20g,白色沉淀D为9.85g,无色滤液E中只含一种溶质。
①无色滤液E中的溶质为 ;
②通过计算确定20g白色粉末A中所含各物质的质量。
(请写出计算及推理过程)
【解析】(1)硫酸铜溶于水得到的是蓝色溶液,可以据此判断该题;
(2)硫酸钡不溶于酸,所以根据白色沉淀全部溶解,可以判断该白色沉淀为碳酸钙,可以据此作答;
(3)通入二氧化碳产生了白色沉淀,根据二氧化碳的性质可以判断该混合物中还含有氢氧化钠和氯化钡;
(4)根据上述分析及题给的条件可以判断出反应为:二氧化碳和氢氧化钠反应生成了碳酸钠,然后氯化钡和碳酸钠的反应,所以最后得到的溶液为氯化钠溶液,可以据此解答该题.
查看习题详情和答案>>
14、一混合气体,可能由氢气、甲烷、一氧化碳和二氧化碳四种气体中的一种或几种组成,为了解该混合气体的组成,进行了下面的实验:
①将混合气体通过澄清的石灰水,未见出现浑浊现象;
②将混合气体点燃,并在火焰上方罩一只冷而干燥的烧杯,烧杯壁上有水珠出现.烧杯倒转后,注入少量澄清的石灰水,振荡,发现烧杯内的石灰水变浑浊;
③将混合气体通过灼热的氧化铜,试管壁上也有水珠出现,但尾气未能使澄清石灰水出现浑浊.
仔细分析上面的实验现象后,对该气体的组成你能得出哪些结论?
查看习题详情和答案>>
①将混合气体通过澄清的石灰水,未见出现浑浊现象;
②将混合气体点燃,并在火焰上方罩一只冷而干燥的烧杯,烧杯壁上有水珠出现.烧杯倒转后,注入少量澄清的石灰水,振荡,发现烧杯内的石灰水变浑浊;
③将混合气体通过灼热的氧化铜,试管壁上也有水珠出现,但尾气未能使澄清石灰水出现浑浊.
仔细分析上面的实验现象后,对该气体的组成你能得出哪些结论?
混合气体中一定不含有一氧化碳和二氧化碳两种气体;
混合气体是由氢气和甲烷两种气体混合而成
.混合气体是由氢气和甲烷两种气体混合而成
(2011?广安)某气体由H2、CO中的一种或两种组成,某化学兴趣小组对该气体的组成进行探究.
[提出问题]该气体由什么物质组成?
[提出假设]猜想Ⅰ:只有氢气;
猜想Ⅱ:只有一氧化碳;
猜想Ⅲ:
[提供信息]由H2、CO中的一种或两种组成的气体能在氧气中安静地燃烧.
[设计实验]将该气体在氧气中完全燃烧的产物依次通过装置A、B,根据装置A、B中物
质质量的变化情况来推测该气体的组成.

[现象与结论]
[分析讨论]
(1)装置A质量增加,说明气体燃烧的产物中有
(2)装置A中浓硫酸的作用
[反思]若某纯净物完全燃烧,将其产物依次通过该套实验装置A、装置B,发现装置A、B的质量都增加了,则该纯净物可能是
查看习题详情和答案>>
[提出问题]该气体由什么物质组成?
[提出假设]猜想Ⅰ:只有氢气;
猜想Ⅱ:只有一氧化碳;
猜想Ⅲ:
氢气与一氧化碳的混合物
氢气与一氧化碳的混合物
;[提供信息]由H2、CO中的一种或两种组成的气体能在氧气中安静地燃烧.
[设计实验]将该气体在氧气中完全燃烧的产物依次通过装置A、B,根据装置A、B中物
质质量的变化情况来推测该气体的组成.

[现象与结论]
| 现象 | 结论 |
| ①.装置A质量增加,装置B质量无变化 | 猜想 猜想Ⅰ 猜想Ⅰ 成立 |
| ②.装置A质量 无变化 无变化 ,装置B质量增加 | 猜想Ⅱ成立 |
| ③.装置A质量增加,装置B质量 增加 增加 | 猜想Ⅲ成立 |
(1)装置A质量增加,说明气体燃烧的产物中有
水
水
生成,推知该气体成分中一定含有氢
氢
元素;装置B质量增加,说明该气体燃烧的产物中有二氧化碳
二氧化碳
生成,推知该气体成分中一定含有碳
碳
元素.(2)装置A中浓硫酸的作用
吸水
吸水
.[反思]若某纯净物完全燃烧,将其产物依次通过该套实验装置A、装置B,发现装置A、B的质量都增加了,则该纯净物可能是
甲烷(乙醇、甲醇等)
甲烷(乙醇、甲醇等)
(任写一种物质的化学式或名称).(2013?顺义区一模)碳家族是化学世界中最庞大的家族,碳及其化合物在生产生活中有着广泛应用.
(1)图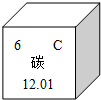 为元素周期表中有关碳元素的信息,碳元素原子核内的质子数为
为元素周期表中有关碳元素的信息,碳元素原子核内的质子数为
(2)含碳的化合物被称为有机化合物,有机高分子材料应用广泛.下列用品,利用合成有机高分子材料的是

(3)二氧化碳的循环对于地球环境有着重要的影响.二氧化碳主要来源于化石燃料的燃烧,化石燃料包括天然气、煤,其中天然气完全燃烧的化学方程式为
(4)工业上用“碳捕捉”技术将CO和CO2混合气体中的CO2捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出):
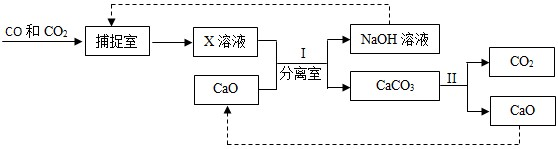
①反应II分离出的CO2可制成干冰,干冰常用于
②分离室中进行的操作是
③下列有关该捕捉过程的叙述中,不正确的有
A.捕捉到的CO2可制备其它化工产品,减少了温室气体排放
B.“分离室”中的反应要吸收大量热
C.整个过程中,只有一种物质可循环利用
D.能量消耗大是该捕捉技术有待解决的问题.
查看习题详情和答案>>
(1)图
 为元素周期表中有关碳元素的信息,碳元素原子核内的质子数为
为元素周期表中有关碳元素的信息,碳元素原子核内的质子数为6
6
.(2)含碳的化合物被称为有机化合物,有机高分子材料应用广泛.下列用品,利用合成有机高分子材料的是
B
B
(填字母序号).
(3)二氧化碳的循环对于地球环境有着重要的影响.二氧化碳主要来源于化石燃料的燃烧,化石燃料包括天然气、煤,其中天然气完全燃烧的化学方程式为
CH4+2O2
CO2+2H2O
| ||
CH4+2O2
CO2+2H2O
.
| ||
(4)工业上用“碳捕捉”技术将CO和CO2混合气体中的CO2捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出):

①反应II分离出的CO2可制成干冰,干冰常用于
人工降雨
人工降雨
;②分离室中进行的操作是
过滤
过滤
;③下列有关该捕捉过程的叙述中,不正确的有
BC
BC
(填字母序号).A.捕捉到的CO2可制备其它化工产品,减少了温室气体排放
B.“分离室”中的反应要吸收大量热
C.整个过程中,只有一种物质可循环利用
D.能量消耗大是该捕捉技术有待解决的问题.