摘要:某学校课外活动小组.对本地化工厂排放废水中的盐酸含量进行了测定.取废水50 g.用质量分数为2%的氢氧化钠溶液进行中和.如右图所示.请你计算废水中盐酸的溶质质量分数. 在测定时.有同学发现在反应过程中.溶液有温度的变化.于是他们进一步进行了探究.在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸.反应中溶液的温度与加入盐酸的体积变化如下: 加入盐酸体积V/mL 2 4 6 8 10 12 14 16 18 20 测得溶液温度t/℃ 15.2 19.6 22.0 26.0 28.2 26.7 25.7 24.7 23.7 22.9 (2)试绘出溶液的温度与加入盐酸的体积之间的变化关系曲线. (3)根据上述曲线变化讨论溶液温度变化的原因. ① 加入盐酸的量在2-10mL之间时: , ② 加入盐酸的量在10-20mL之间时: . (4)若某同学提出“将氢氧化钠固体直接与10%盐酸反应.以探究中和反应是否放热 .此提议是否合理?为什么?答:
网址:http://m.1010jiajiao.com/timu3_id_31952[举报]
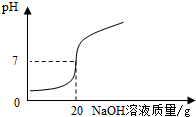 某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为20%的氢氧化钠溶液进行中和,如右图所示.
某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为20%的氢氧化钠溶液进行中和,如右图所示.(1)完全中和50g废水中盐酸需要氢氧化钠溶液的质量是
(2)请你计算废水中盐酸的溶质质量分数.(写出具体的计算过程)
(3)在测定时,有同学发现在氢氧化钠溶液与盐酸反应过程中,溶液有温度的变化.某同学提出“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,此提议是否合理?为什么?
答:
某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用2%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液20g.计算废水中盐酸的溶质质量分数.
在测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究.
(1)①计算废水中盐酸的溶质质量分数 .
②配制100mL10%的盐酸(密度为1.05g/cm3).他们应量取38%的盐酸(密度为1.19g/cm3)多少毫升 mL.
(2)在一定体积的10%的氢氧化钠溶液中,慢慢滴入上述配制的10%的盐酸.有关实验中的数据记录如
试在坐标系中绘出溶液温度变化与加入盐酸体积之间的变化关系图.
(3)根据(2)中关系图,请你从能量变化的角度谈谈对中和反应的认识. .
查看习题详情和答案>>
在测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究.
(1)①计算废水中盐酸的溶质质量分数
②配制100mL10%的盐酸(密度为1.05g/cm3).他们应量取38%的盐酸(密度为1.19g/cm3)多少毫升
(2)在一定体积的10%的氢氧化钠溶液中,慢慢滴入上述配制的10%的盐酸.有关实验中的数据记录如
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 |
| 溶液温度变化(△t)/℃ | 5.2 | 9.6 | 13.0 | 16.0 | 18.2 |

(3)根据(2)中关系图,请你从能量变化的角度谈谈对中和反应的认识.
 某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为20%的氢氧化钠溶液进行中和,如右图所示.
某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为20%的氢氧化钠溶液进行中和,如右图所示.
(1)完全中和50g废水中盐酸需要氢氧化钠溶液的质量是______g.
(2)请你计算废水中盐酸的溶质质量分数.(写出具体的计算过程)
(3)在测定时,有同学发现在氢氧化钠溶液与盐酸反应过程中,溶液有温度的变化.某同学提出“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,此提议是否合理?为什么?
答:______.
查看习题详情和答案>>
 某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用2%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液20g.计算废水中盐酸的溶质质量分数.
某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用2%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液20g.计算废水中盐酸的溶质质量分数.
测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究.
(1)配制100mL10%的盐酸(密度为1.05g/cm3).他们应量取38%的盐酸(密度为1.19g/cm3)多少毫升?
(2)在一定体积的10%的氢氧化钠溶液中,慢慢滴入上述配制的10%的盐酸.有关实验中的数据记录如下:
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 |
| 溶液温度变化(△t)/℃ | 5.2 | 9.6 | 13.0 | 16.0 | 18.2 |
(3)根据(2)中关系图,请你从能量变化的角度谈谈对中和反应的认识. 查看习题详情和答案>>
某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用2%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液20g.计算废水中盐酸的溶质质量分数.
在测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究.
(1)①计算废水中盐酸的溶质质量分数______.
②配制100mL10%的盐酸(密度为1.05g/cm3).他们应量取38%的盐酸(密度为1.19g/cm3)多少毫升______mL.
(2)在一定体积的10%的氢氧化钠溶液中,慢慢滴入上述配制的10%的盐酸.有关实验中的数据记录如
试在坐标系中绘出溶液温度变化与加入盐酸体积之间的变化关系图.
(3)根据(2)中关系图,请你从能量变化的角度谈谈对中和反应的认识.______.
查看习题详情和答案>>
在测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究.
(1)①计算废水中盐酸的溶质质量分数______.
②配制100mL10%的盐酸(密度为1.05g/cm3).他们应量取38%的盐酸(密度为1.19g/cm3)多少毫升______mL.
(2)在一定体积的10%的氢氧化钠溶液中,慢慢滴入上述配制的10%的盐酸.有关实验中的数据记录如
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 |
| 溶液温度变化(△t)/℃ | 5.2 | 9.6 | 13.0 | 16.0 | 18.2 |

(3)根据(2)中关系图,请你从能量变化的角度谈谈对中和反应的认识.______.