题目内容
某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用2%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液20g.计算废水中盐酸的溶质质量分数.
在测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究.
(1)①计算废水中盐酸的溶质质量分数______.
②配制100mL10%的盐酸(密度为1.05g/cm3).他们应量取38%的盐酸(密度为1.19g/cm3)多少毫升______mL.
(2)在一定体积的10%的氢氧化钠溶液中,慢慢滴入上述配制的10%的盐酸.有关实验中的数据记录如
试在坐标系中绘出溶液温度变化与加入盐酸体积之间的变化关系图.
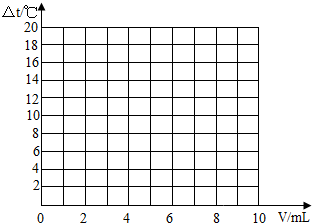
(3)根据(2)中关系图,请你从能量变化的角度谈谈对中和反应的认识.______.
在测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究.
(1)①计算废水中盐酸的溶质质量分数______.
②配制100mL10%的盐酸(密度为1.05g/cm3).他们应量取38%的盐酸(密度为1.19g/cm3)多少毫升______mL.
(2)在一定体积的10%的氢氧化钠溶液中,慢慢滴入上述配制的10%的盐酸.有关实验中的数据记录如
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 |
| 溶液温度变化(△t)/℃ | 5.2 | 9.6 | 13.0 | 16.0 | 18.2 |

(3)根据(2)中关系图,请你从能量变化的角度谈谈对中和反应的认识.______.
(1)①设氯化氢的质量为X.
NaOH+HCl═NaCl+H2O
40 36.5
20g×2% X
=
X=0.365g
稀盐酸的质量分数为:
×100%=0.73%
②溶液稀释前后溶质的质量不变,应量取38%的盐酸(密度为1.19g/cm3)的体积为:
=23.22(mL)
故答案为:0.73%;23.22;
(2)先根据对应的数值描点,连线即可.作图如下:
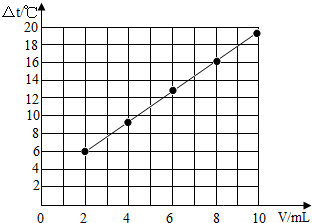
(3)由表中数据可知,随着盐酸和氢氧化钠溶液反应的不断进行,溶液的温度逐渐升高,说明中和反应是放热反应.故填:中和反应是放热反应.
NaOH+HCl═NaCl+H2O
40 36.5
20g×2% X
| 40 |
| 36.5 |
| 20g×2% |
| X |
X=0.365g
稀盐酸的质量分数为:
| 0.365g |
| 50g |
②溶液稀释前后溶质的质量不变,应量取38%的盐酸(密度为1.19g/cm3)的体积为:
| 100×1.05×10% |
| 1.19×38% |
故答案为:0.73%;23.22;
(2)先根据对应的数值描点,连线即可.作图如下:

(3)由表中数据可知,随着盐酸和氢氧化钠溶液反应的不断进行,溶液的温度逐渐升高,说明中和反应是放热反应.故填:中和反应是放热反应.

练习册系列答案
相关题目
某学校课外活动小组用3g少量CO2的CO的混合气体做CO还原CuO实验,实验装詈如下图,实验数据记录如下表,、假定每个反应都完全进行:试计算该实验参加反应的CO的质量分数.
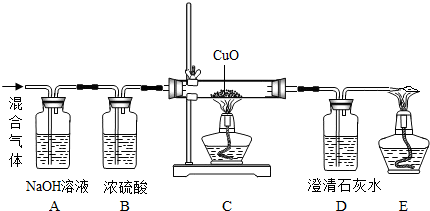
实验记录表

实验记录表
| 实验装置代号 | A | B | D |
| 实验前总质量(g) | 100 | 100 | 100 |
| 实验后总质量(g) | 100.5 | 100.5 | 102.2 |
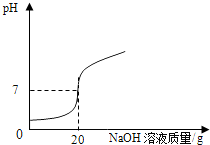 (1)某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为2%的氢氧化钠溶液进行中和,如右图所示.请你计算废水中盐酸的溶质质量分数.(写出具体的计算过程)
(1)某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为2%的氢氧化钠溶液进行中和,如右图所示.请你计算废水中盐酸的溶质质量分数.(写出具体的计算过程)在测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究.在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸,反应中溶液的温度与加入盐酸的体积变化如下:
| 加入盐酸体积V/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 测得溶液温度t/℃ | 15.2 | 19.6 | 22.0 | 26.0 | 28.2 | 26.7 | 25.7 | 24.7 | 23.7 | 22.9 |
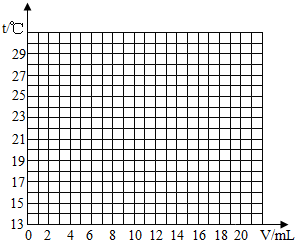
(3)根据上述曲线变化讨论溶液温度变化的原因.
①加入盐酸的量在2~10mL之间时:
②加入盐酸的量在10~20mL之间时:
(4)若某同学提出“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,此提议是否合理?为什么?答:
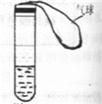 19、某学校课外活动小组利用如图所示的装置做实验:在试管中注入某红色溶液,加热试管一段时间后,溶液红色褪去,冷却后又恢复红色,则原溶液可能是
19、某学校课外活动小组利用如图所示的装置做实验:在试管中注入某红色溶液,加热试管一段时间后,溶液红色褪去,冷却后又恢复红色,则原溶液可能是
 (2005?海门市)某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用2%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液20g.计算废水中盐酸的溶质质量分数.
(2005?海门市)某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用2%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液20g.计算废水中盐酸的溶质质量分数.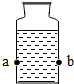 (2013?苏州模拟)某学校课外活动小组,对某造纸厂废水中NaOH含量进行了测定.取一定量的废水,向其中逐渐滴加溶质质量分数为9.8%的稀硫酸(密度约为l.0g/mL),反应过程中不断搅拌并及时测量不同时刻溶液的温度与pH,记录数据如下表:
(2013?苏州模拟)某学校课外活动小组,对某造纸厂废水中NaOH含量进行了测定.取一定量的废水,向其中逐渐滴加溶质质量分数为9.8%的稀硫酸(密度约为l.0g/mL),反应过程中不断搅拌并及时测量不同时刻溶液的温度与pH,记录数据如下表: