摘要:(一)根据化学式的计算: 1.求物质的相对分子质量, 2.求化合物中各元素的质量比, 3.求化合物中某元素的质量分数, 4.求一定量物质中含某元素的质量
网址:http://m.1010jiajiao.com/timu3_id_31711[举报]
根据下列装置图,按要求回答有关问题:
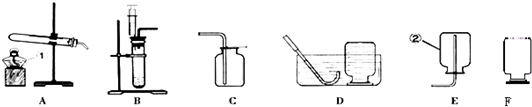
(1)写出图中带有标号仪器的名称:①
(2)若实验室用加热氯酸钾制取干燥的氧气,应选用的装置组合为
(3)若实验室用过氧化氢溶液制取氧气,应选用的发生装置是
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择
(5)小元同学准确称取7.9g纯净的高锰酸钾加热制取氧气,他在试管口放一团棉花,其作用是
意外发现:根据计算,7.9g高锰酸钾完全分解,应生成氧气560mL(标准状况).小元通过数据分析,意外发现收集到的氧气体积和理论计算的氧气体积不相符合,并且在实验中还意外发现锰酸钾能溶于水,二氧化锰不溶于水.
提出假设:小元取实验后的少量固体残渣再次加热,经检验又产生了氧气.根据小元发现的问题和上述实验结果可以做出如下假设:
假设1:二氧化锰也可以受热分解产生氧气;假设2:锰酸钾也可以受热分解产生氧气
假设3:
设计实验:小元用最初加热所得的残渣及必要的实验用品,设计了如下实验流程验证假设2.请在下面实验流程方框中的相应位置填写各步骤的实验操作名称.

请简要叙述步骤5的操作
得出结论:若观察到
查看习题详情和答案>>

(1)写出图中带有标号仪器的名称:①
酒精灯
酒精灯
、②集气瓶
集气瓶
.(2)若实验室用加热氯酸钾制取干燥的氧气,应选用的装置组合为
AC
AC
(填序号),检验氧气已经收集满的方法是将带火星的小木条放在集气瓶口,若木条复燃则收集满了
将带火星的小木条放在集气瓶口,若木条复燃则收集满了
.(3)若实验室用过氧化氢溶液制取氧气,应选用的发生装置是
B
B
(填序号),为了加快双氧水的分解速度,一般在试管中加入药品二氧化锰
二氧化锰
,反应的符号表达式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(4)实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,发生装置可选择
A
A
(填序号).甲烷气体一般采用装置D进行收集,收集满后集气瓶的放置方式如图F所示,据此可推断甲烷一定具备的物理性质是:难溶于水
难溶于水
、密度比空气小
密度比空气小
.(5)小元同学准确称取7.9g纯净的高锰酸钾加热制取氧气,他在试管口放一团棉花,其作用是
防止高锰酸钾粉末冲出,进入导管
防止高锰酸钾粉末冲出,进入导管
;用排水法收集氧气的合适时机是气泡连续均匀冒出时
气泡连续均匀冒出时
;实验结束后,他收集到氧气580mL(标准状况).意外发现:根据计算,7.9g高锰酸钾完全分解,应生成氧气560mL(标准状况).小元通过数据分析,意外发现收集到的氧气体积和理论计算的氧气体积不相符合,并且在实验中还意外发现锰酸钾能溶于水,二氧化锰不溶于水.
提出假设:小元取实验后的少量固体残渣再次加热,经检验又产生了氧气.根据小元发现的问题和上述实验结果可以做出如下假设:
假设1:二氧化锰也可以受热分解产生氧气;假设2:锰酸钾也可以受热分解产生氧气
假设3:
二氧化锰和锰酸钾都可以分解产生氧气
二氧化锰和锰酸钾都可以分解产生氧气
(只填一种)设计实验:小元用最初加热所得的残渣及必要的实验用品,设计了如下实验流程验证假设2.请在下面实验流程方框中的相应位置填写各步骤的实验操作名称.

请简要叙述步骤5的操作
取少量干燥后的固体于试管中充分加热,再将带火星的小
木条伸入试管中
木条伸入试管中
取少量干燥后的固体于试管中充分加热,再将带火星的小
木条伸入试管中
.木条伸入试管中
得出结论:若观察到
带火星木条复燃
带火星木条复燃
,则假设2成立.根据下列实验装置示意图,请回答下列问题:

(1)写出标号①的仪器名称:①______;
(2)实验室用氯酸钾和二氧化锰的混合物制取O2的化学方程式为______;收集O2的装置可选择______(填字母).完全反应后的固体残渣,通过以下四步实验操作可回收得到较纯净的二氧化锰(残渣中只有二氧化锰难于水).正确操作的先后顺序是______(填写选项符号).a.烘干 b.溶解 c.过滤 d.洗涤
分离得到的二氧化锰在反应前后______保持不变.
(3)在实验室用大理石和稀盐酸制取CO2的实验装置中,F装置相对于B装置具有的优点是______;图G所示装置可用来测量生成CO2的体积,其中在水面上放一层植物油的目的______;请在图G方框内补充的仪器,完成测量生成CO2的体积装置 (用黑色水笔画图).取25克大理石与足量的稀盐酸完全反应,收集到二氧化碳为8.8克,求参加反应的碳酸钙为多少摩尔?并求该大理石中碳酸钙的质量分数?(杂质不与酸反应)(写出计算过程)______.
查看习题详情和答案>>
根据下列实验装置示意图,请回答下列问题:

(1)写出标号①的仪器名称:① ;
(2)实验室用氯酸钾和二氧化锰的混合物制取O 2的化学方程式为 ;收集![]() O2的装置可选择 (填
O2的装置可选择 (填![]() 字母)。完全反应后的固体残渣,通过以下四步实验操作可回收得到较纯净的二氧化锰(残渣中只有二氧化锰难于水)。正确操作的先后顺序是 (填写选项符号)。
字母)。完全反应后的固体残渣,通过以下四步实验操作可回收得到较纯净的二氧化锰(残渣中只有二氧化锰难于水)。正确操作的先后顺序是 (填写选项符号)。
a.烘干 b.溶解 c.过滤 d.洗涤
分离得到的二氧化锰在反应前后 保持不变。
(3)在实验室用大理石和稀盐酸制取CO2的实验装置中,F装置相对于B装置具有的优点是 ;
图G所示装置可用来测量生成CO2的体积,其中在水面
上放一层植物油的目的 ;![]()
请在图G方框内 画出补充的仪器,完成测量生成![]() CO2的体积装置
CO2的体积装置
(用黑色水笔画图)。取25克大理石与足量的稀盐酸完全反应, 收集到二氧化碳为8.8克,求参加反应的碳酸钙为多少摩尔?并求该大理石中碳酸钙的质量分数?(杂质不与酸反应)(写出计算过程) 。

在化学实验室,某研究性学习小组发现了一个不和谐的音符,一瓶久置的氢氧化钠固体敞口露置在空气中,他们认为氢氧化钠固体可能变质了,为此他们展开了探究,请你参与.
【查阅资料】Ba(NO3)2溶液呈中性,碳酸钠溶液呈碱性
【实验猜想】可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
【实验探究】(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的Ba(NO3)2溶液,产生白色沉淀,静置后取上层清液,再滴入无色酚酞溶液,溶液变红色.根据实验现象,可确定该固体是 ;
(2)再取固体样品溶于水,加入一定质量分数的稀硫酸,直至过量.测出加入稀硫酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀硫酸,首先与之反应的物质是 .
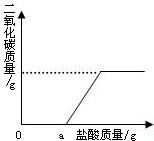
【实验分析】请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀硫酸反应,变质前消耗硫酸的质量 变质后消耗硫酸的质量(填“大于”、“小于”或“等于”).
【综合计算】(1)称取26.5g 该固体样品于锥形瓶中,加入一定质量分数的稀硫酸,直至过量,得到数据如下表:
根据二氧化碳的质量列出求解碳酸钠质量(x)的比例式为
(2)该固体样品中碳酸钠的质量分数是 .
查看习题详情和答案>>
【查阅资料】Ba(NO3)2溶液呈中性,碳酸钠溶液呈碱性
【实验猜想】可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
【实验探究】(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的Ba(NO3)2溶液,产生白色沉淀,静置后取上层清液,再滴入无色酚酞溶液,溶液变红色.根据实验现象,可确定该固体是
(2)再取固体样品溶于水,加入一定质量分数的稀硫酸,直至过量.测出加入稀硫酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀硫酸,首先与之反应的物质是

【实验分析】请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀硫酸反应,变质前消耗硫酸的质量
【综合计算】(1)称取26.5g 该固体样品于锥形瓶中,加入一定质量分数的稀硫酸,直至过量,得到数据如下表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 26.5克 | 148.5克 | 146.3克 |
(2)该固体样品中碳酸钠的质量分数是
某化学兴趣小组在实验室利用下列实验装置及药品,完成以下实验任务:①制备纯净干燥的二氧化碳气体②用一氧化碳气体测定某不纯氧化铁样品的纯度.
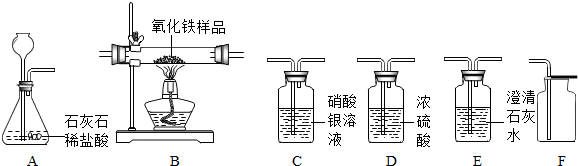
试根据题目要求,回答下列问题:(设过程中所有发生的反应都恰好完全进行,实验中可能挥发少量的HCI气体).
(1)若要制备并收集纯净干燥的二氧化碳,仪器的连接顺序为
(2)装置A中发生反应的化学方程式为
(3)欲用混有少量二氧化碳的一氧化碳气体,测定某不纯氧化铁样品的纯度(杂质不反应),并验证反应中气体生成物的性质.某同学所选仪器的连接顺序为:混合气体→B→E.
①若反应前装置B中样品质量为10g,反应后装置B中固体质量为7.9g,则样品中氧化铁的质量分数为
②若用反应后装置E中增加的质量来计算样品中氧化铁的质量分数,结果将
③从环境保护的角度考虑,针对该套实验装置不足提出的具体改进意见
查看习题详情和答案>>

试根据题目要求,回答下列问题:(设过程中所有发生的反应都恰好完全进行,实验中可能挥发少量的HCI气体).
(1)若要制备并收集纯净干燥的二氧化碳,仪器的连接顺序为
ACDF
ACDF
.(2)装置A中发生反应的化学方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)欲用混有少量二氧化碳的一氧化碳气体,测定某不纯氧化铁样品的纯度(杂质不反应),并验证反应中气体生成物的性质.某同学所选仪器的连接顺序为:混合气体→B→E.
①若反应前装置B中样品质量为10g,反应后装置B中固体质量为7.9g,则样品中氧化铁的质量分数为
70%
70%
.②若用反应后装置E中增加的质量来计算样品中氧化铁的质量分数,结果将
偏大
偏大
(选填“偏大”、“偏小”、“不受影响”之一),请说明理由一氧化碳中混有的二氧化碳没有除去,会使装置E吸收的二氧化碳质量偏大,所以由此计算出的氧化铁的质量偏大,其质量分数也偏大
一氧化碳中混有的二氧化碳没有除去,会使装置E吸收的二氧化碳质量偏大,所以由此计算出的氧化铁的质量偏大,其质量分数也偏大
.③从环境保护的角度考虑,针对该套实验装置不足提出的具体改进意见
在E装置的短管处放一只点燃的酒精灯
在E装置的短管处放一只点燃的酒精灯
.