题目内容
根据下列实验装置示意图,请回答下列问题:

(1)写出标号①的仪器名称:① ;
(2)实验室用氯酸钾和二氧化锰的混合物制取O 2的化学方程式为 ;收集![]() O2的装置可选择 (填
O2的装置可选择 (填![]() 字母)。完全反应后的固体残渣,通过以下四步实验操作可回收得到较纯净的二氧化锰(残渣中只有二氧化锰难于水)。正确操作的先后顺序是 (填写选项符号)。
字母)。完全反应后的固体残渣,通过以下四步实验操作可回收得到较纯净的二氧化锰(残渣中只有二氧化锰难于水)。正确操作的先后顺序是 (填写选项符号)。
a.烘干 b.溶解 c.过滤 d.洗涤
分离得到的二氧化锰在反应前后 保持不变。
(3)在实验室用大理石和稀盐酸制取CO2的实验装置中,F装置相对于B装置具有的优点是 ;
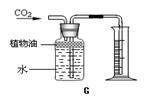
图G所示装置可用来测量生成CO2的体积,其中在水面
上放一层植物油的目的 ;![]()
请在图G方框内 画出补充的仪器,完成测量生成![]() CO2的体积装置
CO2的体积装置
(用黑色水笔画图)。取25克大理石与足量的稀盐酸完全反应, 收集到二氧化碳为8.8克,求参加反应的碳酸钙为多少摩尔?并求该大理石中碳酸钙的质量分数?(杂质不与酸反应)(写出计算过程) 。

长颈漏斗 2KClO3 ![]() 2KCl+3O2↑
2KCl+3O2↑
C或D bcda 质量和化学性质保持不变 F装置可以随时控制反应的发生或停止。(随开随用,随关随停) 防止二氧化碳溶于水并与水反应
要画出橡皮塞、导气管的位置才得分
 |
| (13)解 设反应需消耗xmol碳酸钙,其质量为m克 |
| n(CO2)=8.8÷44=0.2(mol) |
| CaCO3 + 2HCl→ CaCl2+ CO2 ↑+ H2O X=0.2(mol) |
m(CaCO3)=0.2×100=20(g)
CaCO3%=20/25×100%=80%






