摘要:27.实验室需配制4%的氢氧化钠溶液200g.并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数. (1)配制200g质量分数为4%的氢氧化钠溶液.需要氢氧化钠固体的质量为 ▲ g.水的体积为 ▲ mL(水的密度近似看作1g/cm3). (2)取10g此盐酸于烧杯中.逐滴滴加溶质质量分数为 4%的氢氧化钠溶液.用pH计 测定溶液的pH.得到的数据如下: 加入氢氧化钠 的体积/mL 0 1.0 8.0 9.5 10.5 12.0 16.5 烧杯中溶液pH 1.0 1.3 2.0 3.9 9.9 11.9 12.8 依据表中数据绘制出烧杯中溶液的pH与加入氢氧 化钠溶液体积(V)之间的变化关系图. (3)根据上图查出氢氧化钠与盐酸恰好完全反应时.所滴加氢氧化钠溶液的体积为 ▲ mL.A点所表示的溶液中溶质的化学式为 ▲ . (4)计算此瓶盐酸的溶质质量分数.(请写出计算过程.氢氧化钠溶液的密度按1.0g/mL计算) ▲
网址:http://m.1010jiajiao.com/timu3_id_31314[举报]
 实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数.
实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数.(1)配制200g质量分数为4%的氢氧化钠溶液,需要氢氧化钠固体的质量为
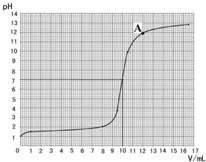
(2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)测定溶液的pH,得到的数据如下:
| 加入氢氧化钠 的体积/mL |
0 | 1.0 | 8.0 | 9.5 | 10.5 | 12.0 | 16.5 |
| 烧杯中溶液pH | 1.0 | 1.3 | 2.0 | 3.9 | 9.9 | 11.9 | 12.8 |
(3)根据上图查出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积为
(4)计算此瓶盐酸的溶质质量分数.(请写出计算过程.氢氧化钠溶液的密度按1.0g/mL计算)
 实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某盐酸溶液的溶质质量分数.
实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某盐酸溶液的溶质质量分数.
(1)配制200g质量分数为4%的氢氧化钠溶液.需要氢氧化钠固体的质量为______g.
(2)配制过程中除了用到天平、烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是______,
其作用是______.
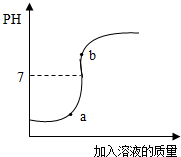
(3)用配得的氢氧化钠溶液与待测溶质质量分数的盐酸溶液反应,实验过程中溶液的pH变化曲线如图所示:
①要得到此变化曲线,所进行的操作是______(填字母).
A.将盐酸溶液滴加到氢氧化钠溶液中
B.将氢氧化钠溶液滴加到盐酸溶液中
②b点对应的溶液中的溶质为______(写化学式).
(4)恰好完全反应时,消耗4%的氢氧化钠溶液20g和25g某质量分数盐酸溶液,试计算该盐酸溶液中溶质的质量分数(请写出计算过程).______.
查看习题详情和答案>>
 实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数.
实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数.
(1)配制200g质量分数为4%的氢氧化钠溶液,需要氢氧化钠固体的质量为______g,水的体积为______mL(水的密度近似看作1g/cm3).
(2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)测定溶液的pH,得到的数据如下:
| 加入氢氧化钠 的体积/mL | 0 | 1.0 | 8.0 | 9.5 | 10.5 | 12.0 | 16.5 |
| 烧杯中溶液pH | 1.0 | 1.3 | 2.0 | 3.9 | 9.9 | 11.9 | 12.8 |
(3)根据上图查出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积为______mL,A点所表示的溶液中溶质的化学式为______.
(4)计算此瓶盐酸的溶质质量分数.(请写出计算过程.氢氧化钠溶液的密度按1.0g/mL计算)______. 查看习题详情和答案>>
实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某盐酸溶液的溶质质量分数。
(1)配制200g质量分数为4%的氢氧化钠溶液。需要氢氧化钠固体的质量为_________g。
(2)配制过程中除了用到天平、烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是__________,其作用是___________。
(3)用配得的氢氧化钠溶液与待测溶质质量分数的盐酸溶液反应,实验过程中溶液的pH变化曲线如图所示:
(1)配制200g质量分数为4%的氢氧化钠溶液。需要氢氧化钠固体的质量为_________g。
(2)配制过程中除了用到天平、烧杯、量筒、胶头滴管外,还需用到的玻璃仪器是__________,其作用是___________。
(3)用配得的氢氧化钠溶液与待测溶质质量分数的盐酸溶液反应,实验过程中溶液的pH变化曲线如图所示:
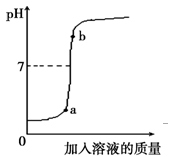
①要得到此变化曲线,所进行的操作是__________(填字母)。
A.将盐酸溶液滴加到氢氧化钠溶液中 B.将氢氧化钠溶液滴加到盐酸溶液中
②b点对应的溶液中的溶质为___________(写化学式)。
(4)恰好完全反应时,消耗4%的氢氧化钠溶液20g和25g某质量分数盐酸溶液,试计算该盐酸溶液中溶质的质量分数(请写出计算过程)_____________。
查看习题详情和答案>>
A.将盐酸溶液滴加到氢氧化钠溶液中 B.将氢氧化钠溶液滴加到盐酸溶液中
②b点对应的溶液中的溶质为___________(写化学式)。
(4)恰好完全反应时,消耗4%的氢氧化钠溶液20g和25g某质量分数盐酸溶液,试计算该盐酸溶液中溶质的质量分数(请写出计算过程)_____________。
实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数。
(1)配制200g质量分数为4%的氢氧化钠溶液,需要氢氧化钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。
 (2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
(2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)
测定溶液的pH,得到的数据如下:
| 加入氢氧化钠 的体积/mL | 0 | 1.0 | 8.0 | 9.5 | 10.5 | 12.0 | 16.5 |
| 烧杯中溶液pH | 1.0 | 1.3 | 2.0 | 3.9 | 9.9 | 11.9 | 12.8 |
依据表中数据绘制出烧杯中溶液的pH与加入氢氧
化钠溶液体积(V)之间的变化关系图。
(3)根据上图查出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积为 mL,A点所表示的溶液中溶质的化学式为 。
(4)计算此瓶盐酸的溶质质量分数。(请写出计算过程。氢氧化钠溶液的密度按1.0g/mL计算)
查看习题详情和答案>>