网址:http://m.1010jiajiao.com/timu3_id_310383[举报]
|
下列有关活化分子的说法正确的是 | |
| [ ] | |
A. |
增大反应物浓度可以提高活化分子百分数 |
B. |
增大压强一定能提高单位体积内活化分子总数 |
C. |
使用合适的催化剂可以降低活化分子的能量 |
D. |
升高温度一定能提高活化分子百分数 |
B.增大压强一定能提高单位体积内活化分子总数
C.使用合适的催化剂可以降低活化分子的能量
D.升高温度一定能提高活化分子百分数
2NO(g)+2CO(g)
| 催化剂 |
为了测定在某种催化剂作用下该反应的反应速率,t1℃下,在一等容的密闭容器中,某科研机构用气体传感器测得了不同时间的NO和CO的浓度如表1(CO2和N2的起始浓度为0).
表1
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/×10-4mol?L-1 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/×10-3mol?L-1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
(1)在上述条件下该反应能自发进行,则正反应必然是
(2)前3s内的平均反应速率v(N2)=
(3)假设在密闭容器中发生上述反应,达到平衡时改变下列条件,能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
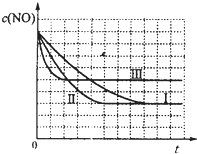
(4)研究表明:在使用等质量催化剂时,增大催化剂的比表面积可提高化学反应速率.根据表2设计的实验测得混合气体中NO的浓度随时间t变化的趋势如图1所示:
| 实验编号 | T/℃ | NO初始浓度/mol?L-1 | CO初始浓度/mol?L-1 | 催化剂的比表面积/m2?g-1 |
| ① | 350 | 1.20×10-2 | 5.80×10-2 | 124 |
| ② | 280 | 1.20×10-2 | 5.80×10-2 | 124 |
| ③ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
(5)已知:N2(g)+O2(g)=2NO(g)△H1=+180.5kJ?mol-1
2C(s)+O2(g)=2CO(g)△H2=-221.0kJ?mol-1
C(s)+O2(g)=CO2(g)△H3=-393.5kJ?mol-1
则处理汽车尾气反应中的a=
(6)用活性炭还原法也可以处理氮氧化物,有关反应为:C(s)+2NO(g)?N2(g)+CO2(g)△H4.向某密闭容器加入一定量的活性炭和NO,在t2℃下反应,
有关数据如表3.
| NO | N2 | CO | |
| 起始浓度mol.L-1 | 0.10 | 0 | 0 |
| 平衡浓度/mol.L-1 | 0.04 | 0.03 | 0.03 |
 CH3OH
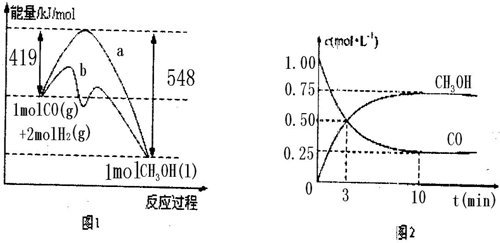
CH3OH图1表示该反应进行过程中的能量变化;图2表示100°C,在体积为2L的恒容容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况.
(1)已知CO的燃烧热为283kJ/mol,H2的燃烧热为285.8kJ/mol,写出表示CH3OH燃烧热的热化学方程式
| 3 |
| 2 |
| 3 |
| 2 |
(2)根据上图2计算:该温度下,反应CO(g)+2H2(g)
 CH3OH(g)△H<0的平衡常数为
CH3OH(g)△H<0的平衡常数为| 1 |
| 2 |
| 1 |
| 2 |
A.降低温度B.加催化剂
C.充入氩气,使体系压强增大D.再充入1molCO和2molH2
E.恒温恒容改为恒温恒压.
(10分)甲醇是一种非常好的燃料。熔点-97.8°C,沸点64.5°C。一定条件下,
CO与H2反应可制得甲醇:CO+2H2 CH3OH
图1表示该反应进行过程中的能量变化:
图2表示100°C,在体积为2L的恒容容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况。
(1)已知CO的燃烧热为283kJ/mol,H2的燃烧热为285.8kJ/mol,结合图1写出液态CH3OH燃烧热的热化学方程式 。
(2)根据上图2计算:该温度下,反应CO(g)+2H(g) CH3OH(g)的平衡常数为 ;10min后,容器内的压强变为原来的 倍;改变下列条件,能提高CO转化率的是 。
A.降低温度 B.加催化剂
C.充入氩气,使体系压强增大 D.再充入1molCO和2molH2
E.恒温恒容改为恒温恒压
(3)已知:CH3OH可以在一定条件下转化为HCOOH,HCOOH和CH3COOH性质相似。25°C,0.1mol/LHCOOH溶液的pH>1。室温下,向0.1mol/L的HCOOH溶液中滴加NaOH溶液,当溶液中离子浓度关系满足:
c(HCOO-)<c(Na+)时,则反应的情况可能为 。(填字母)
A.NaOH不足,HCOOH剩余
B.HCOOH与NaOH恰好完全反应
C.NaOH过量
查看习题详情和答案>>